-
矿山废水中含有大量的H2SO4和CuSO4,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水pH和重金属离子含量达到排放标准。
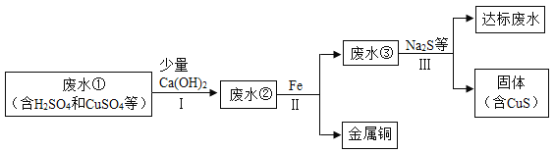
已知:步骤Ⅰ中Ca(OH)2与CuSO4并没有发生反应;CuSO4属于一种常见的重金属盐。
(1)步骤I发生反应的化学反应方程式为______。
(2)废水①中一定含有的阳离子有____。
(3)加入少量Ca(OH)2可以降低步骤Ⅱ中铁的消耗量,原因是____。
(4)步骤Ⅲ需加入Na2S才能使废水达到排放标准,由此推测废水③不达标的主要原因是其中还含有较多的____(填化学式或离子符号);达标废水pH比废水①pH ____(填“大”或“小”)。
-
矿山废水中含有大量的H2SO4和CuSO4,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水pH和重金属离子含量达到排放标准。
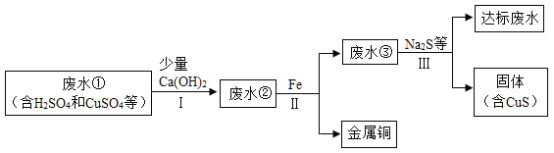
已知:步骤I中Ca(OH)2与CuSO4并没有发生反应; CuSO4 属于一种常见的重金属盐。
(1)废水①中一定含有的阳离子有______________。
(2)步骤II和步骤Ⅲ都需进行的操作是______________,实验室进行该操作是用到的一种玻璃仪器是______________。
(3)步骤II得到金属铜的化学反应方程式为______________。
(4)加入少量Ca(OH)2可以降低步骤II中铁的消耗量,原因是______________。
(5)步骤Ⅲ需加入Na2S才能使废水达到排放标准,由此推测废水③不达标的主要原因是其中还含有较多的______________,(填化学式或离子符号) ;达标废水pH比废水①pH____________(填“大”或“小”)。
-
矿山废水中含有大量的H2SO4和CuSO4,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水pH和重金属含量达到排放标准。
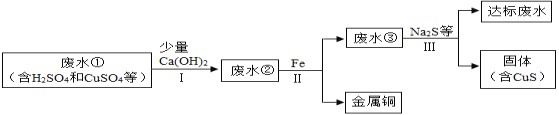
已知:步骤Ⅰ无蓝色沉淀生成。
(1)步骤Ⅱ和步骤Ⅲ都需进行的操作是________。
(2)步骤Ⅱ得到金属铜的反应的化学方程式为________。
(3)加入Ca(OH)2可以降低铁屑的消耗量,原因是_______(请用文字并结合化学方程式解释)。
(4)步骤Ⅲ需加入Na2S才能使废水达到排放标准,由此推测废水③不达标的主要原因是其中有___________。
-
矿山废水中含有大量的H2SO4和CuSO4,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水pH和重金属含量达到排放标准。

已知:步骤I无蓝色沉淀生成。
(1)步骤Ⅱ和步骤Ⅲ都需进行的操作是___________________;
(2)步骤Ⅱ得到金属铜的反应的化学方程式为___________________________;
(3)加入Ca(OH)2可以降低铁屑的消耗量,原因是_______________________;
(4)步骤Ⅲ需加入Na2S才能使废水达到排放标准,由此推测废水③不达标的主要原因是其中含有__________________。
-
矿山废水中含有大量的H2SO4和CuSO4,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水pH和重金属含量达到排放标准。
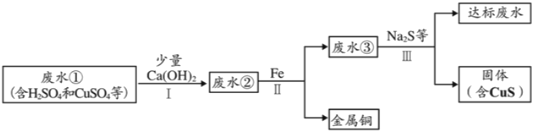
已知:步骤I无蓝色沉淀生成。
(1)步骤Ⅱ和步骤Ⅲ都需进行的操作是___________________;
(2)步骤Ⅱ得到金属铜的反应的化学方程式为___________________________;
(3)加入Ca(OH)2可以降低铁屑的消耗量,原因是_______________________;
(4)步骤Ⅲ需加入Na2S才能使废水达到排放标准,由此推测废水③不达标的主要原因是其中含有__________________。
-
矿山废水中含有大量的H2SO4和CuSO4,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水pH和重金属含量达到排放标准。

已知:步骤I无蓝色沉淀生成。
(1)步骤Ⅱ和步骤Ⅲ都需进行的操作是_______。
(2)步骤Ⅱ得到金属铜的反应的化学方程式为_______。
(3)加入Ca(OH)2可以降低铁屑的消耗量,原因是_______(请用文字并结合化学方程式解释)。
(4)步骤Ⅲ需加入Na2S才能使废水达到排放标准,由此推测废水③不达标的主要原因 是其中含有_______。
-
矿山废水中含有大量的H2SO4和CuSO4,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水pH和重金属含量达到排放标准。

已知:步骤I无蓝色沉淀生成。
(1)步骤Ⅱ和步骤Ⅲ都需进行的操作是_______。
(2)步骤Ⅱ得到金属铜的反应的化学方程式为_______。
(3)加入Ca(OH)2可以降低铁屑的消耗量,原因是_______(请用文字并结合化学方程式解释)。
(4)步骤Ⅲ需加入Na2S才能使废水达到排放标准,由此推测废水③不达标的主要原因 是其中含有_______。
-
某工厂的废水中含有大量的H2SO4和CuSO4,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水pH和重金属含量达到排放标准。
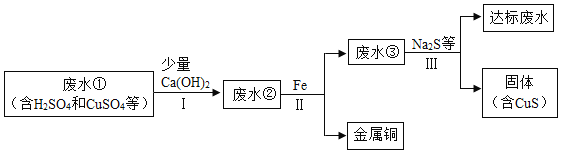
已知:步骤Ⅰ无蓝色沉淀生成。
(1)步骤Ⅱ和步骤Ⅲ都需进行的操作是____________。
(2)加入Ca(OH)2可以降低铁屑的消耗量,原因是__________(请用文字解释)。
(3)步骤Ⅲ需加入Na2S,由此推测废水③不达标的主要原因是其中含有____________。
-
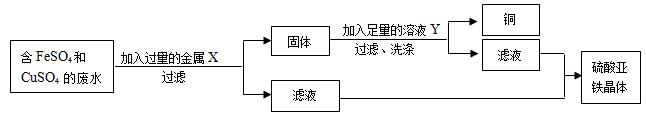
某校化学实验室废液桶中收集了溶解大量FeSO4和CuSO4(是重金属污染物之一)的废水,若直接排放到下水道既造成污染又造成浪费。某化学课外小组同学运用所学化学知识对废水进行处理,并回收硫酸亚铁晶体和铜,实验方案如下:
请回答:
①X是 ,将其加入废水后发生反应的化学方程式为________________ ;
②Y是 ,利用其除去固体中的杂
-
某化学兴趣小组同学模拟如图流程对含有大量H2SO4和CuSO4的废水进行处理,以回收金属铜,并使废水pH和重金属含量达到排放标准。
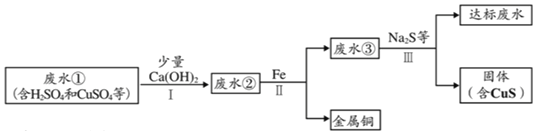
已知:步骤I无蓝色沉淀生成。
(1)Ca(OH)2的俗名为______;可以用来粉刷墙壁,墙壁先出汗,后变硬,写出相关化学反应方程式______。稀硫酸的工业用途有:______(举一例即可)。
(2)步骤Ⅱ和步骤Ⅲ都需进行的操作是______,该操作常用的玻璃仪器除玻璃棒、烧杯外,还有______;玻璃棒作用______。
(3)步骤Ⅱ得到金属铜的反应的化学方程式为______。









