-
某实验小组用石墨做电极进行电解水实验,为增加导电性,改用Ca(OH)2饱和溶液进行电解,实验时除两个电极均有气泡冒出外,溶液中还出现了白色浑浊,该小组对白色浑浊出现的原因进行了如下探究。
(猜想与假设)
①溶液温度升高导致Ca(OH)2析出而出现白色浑浊。
②水减少导致Ca(OH)2析出而出现白色浑浊。
③与石墨电极有关。
(查阅资料)
①Ca(OH)2的溶解度:20℃时为0.16g,100℃时为0.07g。
②在加热条件下铜能与氧气反应生成黑色的氧化铜。铜与稀硫酸不反应;氧化铜能与稀硫酸反应。
(进行实验)
| 实验 | 实验装置 | 主要实验操作 | 实验现象 |
| 1 | ﹣﹣ | 取20mLCa(OH)2 饱和溶液加热至沸腾 | 溶液中未出现白色浑浊 |
| 2 | 
| 取Ca(OH)2饱和溶液于烧杯中,加5ml水,通电3min | 烧杯中溶液体积几乎无明显变化,溶液中明显出现白色浑浊 |
| 3 | 更换石墨电极为铜电极,取Ca(OH)2 饱和溶液于烧杯中,通电3min | 与电源正极相连的铜电极变黑,溶液中未出现白色浑浊 |
(解释与结论)
(1)实验1得出的结论是_____。
(2)实验2通电3min后得到的溶液为_____(填“饱和”或“不饱和”)溶液。
(3)猜想与假设②不成立,依据的现象是_____。
(4)实验3中更换石墨电极为铜电极的目的是_____。
(反思与评价)
(5)为除去实验3中铜电极上的黑色物质,需要的试剂是_____。
(6)通过探究过程,用石墨做电极进行实验时,Ca(OH)2溶液中出现白色浑浊的原因是_____。
-
某实验小组用石墨做电极进行电解水实验,为增加导电性,改用Ca(OH)2饱和溶液进行电解,实验时除两个电极均有气泡冒出外,溶液中还出现了白色浑浊,该小组对白色浑浊出现的原因进行了如下探究。
(猜想与假设)
① 溶液温度升高导致Ca(OH)2析出而出现白色浑浊。
② 水减少导致Ca(OH)2析出而出现白色浑浊。
③ 与石墨电极有关。
(查阅资料)
① Ca(OH)2的溶解度:20℃时为0.16 g,100℃时为0.07 g。
② 在加热条件下铜能与氧气反应生成黑色的氧化铜。铜与稀硫酸不反应;氧化铜能与稀硫酸反应。
(进行实验)
| 实验 | 实验装置 | 主要实验操作 | 实验现象 |
| 1 | | 取20mLCa(OH)2 饱和溶液加热至沸腾 | 溶液中未出现白色浑浊 |
| 2 | 
| 取Ca(OH)2饱和溶液于烧杯中,加5 ml水,通电3 min | 烧杯中溶液体积几乎无明显变化,溶液中明显出现白色浑浊 |
| 3 | 更换石墨电极为铜电极,取Ca(OH)2 饱和溶液于烧杯中,通电3 min | 与电源正极相连的铜电极变黑,溶液中未出现白色浑浊 |
(解释与结论)
(1)实验1得出的结论是_______。
(2)实验2通电3 min后得到的溶液为_______(填“饱和”或“不饱和”)溶液。
(3)猜想与假设②不成立,依据的现象是_______。
(4)实验3中更换石墨电极为铜电极的目的是_______。
(反思与评价)
(5)为除去实验3中铜电极上的黑色物质,需要的试剂是______。
(6)通过探究过程,用石墨做电极进行实验时,Ca(OH)2溶液中出现白色浑浊的原因是_______。
-
某实验小组用石墨做电极进行电解水实验,为增加导电性,改用Ca(OH)2饱和溶液进行电解,实验时除两个电极均有气泡冒出外,溶液中还出现了白色浑浊,该小组对白色浑浊出现的原因进行了如下探究。
(猜想与假设)
① 溶液温度升高导致Ca(OH)2析出而出现白色浑浊。
② 水减少导致Ca(OH)2析出而出现白色浑浊。
③ 与石墨电极有关。
(查阅资料)
① Ca(OH)2的溶解度:20℃时为0.16 g,100℃时为0.07 g。
② 在加热条件下铜能与氧气反应生成黑色的氧化铜。铜与稀硫酸不反应;氧化铜能与稀硫酸反应。
(进行实验)
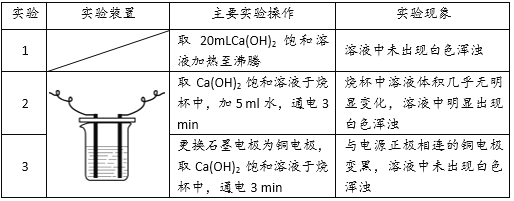
(解释与结论)
(1)实验1得出的结论是_______。
(2)实验2通电3 min后得到的溶液为_______(填“饱和”或“不饱和”)溶液。
(3)猜想与假设②不成立,依据的现象是_______。
(4)实验3中更换石墨电极为铜电极的目的是_______。
(反思与评价)
(5)为除去实验3中铜电极上的黑色物质,需要的试剂是______。
(6)通过探究过程,用石墨做电极进行实验时,Ca(OH)2溶液中出现白色浑浊的原因是_______。
-
某实验小组用石墨做电极进行电解水实验,为增加导电性,改用氢氧化钙饱和溶液进行电解,实验时除两个电极均有气泡冒出外,在正极石墨电极的附近溶液中还出现了白色浑浊,该小组对白色浑浊出现的原因进行了如下探究。
[资料]
Ⅰ.氢氧化钙的溶解度曲线如图所示。

Ⅱ.氢氧化钙饱和溶液通电后温度约上升5℃。
[猜想]
①电解过程中溶液温度升高导致Ca(OH)2析出而出现白色浑浊。
②电解过程中水减少导致Ca(OH)2析出而出现白色浑浊。
③与石墨电极(主要成分是碳)有关。
[实验]
| 实验 | 实验装置 | 主要实验操作 | 实验现象 |
| 1 | | 取10mL Ca(OH)2饱和溶液,稍加热,溶液温度上升5℃ | 溶液中未出现白色浑浊 |
| 2 | 
| 用石墨做电极,取Ca(OH)2饱和溶液于水槽中,通电2分钟 | a、b试管中都有气泡产生;a试管中溶液未出现白色浑浊;b试管中溶液明显出现白色浑浊 |
| 3 | 更换石墨电极为铜电极,取Ca(OH)2饱和溶液于水槽中,通电2分钟 | a、b试管中都有气泡产生;与电源正极相连的铜电极变墨,a、b试管中溶液未出现白色浑浊 |
(1)Ca(OH)2的溶液度随温度升高而__________(填“减少”或“增大”);实验1中当液温度上升5℃后得到的溶液为Ca(OH)2 __________(填“饱和”或“不饱和”)溶液。
(2)实验1得出的结论是___________________________________________________________。
(3)实验2,取b试管中白色浑浊溶液,加10mL水,振荡,发现试管中白色浑浊不溶解,据此证明猜想_______(填序号)不合理。
(4)实验3中更换石墨电极为铜电极的目的是__________________________________________;与电源正极相连的铜电极变黑的原因是_____________________________________________(用化学方程式表示);为除去铜电极上的黑色物质,需要的试剂是_____________(写一种即可)。
(5)通过探究过程,用石墨做电极进行实验时,正极石墨电极附近Ca(OH)2溶液出现白色浑浊的原因是__________________________________________________________________________。
-
某实验小组用石墨做电极进行电解水实验,为增加导电性,改用氢氧化钙饱和溶液进行电解,实验时除两个电极均有气泡冒出外,在正极石墨电极的附近溶液中还出现了白色浑浊,该小组对白色浑浊出现的原因进行了如下探究。
[资料]
Ⅰ.氢氧化钙的溶解度曲线如图所示。

Ⅱ.氢氧化钙饱和溶液通电后温度约上升5℃。
[猜想]
①电解过程中溶液温度升高导致Ca(OH)2析出而出现白色浑浊。
②电解过程中水减少导致Ca(OH)2析出而出现白色浑浊。
③与石墨电极(主要成分是碳)有关。
[实验]
| 实验 | 实验装置 | 主要实验操作 | 实验现象 |
| 1 | | 取10mL Ca(OH)2饱和溶液,稍加热,溶液温度上升5℃ | 溶液中未出现白色浑浊 |
| 2 | 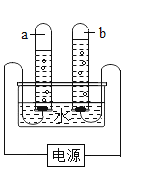
| 用石墨做电极,取Ca(OH)2饱和溶液于水槽中,通电2分钟 | a、b试管中都有气泡产生;a试管中溶液未出现白色浑浊;b试管中溶液明显出现白色浑浊 |
| 3 | 更换石墨电极为铜电极,取Ca(OH)2饱和溶液于水槽中,通电2分钟 | a、b试管中都有气泡产生;与电源正极相连的铜电极变黑,a、b试管中溶液未出现白色浑浊 |
(1)Ca(OH)2的溶液度随温度升高而__________(填“减少”或“增大”);实验1中当液温度上升5℃后得到的溶液为Ca(OH)2 __________(填“饱和”或“不饱和”)溶液。
(2)实验1得出的结论是___________________________________________________________。
(3)实验2,取b试管中白色浑浊溶液,加10mL水,振荡,发现试管中白色浑浊不溶解,据此证明猜想_______(填序号)不合理。
(4)实验3中更换石墨电极为铜电极的目的是__________________________________________;与电源正极相连的铜电极变黑的原因是_____________________________________________(用化学方程式表示);为除去铜电极上的黑色物质,需要的试剂是_____________(写一种即可)。
(5)通过探究过程,用石墨做电极进行实验时,正极石墨电极附近Ca(OH)2溶液出现白色浑浊的原因是__________________________________________________________________________。
-
实验小组同学验证Ca(OH)2溶液导电性的实验装置如图1所示。实验观察到灯泡变亮的同时,两个电极上均有气体产生,且阳极附近出现了白色浑浊。小组同学对白色浑浊物的成分进行了如下探究。
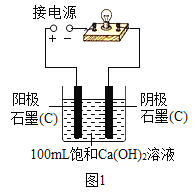
(猜想一)甲同学认为:白色浑浊物是Ca(OH)2。
(实验一)为了验证甲同学的猜想,进行如下实验。取少量白色浊液于试管中,加入足量水,充分振荡,观察到仍有白色浑浊。
(猜想二)乙同学认为:白色浑浊物中含有CaCO3。
(实验二)为了验证乙同学的猜想,进行如下实验。取少量白色浊液于试管中,滴加稀盐酸,白色浑浊消失,没有观察到有气泡产生。
(实验三)为了进一步验证乙同学的猜想,进行如下实验。
| 实验装置图 | 实验操作 | 实验现象 |
| 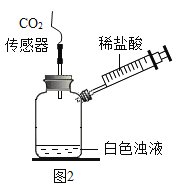
| 将注射器内稀盐酸推入瓶中,并用二氧化碳传感器测得装置内二氧化碳的体积分数 | I.白色浑浊消失,没有观察到有气泡产生 II.检测到二氧化碳含量随时间的变化如下图所示 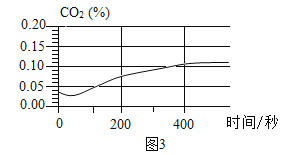
|
(解释与结论)
(1)用石墨电极验证Ca(OH)2溶液的导电性实验时,两个电极上产生大量气体,发生的是电解水的反应,写出反应的化学方程式________。
(2)甲同学提出白色浑浊为Ca(OH)2的理由是_____。
(3)由实验三得出的结论是____,相关反应的化学方程式为____。
(反思与交流)
(4)实验二中没有观察到明显气泡的可能原因是____。
(5)丙同学为了进一步探究白色浑浊物产生的原因,用铂(Pt)电极代替石墨(C)电极完成图1所示实验,其目的是________。
-
从电解水实验中我们可以获得很多的信息.下列说法正确的是( )
A.电极上有气泡产生,两支玻璃管内气体的质量比约为2:1
B.水是由氢气和氧气组成的
C.在电解水实验中加入少量的氢氧化钠是为了增加水的导电性
D.与电源负极相连的玻璃管中的气体能使带火星的木条复燃
-
为验证水的组成元素及探究水在电极端所发生的变化,兴趣小组用如图1所示装置(夹持仪器省略)进行实验:
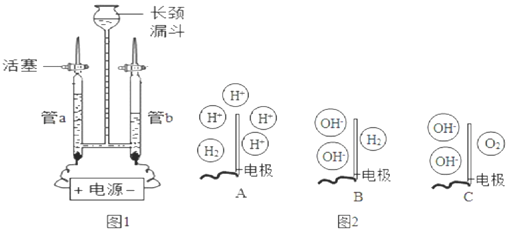
查阅资料:硫酸钠可增强水的导电性,可认为在电解水过程中不反应,硫酸钠溶液呈中性。
Ⅰ.验证水的组成元素
步骤一:向长颈漏斗中加水(含少量Na2SO4)至充满管a和管b,关闭活塞,接通电源,一段时间后关闭电源。
步骤二:检验管中气体。
(1)电解过程观察到的现象有:_____。
(2)用燃着的木条分别置于玻璃管尖嘴口,打开活塞,若观察到气体燃烧产生淡蓝色火焰,则证明气体为H2;若观察到_____,则证明气体为O2。
(3)若要确定水中氢、氧元素的原子个数比,需要测定_____。
Ⅱ.探究水在电极端所发生的变化
步骤一:向装置中重新加滴有酚酞的水(含少量Na2SO4)至充满管a和管b,保持活塞打开,接通电源,一段时间后关闭电源。
(1)实验中发现管b电极附近的溶液迅速变红,管a电极附近的溶液仍为无色,用pH试纸测定管a电极附近的溶液,pH小于7。说明管a电极附近的溶液呈_____性(选填“酸”、“碱”或“中”),管b电极附近的溶液呈碱性。
(2)图2中能表示电解时管b中水在电极端所发生变化的结果的是_____(填对应选项的字母)。
-
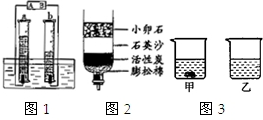
(1)按图1简易装置电解水,A、B是电源的两个电极.
①通电一段时间后,量筒a中收集到的气体是________,B是电源的________极.
②电解水的实验中,加入适量的NaOH可以增加水的导电性而使电解速率加快.在加了氢氧化钠的水中通电一段时间后,溶液中的变化是________.
A.溶质质量减少 B.溶剂质量减少 C.溶液质量增加 D.溶质质量分数增大
(2)化学是研究物质的组成、结构、性质及其变化规律的基础自然科学.请回答下列问题:
①从组成角度看:水是由________组成的﹔
②从微粒角度看:水是由________构成的﹔
③从资源角度看:水是生命之源,图2是用来净化河水的简易装置,下列说法错误的是________.
A.水是一种重要的溶剂 B.利用图2装置能把硬水变为软水 C.通过过滤可以除去水中所有的杂质 D.利用图2装置能对水杀菌消毒.
④从变化角度看:水通电分解生成最理想的能源-氢气,电解一定量的水,当其中一个电极产生5ml气体时,另一个电极产生的气体体积可能是________ml.
(3)水是很好的溶剂.下表列出了氯化铵和氯化钠的溶解度,请回答问题:
①40℃时,向两个分别盛有45gNH4Cl和NaCl的烧杯中,各加入100g的水,充分溶解后,结果如图3所示,则乙烧杯中的溶质是________.
②采用一种操作方法,将上述烧杯中的固体全部溶解,变为不饱和溶液.在这个过程中,下列说法正确的是________.(填字母)
A.溶剂质量不变 B.溶液中溶质的质量分数一定减少 C.溶液质量一定增大 D.溶液中溶质的质量分数可能增大
| 温度/℃ | | 20 | 40 | 60 | 80 | 100 |
溶解度
/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 |
-
下列说法错误的是 ( )
A.用肥皂水鉴别硬水和软水
B.碳的可燃性决定了碳可做燃料
C.石墨的导电性决定了石墨可做电极
D.在电解水实验中正负极气体体积比是2:1










