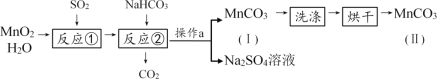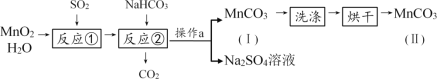-
以软锰矿粉(主要含MnO2,还有少量Fe2O3)为原料制取MnCO3的流程如图1.
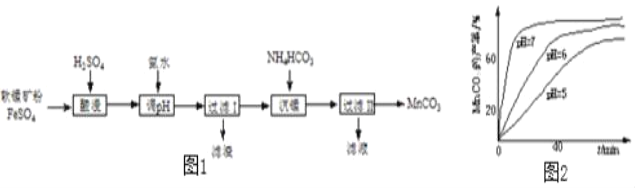
(1)“酸浸”时发生的反应有2FeSO4+MnO2+2H2SO4=_____+MnSO4+2H2O和_____。
(2)“过滤Ⅰ”所得滤渣的主要成分是_____。
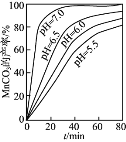
(3)“沉锰”时测得MnCO3的产率与溶液pH、反应时间t的关系如图2,反应要控制pH=_____,其理由是_____、_____。
(4)“过滤Ⅱ”所得滤液中溶质的主要成分是_____。
(5)为测定某软锰矿中MnO2的质量分数,称取2.0 g软锰矿样品,加入3.35 g草酸钠(Na2C2O4)固体,再加足量稀硫酸(杂质不参加反应),充分反应后,过量的Na2C2O4用31.6 g/L KMnO4溶液进行反应,当滴入10.0 mL KMnO4溶液时恰好完全反应。
已知:①MnO2+Na2C2O4+2H2SO4=MnSO4 +2CO2↑+2H2O+Na2SO4 ;②2KMnO4+5Na2C2O4+8H2SO4=2MnSO4+5Na2SO4+K2SO4+10CO2↑+8H2O.
求该软锰矿中MnO2的质量分数。_____(相对分子质量:KMnO4 158;Na2C2O4 134;MnO2 87)
-
以软锰矿粉(主要含MnO2,还有少量Fe2O3)为原料制取MnCO3的流程如图1.
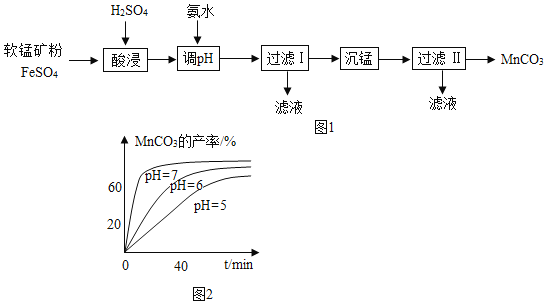
(1)“酸浸”时发生的反应有2FeSO4+MnO2+2H2SO4=_____+MnSO4+2H2O和_____。
(2)“过滤Ⅰ”所得滤渣的主要成分是_____。
(3)“沉锰”时测得MnCO3的产率与溶液pH、反应时间t的关系如图2,反应要控制pH=_____,其理由是_____、_____。
(4)“过滤Ⅱ”所得滤液中溶质的主要成分是_____。
(5)为测定某软锰矿中MnO2的质量分数,称取2.0 g软锰矿样品,加入3.35 g草酸钠(Na2C2O4)固体,再加足量稀硫酸(杂质不参加反应),充分反应后,过量的Na2C2O4用31.6 g/L KMnO4溶液进行反应,当滴入10.0 mL KMnO4溶液时恰好完全反应。
已知:①MnO2+Na2C2O4+2H2SO4=MnSO4 +2CO2↑+2H2O+Na2SO4 ;②2KMnO4+5Na2C2O4+8H2SO4=2MnSO4+5Na2SO4+K2SO4+10CO2↑+8H2O.
求该软锰矿中MnO2的质量分数。_____(相对分子质量:KMnO4 158;Na2C2O4 134;MnO2 87)
-
碳酸锰(MnCO3)是一种高性能磁性材料。以软锰矿粉(主要含MnO2,还含有少量的Fe2O3、Al2O3等杂质)为原料制取MnCO3的流程如下:
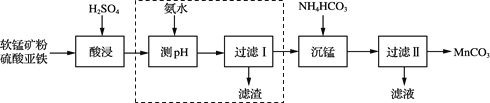
已知“沉锰”反应为MnSO4+2NH4HCO3===(NH4)2SO4+MnCO3↓+H2O+CO2↑
(1)“酸浸”时发生的主要反应为2FeSO4+MnO2+2H2SO4===X+MnSO4 +2H2O,X的化学式为______;“酸浸”时还发生的反应有______(任写一个化学方程式)。
(2)流程中虚线内工序的主要目的是______。“沉锰”工序中,如图为MnCO3的产率与溶液pH、反应时间t的关系,由图可知应控制溶液的pH 为______。
(3)“过滤Ⅱ”后续的操作为洗涤、干燥,证明MnCO3固体已经洗涤干净的操作是______。
-
MnCO3用作涂料和清漆的颜料。MnCO3不溶于水,100℃时开始分解。以软锰矿(主要成分MnO2)为原料制备高纯MnCO3的流程如下:
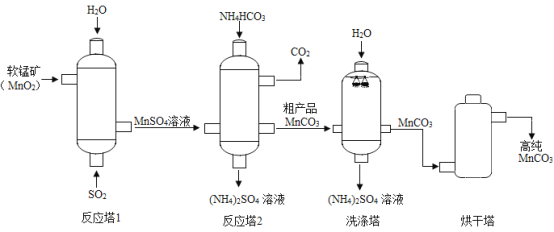
(1)反应塔1中的反应为: ,其中化合价发生改变的元素是______。
,其中化合价发生改变的元素是______。
(2)烘干塔中需选择“低温”干燥的原因是__________。
-
MnCO3用作涂料和清漆的颜料。MnCO3不溶于水,100℃时开始分解。以软锰矿(主要成分MnO2)为原料制备高纯MnCO3的流程如下:
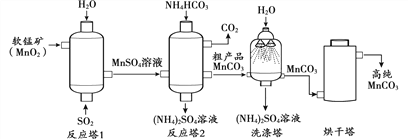
(1)反应塔1中的反应为:MnO2+SO2==MnSO4,其中化合价发生改变的元素是________。
(2)洗涤塔中喷水的目的是__________。
(3)烘干塔中需选择“低温”干燥的原因是_______________。
(4)上述流程中的产品除高纯MnCO3外,还有______________。
-
我国某科研团队以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料,制取高纯碳酸锰,工艺流程如下图:
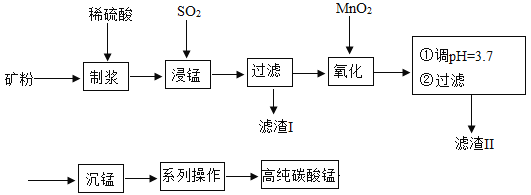
已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为_____、_____(写化学式) ;
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:_____, 该反应中共有_____种元素的化合价发生了改变。
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:_____。
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为_____%(保留一位小数)
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
| 矿酸比 | 温度/(℃) | 浸出率/(%) |
| 1 | 1:0.5 | 60 | 80.2 |
| 2 | 1:0.5 | 80 | 83.8 |
| 3 | 1:0.6 | 60 | X |
| 4 | 1:0.6 | 80 | 91.8 |
表中 X 最有可能的数值为_____。
a.79.7 b.80.8 c.87.6 d.92.8
-
我国某科研团队以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料,制取高纯碳酸锰,工艺流程如下图:
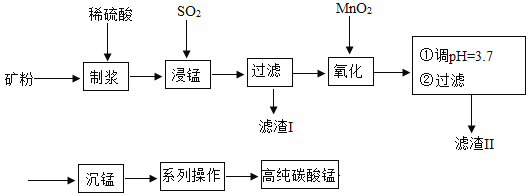
已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为_____、_____(写化学式) ;
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:_____, 该反应中共有_____种元素的化合价发生了改变。
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:_____。
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为_____%(保留一位小数)
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
| 矿酸比 | 温度/(℃) | 浸出率/(%) |
| 1 | 1:0.5 | 60 | 80.2 |
| 2 | 1:0.5 | 80 | 83.8 |
| 3 | 1:0.6 | 60 | X |
| 4 | 1:0.6 | 80 | 91.8 |
表中 X 最有可能的数值为_____。
a.79.7 b.80.8 c.87.6 d.92.8
-
某化学活动小组在实验室以MnO2固体为原料制取少量MnCO3,基本流程如下:
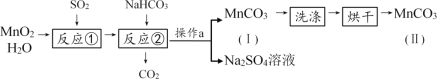
已知:MnSO4与MnCl2都可溶于水;MnCO3难溶于水且在100℃时开始分解。
(1)反应①为化合反应,产物为MnSO4。该反应的化学方程式为_______,下列物质中不能与MnSO4反应的有_______。
A.稀硫酸 B.BaCl2 C.盐酸 D.Na2CO3
(2)操作a要用到的实验用品中,除玻璃仪器外,还有_____(填具体的实验用品)。
(3)产品MnCO3(Ⅱ) 比MnCO3(Ⅰ) 更纯净,原因是产品MnCO3(Ⅰ) 经过洗涤、烘干以后,表面附着的H2O及__________(填化学式)等杂质已被除去。
(4)为了获得纯净的MnCO3,烘干时需要控制的条件是________。
-
某化学活动小组在实验室以MnO2固体为原料制取少量MnCO3,基本流程如下:
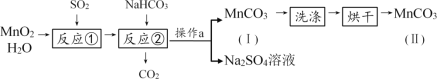
已知:MnSO4与MnCl2都可溶于水;MnCO3难溶于水且在100℃时开始分解。
(1)反应①为化合反应,产物为MnSO4。该反应的化学方程式为_______,下列物质中不能与MnSO4反应的有_______。
A.稀硫酸 B.BaCl2 C.盐酸 D.Na2CO3
(2)操作a要用到的实验用品中,除玻璃仪器外,还有_____(填具体的实验用品)。
(3)产品MnCO3(Ⅱ) 比MnCO3(Ⅰ) 更纯净,原因是产品MnCO3(Ⅰ) 经过洗涤、烘干以后,表面附着的H2O及__________(填化学式)等杂质已被除去。
(4)为了获得纯净的MnCO3,烘干时需要控制的条件是________。
-
高锰酸钾主要用于化工、制药等工业。以软锰矿(主要成分MnO2)为原料生产高锰酸钾的流程如图所示。

(1)在烘炒锅中进行原料混合,混合前应将软锰矿粉碎,其作用是_________。
(2)平炉中发生反应生成K2MnO4和H2O,则参加反应的物质有_________。
(3)电解槽中发生反应的化学方程式为2K2MnO4+ 2H2O 2KMnO4+ 2KOH + H2↑,该反应前后化合价发生变化的元素有_________。
2KMnO4+ 2KOH + H2↑,该反应前后化合价发生变化的元素有_________。