某课外活动小组进行如下实验探究:测定水中氢氧元素质量比。(已知:),根据下图进行实验,反应后测得甲中玻璃管(含药品)质量减少ag,乙中U形管(含药品)质量增加bg。
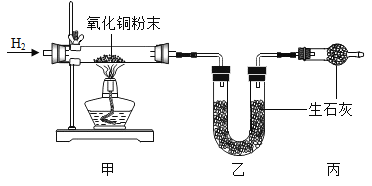
①水中氢、氧元素的质量比是__________(用含a、b的式子表示)。
②下列因素中,对测定结果有影响的是__________(填序号)。
ACuO粉末不干燥
BCuO没有完全转化为Cu
C没有丙装置
九年级化学实验题中等难度题
某课外活动小组进行如下实验探究:测定水中氢氧元素质量比。(已知:),根据下图进行实验,反应后测得甲中玻璃管(含药品)质量减少ag,乙中U形管(含药品)质量增加bg。

①水中氢、氧元素的质量比是__________(用含a、b的式子表示)。
②下列因素中,对测定结果有影响的是__________(填序号)。
ACuO粉末不干燥
BCuO没有完全转化为Cu
C没有丙装置
九年级化学实验题中等难度题
某课外活动小组进行如下实验探究:测定水中氢氧元素质量比。(已知:),根据下图进行实验,反应后测得甲中玻璃管(含药品)质量减少ag,乙中U形管(含药品)质量增加bg。

①水中氢、氧元素的质量比是__________(用含a、b的式子表示)。
②下列因素中,对测定结果有影响的是__________(填序号)。
ACuO粉末不干燥
BCuO没有完全转化为Cu
C没有丙装置
九年级化学实验题中等难度题查看答案及解析
测定水中氢、氧元素的质量比。根据下图进行实验,反应后测得甲中玻璃管(含药品)质量减少a g,乙中U形管(含药品)质量增加b g。
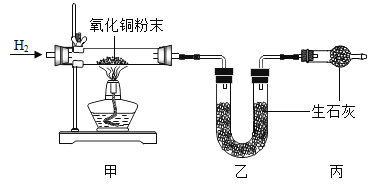
(1)水中氢、氧元素的质量比是__(用含a、b的式子表示)。
(2)下列因素中,对测定结果有影响的是____(填序号)。
A CuO粉末不干燥
B CuO没有完全转化为Cu
C 没有丙装置
九年级化学填空题中等难度题查看答案及解析
(7 分)小明上网阅读时得知根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量(Ar)的实验。小明很感兴趣,和化学兴趣小组的同学设计了如下探究活动,请结合下图回答问题。
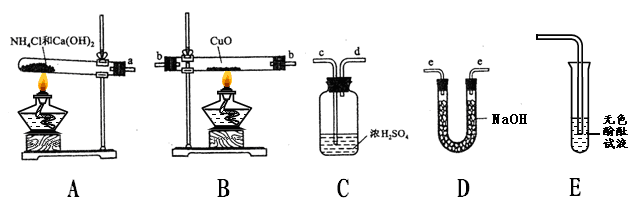
(1)实验室利用氯化铵和氢氧化钙固体之间的复分解反应制取氨气。小明将A与E连接,观察到无色酚酞试液变红,说明氨气显________(填“酸性”、“中性”、或“碱性”)。A中发生反应的化学方程式为________。
(2)小刚将纯净干燥的氨气通入B中,观察到玻璃管内黑色固体变为亮红色,管口有液滴,同时生成空气中含量最多的气体,B中发生反应的化学方程式为________。
(3)小组同学测定铜元素相对原子质量(Ar)的实验设想是:先称量反应物CuO的质量M(CuO),反应完全后测定生成物水的质量M(H2O),由此计算出Cu的相对原子质量。
①小组每位同学从所提供的仪器中选择并组装了一套用于本实验的装置,其中简单、合理的是(填序号,装置可重复使用)________。
A.acdbbeecd B.aeebbcdee C.aeebbeecd D.abbeecd
②在本实验中,使测定结果Ar(Cu)偏大的是_______________ (填序号);
A.CuO未完全起反应
B.CuO不干燥
C.氢氧化钠固体不干燥
D.CuO中混有不反应的杂质
E.NH4C1与Ca(OH)2混合物不干燥
③在本实验中,还通过测定_______________和_____________的质量达到目的。
九年级化学探究题中等难度题查看答案及解析
(12分)某化学小组利用如图所示装置测定铜锌合金样品中锌的质量分数.C为有刻度的玻璃仪器,可装
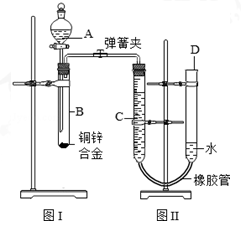
合适的液体,根据液面位置变化测定气体体积.探究过程如下:
(1)连接实验装置并检查装置气密性,将药品、水装入各仪器中.检查图Ⅱ装置气密性的方法是 .
(2)调整好装置后,再进行的操作还有:
① 记录C的液面位置;
② 待B中不再有气体产生并恢复至室温;
③ 由A向B滴加足量稀硫酸;
④ 调节D的位置至C、D中液面高度一致,记录C中液面位置.上述操作的合理顺序是 (填序号).B中发生反应的化学方程式是 。
(3)经一系列操作,准确称量并记录B中剩余固体物质的质量.“一系列操作”是指过滤、 、 .
(4)计算铜锌合金样品中锌的质量分数.该小组的甲同学根据完全反应后B中固体物质的质量计算样品中锌的质量分数;乙同学依据完全反应后生成气体的体积,并利用该气体在常温下的密度,根据化学方程式进行相关计算,得到样品中锌的质量分数.甲、乙同学要计算出锌的质量分数,都缺少的一个数据是 。
(5)重新实验后,甲、乙同学分别求出锌的质量分数.通过误差分析,化学小组发现乙同学所用数据会导致计算结果偏大,原因是 .
九年级化学填空题中等难度题查看答案及解析

九年级化学解答题中等难度题查看答案及解析
黄铁矿(主要成分为FeS2 ,杂质不含硫元素)是我国大多数硫酸厂制取硫酸的主要原料。化学课外活动小组为测定某黄铁矿中FeS2含量,进行了如下的实验探究(假设每步反应均完全),
[查阅资料]
①
②
[实验探究]
I .称取1.60 g黄铁矿样品放入如图①所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。
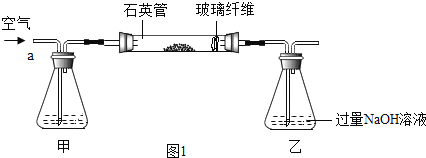
II.反应结束后,将乙瓶中的溶液进行如图②处理。
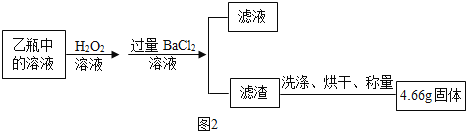
[问题讨论]
(1)I装置中甲瓶内盛放的试剂是氢氧化钠溶液,其作用是_____。
[含量测定]
(2)II中最终得到的4.66 g固体是_____(填物质的化学式);
(3)该黄铁矿中FeS2 的质量分数_____。
[交流反思]
(4)如果缺少甲装置,则最终测得FeS2的质量分数将会_____(填“偏大”“偏小”或“不变”);
(5) II中证明所加BaCl2溶液过量的方法是_____。
九年级化学科学探究题困难题查看答案及解析
某化学兴趣活动小组为测定空气中氧气的含 量,进行如下探究实验:
如图所示,在一个具有刻度和可以滑动的活塞的玻璃容器中放入一粒白磷(白磷燃烧和红磷一样发生的是相同的反应,不同的是所需的最低温度为40℃),将玻璃容器固定好,放在盛有85℃热水的烧杯上。请回答下列问题:

实验中可以看到玻璃容器内白磷燃烧时的 现象是 ,该反应的文字表达式是 。实验结束后,恢复至常温,活塞应停在刻度__________处,出现该现象的原因是:白磷燃烧消耗了空气中气态的__________而生成了固态的________,从而使玻璃容器内的气体体积__________(填“增大”、“减小”或“不变”)。
此反应中白磷要过量,目的是_____________________________。
九年级化学填空题中等难度题查看答案及解析
九年级化学填空题中等难度题查看答案及解析
黄铁矿(主要成分为FeS2,杂质不含硫元素)是我国大多数硫酸厂制取硫酸的主要原料。化学课外活动小组为测定某黄铁矿中FeS2含量进行了如下的实验探究(假设每步反应均完全)。
【查阅资料】 ①4FeS2+11O2 2Fe2O3+8SO2
②Na2SO3+H2O2=Na2SO4+H2O
【实验探究】
Ⅰ. 称取2.40 g黄铁矿样品放入下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。
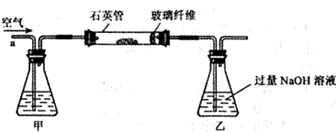
Ⅱ. 反应结束后,将乙瓶中的溶液进行如下处理:
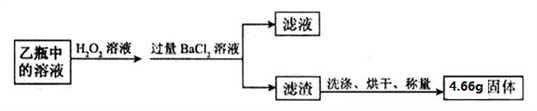
【问题讨论】
(1)Ⅰ装置中甲瓶内盛放的试剂是氢氧化钠溶液,其作用是______________。
(2)Ⅰ装置中乙瓶内发生反应的化学反应方程式是____________________。
【含量测定】
(3)计算该黄铁矿中FeS2的质量分数__________________。(请写出计算过程)
【交流反思】
(4)如果缺少甲装置,则最终测得FeS2的质量分数将会________________(填“偏大”“偏小”或“不变”)。
(5)Ⅱ中检验滤渣是否洗涤干净的方法是,取最后一次洗涤液,加入_____________,说明已洗涤干净。
【拓展应用】
工业上以黄铁矿为原料生产硫酸的工艺流程图如下所示:
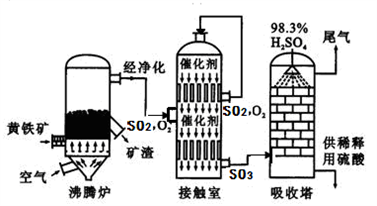
(6)接触室中发生反应的化学方程式为________________________。化学实验室常需要用到较稀的硫酸,把浓硫酸稀释的操作是_______________________________________,硫酸是一种重要的化工产品,用途十分广泛,请写出稀硫酸的一种用途______________________。
(7)依据生产硫酸的工艺流程图,下列说法正确的是_______________(填字母)。
A.为使黄铁矿充分燃烧,需将其粉碎 B.催化剂能够提高SO2的反应速率和产量
C.沸腾炉排出的矿渣可供炼铁 D.吸收塔中为了提高吸收效率,采用喷淋的方式
九年级化学信息分析题中等难度题查看答案及解析
黄铁矿(主要成分为FeS2,杂质不含硫元素)是我国大多数硫酸厂制取硫酸的主要原料。化学课外活动小组为测定某黄铁矿中FeS2含量进行了如下的实验探究(假设每步反应均完全)。
【查阅资料】
①4FeS2+11O2 2Fe2O3+8SO2
②Na2SO3+H2O2=Na2SO4+H2O
③Na2SO4+BaCl2=BaSO4 ↓+2NaCl
④Na2CO3+BaCl2=BaCO3 ↓+2NaCl
【实验探究】
Ⅰ. 称取1.60 g黄铁矿样品放入下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。
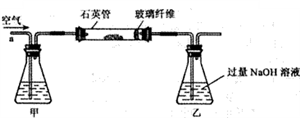
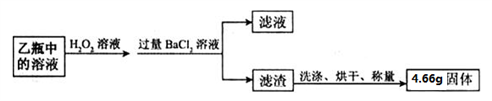
Ⅱ. 反应结束后,将乙瓶中的溶液进行如下处理:
【问题讨论】
(1)Ⅰ中装置中甲瓶内盛放的试剂是氢氧化钠溶液,其作用是____________。
【含量测定】
(2)Ⅱ中最终得到的4.66g固体是_________(填物质的化学式)。
(3)计算该黄铁矿中FeS2的质量分数。_________(请写出计算过程)
【交流反思】
(4)如果缺少甲装置,则最终测得FeS2的质量分数将会_________(填“偏大”“偏小”或“不变”)。
(5)Ⅱ中证明所加BaCl2溶液过量的方法是_________________。
【拓展应用】
工业上以黄铁矿为原料生产硫酸的工艺流程图如下所示:
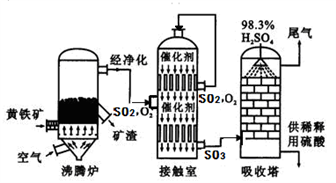
(6)接触室中发生反应的化学方程式为_________________。化学实验室现有质量分数为98%的浓硫酸,但在实验中常需要用到较稀的硫酸。要把100g上述浓硫酸稀释成质量分数为10%的硫酸,需要水的质量是________g,稀释时,应将_________沿烧杯内壁慢慢注入_______中,并不断用玻璃棒搅拌。硫酸是一种重要的化工产品,用途十分广泛,请写出稀硫酸的一种用途_______________。
(7)依据生产硫酸的工艺流程图,下列说法正确的是________(填字母)。
A.为使黄铁矿充分燃烧,需将其粉碎
B.催化剂能够提高SO2的反应速率和产量
C.SO2可做为生产硫酸的原料循环再利用
D.沸腾炉排出的矿渣可供炼铁
九年级化学信息分析题极难题查看答案及解析