-
(5分)食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富。
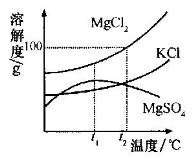
(1)海水晒盐的原理是_ ;
(2)晒盐过程中得到粗盐和卤水。卤水的主要成分及其溶解度的变化如右图t2℃时,MgCl2的溶解度为_ g.将t2℃时MgCl2、KCl和MgS04三种物质的饱和溶液分别降温至t1℃时,析出的晶体是_ (填物质化学式);
(3)将纯净的氯化钠固体配制成溶液。20℃时,向4个盛有50g水的烧杯中,分别加人一定质量的氯化钠并充分溶解。4组实验数据如下表:
| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化納的质量/g | 4.5 | 9 | 18 | 20 |
| 溶液质量/g | 54.5 | 59 | 68 | 68 |
若将②中得到的溶液稀释成质量分数为0.9%的生理盐水,需加水的质量是__ _g;
关于上述实验的叙述不正确的是_ (填字母序号)。
A.①②所得溶液是该温度下的不饱和溶液
B.③④所得溶液溶质的质量分数相等
C.20℃时,氯化钠的溶解度为36g
D.20℃时,将④恒温蒸发25g水,过滤得18g固体
-
食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富。
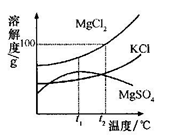
(1)海水晒盐的原理是 。
(2)晒盐过程中得到粗盐和卤水。卤水的主要成分及其溶解度的变化如右图。t2℃时,MgCl2的溶解度为 g。将t2℃时MgCl2、KCl和MgS04三种物质的饱和溶液分别降温至t1℃时,析出晶体的是 (填化学式)。
(3)将纯净的氯化钠固体配制成溶液。20℃时,向4个盛有50g水的烧杯中,分别加入一定质量的氯化钠并充分溶解。4组实验数据如下表:
| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化钠的质量/g | 4.5 | 9 | 18 | 20 |
| 溶液质量/g | 54.5 | 59 | 68 | 68 |
关于上述实验的叙述不正确的是 (填字母序号)。
A.①②所得溶液是该温度下的不饱和溶液
B.③④所得溶液溶质的质量分数相等
C.20℃时,氯化钠的溶解度为36g
D.20℃时,将④恒温蒸发25g水,过滤得18g固体
-
食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富。
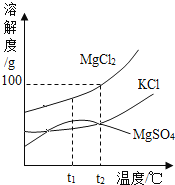
(1)海水晒盐的原理是________;
(2)晒盐过程中得到粗盐和卤水。卤水的主要成分及其溶解度的变化如右图t2℃时,MgCl2的溶解度为_______g;将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液分别降温至t1℃时,析出的晶体是________(填物质化学式);
(3)将纯净的氯化钠固体配制成溶液。20℃时,向4个盛有50g水的烧杯中,分别加入一定质量的氯化钠并充分溶解。4组实验数据如下表:
| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化納的质量/g | 4.5 | 9 | 18 | 20 |
| 溶液质量/g | 54.5 | 59 | 68 | 68 |
若将②中得到的溶液稀释成质量分数为0.9%的生理盐水,需加水的质量是_____g;
关于上述实验的叙述不正确的是______(填字母序号)。
A.①②所得溶液是该温度下的不饱和溶液
B.③④所得溶液溶质的质量分数相等
C.20℃时,氯化钠的溶解度为36g
D.20℃时,将④恒温蒸发25g水,过滤得18g固体
-
食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富。
(1)海水晒盐的原理是____________________________。
(2)如图1所示,实验室用氯化钠溶液模拟海水晒盐过程,则一定属于饱和溶液的是________(填字母)。
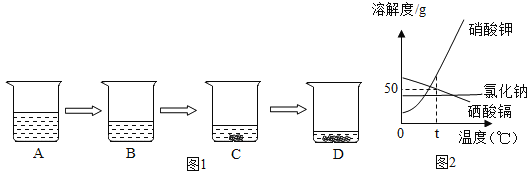
(3)氯化钠、硝酸钾、硒酸镉的溶解度曲线如图2所示,请回答
①t℃时,将65g硒酸镉加入150g水中,所得溶液的溶质质量分数为____________(精确到0.1%);
②硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是_________________________________;
③将t℃时等质量三种物质的饱和溶液降温至0℃,下列说法正确的是_____________。
a.溶质质量分数:硒酸镉>氯化钠>硝酸钾
b.溶质质量:硝酸钾>硒酸镉>氯化钠
c.溶液质量:硒酸镉>氯化钠>硝酸钾
d.三种物质的溶解度均减小
(4)海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等,综合利用海水制备烧碱的流程如图3所示:
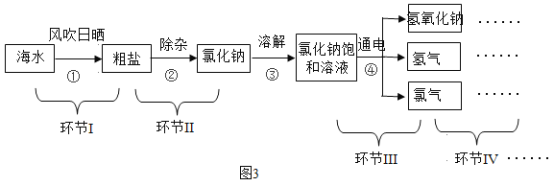
①环节Ⅱ除去粗盐中MgCl2、CaCl2、Na2SO4杂质,可依次加入______________(填试剂名称)溶液,过滤,再加人适量稀盐酸,蒸发,得到纯净的氯化钠固体:
②环节Ⅲ反应的化学方程式为______________________________________________。
-
(7分)我省多个城市濒临南海,有丰富的海洋资源。海洋是一个巨大的资源库,我们可以从海水中提取食盐,并以此为原料制得具有广泛用途的烧碱。制取的主要工艺流程如下:
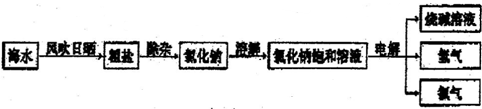
(1)利用风吹日晒可以从海水中提取粗盐,风吹日晒的主要作用是 。
(2)常用过滤的方法除去食盐中混有的泥沙,该操作中玻璃棒的作用是 。
(3)粗盐中还含有Na2SO4、CaCl2、MgCl2等可溶性杂质,除杂质时所加的四种试剂是NaOH溶液、Na2CO3溶液、BaCl2溶液、盐酸(均过量),其中加入NaOH溶液的目的是 ,除杂质时先加BaCl2溶液后加Na2CO3溶液的理由是 。
(4)该化工厂将副产品氢气和氯气加以利用:氢气在氢气中燃烧生成氯化氢,氯化气溶于水得到盐酸。写出氢气在氯气中燃烧的化学方程式 ,通过这个化学反应你对燃烧的新认识是 。
-
我国拥有丰富的海洋资源,我们可以从海水中提取食盐,并以此为原料制得具有广泛用途的产品。
(1)海水晒盐是利用了_____的方法使食盐晶体析出,得到粗盐。
(2)某制碱工厂以粗盐为原料制纯碱,部分工艺流程如下:
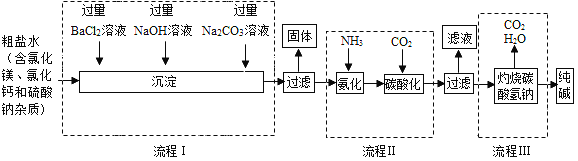
①流程I中为了除去杂质,依次加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,下列说法正确的是_____(填字母编号);
A.加入三种溶液的顺序不能调整
B.加入三种溶液可将粗盐水中的SO4、Mg2+、Ca2+转化为沉淀
C.按流程I所加溶液的顺序除杂,过滤后得到四种沉淀
②在流程I中,加入氢氧化钠溶液时发生反应的化学方程式是_____;
③流程I中Na2CO3溶液的作用是_____;
④写出流程Ⅲ中发生反应的化学方程式_____。
(3)将已配制好的100g质量分数为6%的氧化钠溶液变成质量分数为20%的氯化钠溶液,需要再加入NaCl的质量是_____g。
-
(2010·遵义,15)我国拥有丰富的海洋资源,我们可以从海水中提取食盐,并以此为原料制得具有广泛用途的烧碱,其制取的主要工艺流程如下:
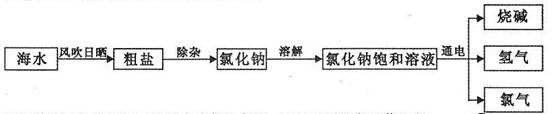
(1)利用风吹日晒可以从海水中提取粗盐,风吹日晒的主要作用是________ ;
(2)氯化钠溶解过程中搅拌的目的是 ________ ;
(3)写出氯化钠饱和溶液在通电条件下发生反应的化学方程式________
-
NaCl在生产和生活中具有广泛的用途,是一种重要的资源。通过晾晒海水可以得到粗盐和母液(又叫苦卤)。下图为母液中最主要的四种盐(NaCl、KCl、MgCl2、MgSO4)的溶解度曲线图。回答下列问题:
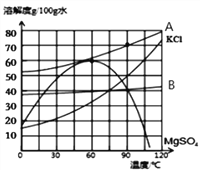
(1)①90℃时,四种盐中MgCl2的溶解度最大,则表示 MgCl2溶解度曲线的是_________。(填“A”或“B”)此时饱和MgCl2溶液的质量分数为_______(请写出计算表达式即可)
②四种盐中溶解度受温度变化的影响最小的 是___________。(填化学式)
(2)60℃时,若母液中的NaCl、KCl、MgCl2、MgSO4都已达到饱和,为了获得较纯净的MgSO4晶体,可采用的方法是_____________。
(3)工业上常通过加入碱溶液与母液中的Mg2+反应来制取Mg(OH)2沉淀。为了探究获得较高Mg2+沉淀率的反应条件,进行下列对比实验(每组实验取250mL母液):
| 实验序号 | 反应温度/℃ | 反应时间/min | 反应pH值 | Mg2+的沉淀率/% |
| a | 40 | 60 | 10 | 90.1 |
| b | 40 | 60 | 12 | 92.7 |
| c | 40 | 90 | 12 | 93.6 |
| d | 50 | 60 | 12 | 96.4 |
| e | 50 | 90 | 12 | x |
①反应过程中需测定溶液的pH,则测定溶液pH的操作是:先在玻璃片上放一小片pH试纸,然后用_____________,再将试纸显示的颜色与标准比色卡比较,读取溶液的pH。
②实验a和b对比,可得到的结论是___________________。
③表格中X的数值可能为__________(填编号)。
A.95.8 B.92.1 C.97.2 D.93.1
-
我国拥有丰富的海洋资源,我们可以从海水中提取食盐,并以此为原料制得具有广泛用途的烧碱,其制取的主要工艺流程如下:
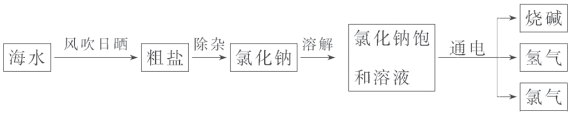
(1)利用风吹日晒可以从海水中提取粗盐,风吹日晒的主要作用是 ;
(2)氯化钠溶解过程中搅拌的目的是 ;
(3)写出氯化钠饱和溶液在通电条件下发生反应的化学方程式 。
-
我国拥有丰富的海洋资源,我们可以从海水中提取食盐,并以此为原料制得具有广泛用途的烧碱,其制取的主要工艺流程如下:
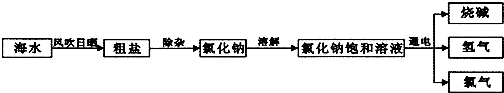
(1)氯化钠溶解过程中搅拌的目的是________;
(2)写出氯化钠饱和溶液在通电条件下发生反应的化学方程式________.










