-
硫化钠是重要化工产品,主要用于皮革、毛纺、高档纸张、染料等行业。工业上利用工业尾气硫化氢(H2S)制得产品硫化钠固体。其工业流程示意图如下图:
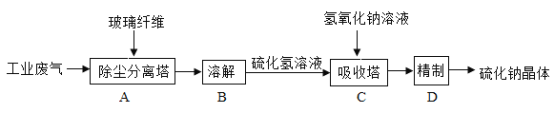
(1)图中A操作利用玻璃纤维作除尘分离塔的滤材,玻璃纤维的作用是过滤,该操作在实验室里要使用玻璃棒的作用为_____。
(2)硫化氢中硫元素的化合价为_____。硫化氢气体能溶于水,其水溶液呈酸性,称为氢硫酸,则其pH_____(填“<”、“>”或“=”)7。
(3)目前采用氢氧化钠溶液吸收工业尾气中的硫化氢,可减少空气污染。吸收塔中氢氧化钠溶液与硫化氢溶液发生硫化钠和水,写出该反应的化学方程式为_____,其基本类型为_____。
(4)产品硫化钠的物质类别属于_____(“酸”、“碱”、“盐”或“氧化物”)。硫化钠固体在空气中易氧化并易溶于水,保存硫化钠的正确方法为_____。
(5)硫化钠的溶解度随着温度升高明显增大。D操作中精制过程,从硫化钠的饱和溶液中分离出硫化钠晶体,采用的结晶方法是_____(填“蒸发溶剂”或“降温结晶”)。
-
硫化钠(Na2S)可用于皮革、染料工业等。工业上可用氢氧化钠溶液吸收燃煤产生的硫化氢(H2S)气体制造硫化钠,化学反应方程式如下:H2S+2NaOH==Na2S+2H2O。用此法生产3.9 t 硫化钠至少需消耗溶质质量分数为10%的氢氧化钠溶液多少t?
-
工业尾气硫化氢(H2S)是一种有毒气体,溶于水成为氢硫酸(H2S),目前采用氢氧化钠溶液吸收可以减少对空气的污染,并且可以制得工业产品硫化钠固体(硫化钠可溶于水)。工业流程如下图所示,则下列说法正确的是
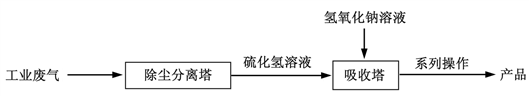
A. 系列操作中含有过滤这一操作 B. 可用石蕊试液测定氢硫酸溶液的酸碱度
C. 终产品硫化钠的化学式为Na2S D. 吸收塔内发生的化学反应基本类型是中和反应
-
(3分)硫化钠是重要的化工产品。工业上采用无水芒硝(Na2SO4)-炭粉还原法生产硫化钠(Na2S),其流程示意图如下:

(1)上述流程中,获得固体A的操作是________,固体A的化学式为________。
(2)若“煅烧”所得气体是分子个数比为1∶1的两种碳的氧化物,则“煅烧”时发生的总反应的化学方程式为________。
-
硫化钠是重要的化工产品.工业上采用无水芒硝(Na2SO4)-炭粉还原法生产硫化钠(Na2S),其流程示意图如下:

(1)上述流程中,获得固体A的操作是________,固体A的化学式为________.
(2)若“煅烧”所得气体是分子个数比为1:1的两种碳的氧化物,则“煅烧”时发生的总的化学反应方程式为________.
-
硫化钠是重要的化工产品.工业上采用无水芒硝(Na2SO4)-炭粉还原法生产硫化钠(Na2S),其流程示意图如下:

(1)上述流程中,获得固体A的操作是________,固体A的化学式为________.
(2)若“煅烧”所得气体是分子个数比为1:1的两种碳的氧化物,则“煅烧”时发生的总的化学反应方程式为________.
-
硫化钠是重要化工产品.工业上采用无水芒硝(Na2SO4)-炭粉还原法生产硫化钠(Na2S),其流程示意图如图:
(1)上述流程中,获得固体A的操作是过滤,若滤纸与普通漏斗内壁不紧贴,导致的后果是______,固体A的化学式为______.硫化钠中硫元素的化合价为______价.
(2)煅烧中炭粉的作用除了提供还原剂外,还能具有______作用
(3)若“煅烧”所得气体是分子个数比为1:1的两种碳的氧化物,则“煅烧”时发生的总的化学反应方程式为______ 3Na2S+4CO2↑+4CO↑

-
硫化钠是重要化工产品.工业上采用无水芒硝(Na2SO4)-炭粉还原法生产硫化钠(Na2S),其流程示意图如图:
(1)上述流程中,获得固体A的操作是过滤,若滤纸与普通漏斗内壁不紧贴,导致的后果是______,固体A的化学式为______.硫化钠中硫元素的化合价为______价.
(2)煅烧中炭粉的作用除了提供还原剂外,还能具有______作用
(3)若“煅烧”所得气体是分子个数比为1:1的两种碳的氧化物,则“煅烧”时发生的总的化学反应方程式为______ 3Na2S+4CO2↑+4CO↑

-
盐酸是重要的无机化工产品,广泛用于染料、医药、食品、冶金等行业。
(1)实验室使用的稀盐酸通常都是将浓盐酸用水稀释而成的。现欲用溶质质量分数为37%的浓盐酸(密度为1.189·mL )配制14.6%的稀盐酸100g。步骤为:计算、________、稀释。经过计算可知需要浓盐酸的体积为_______,量取水时应选用规格(从10mL、50mL、100mL中选取)为_______mL的量筒。最后将稀盐酸转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是________(填字母序号)。
)配制14.6%的稀盐酸100g。步骤为:计算、________、稀释。经过计算可知需要浓盐酸的体积为_______,量取水时应选用规格(从10mL、50mL、100mL中选取)为_______mL的量筒。最后将稀盐酸转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是________(填字母序号)。
A100g B14.6% C稀盐酸
(2)该稀盐酸还可用来测定镀锌铁皮锌镀层的质量。将该铁皮与足量稀盐酸反应,待产生的气泡明显减少时取出(此时可认为锌己反应完全,铁还未参与反应),洗涤,烘干,称量,减少的质量即为锌镀层的质量。下列实验操作对测定结果的影响,判断错误的是__________(填字母序号)。
A铁皮未及时取出,会导致测定结果偏小
B铁皮未洗涤干净,会导致测定结果偏大
C烘干时间过长,会导致测定结果偏小
D把稀盐酸换成稀硫酸,会导致测定结果偏大
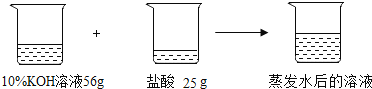
(3)取用上述所配稀盐酸25g与56g溶质质量分数为10%的氢氧化钾溶液相混合(含2滴酚酞试液),混合液刚好由红色变为无色,可认为恰好完全反应。将反应后所得溶液蒸发6.5g水(此过程中无晶体析出),求此时溶液的溶质质量分数。(写出具体计算过程,注意格式)__________。
-
(9分)盐酸是重要的无机化工产品,广泛用于染料、医药、食品、冶金等行业。
(1)实验室使用的稀盐酸通常都是将浓盐酸用水稀释而成的。现欲用溶质质量分数为37%的浓盐酸配制14.6%的稀盐酸100g。步骤为:计算、 、稀释。量取水时应选用规格为 (从10、50、100中选取)rnL的量筒。最后将稀盐酸转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是 (填字母序号)。
A.100g B.14.6% C.稀盐酸
(2)若用上述所配稀盐酸(100g溶质质量分数为14.6%)制取氢气,理论上可制得氢气多少克?(写出具体计算过程,注意格式)
(3)该稀盐酸还可用来测定镀锌铁皮锌镀层的质量。将该铁皮与足量稀盐酸反应,待产生的气泡明显减少时取出(此时可认为锌己反应完全,铁还未参与反应),洗涤,烘干,称量,减少的质量即为锌镀层的质量。下列实验操作对测定结果的影响,判断不正确的是 (填字母序号)。
A.铁皮未及时取出,会导致测定结果偏小
B.铁皮未洗涤干净,会导致测定结果偏大
C.烘干时间过长,会导致测定结果偏小
D.把稀盐酸换成稀硫酸,会导致测定结果偏大
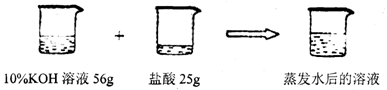
(4)取用上述所配稀盐酸25g与56g溶质质量分数为10%的氢氧化钾溶液相混合(含2滴酚酞试液),混合液刚好由红色变为无色,可认为恰好完全反应。将反应后所得溶液蒸发6.5g水(此过程中无晶体析出),求此时溶液的溶质质量分数。(写出具体计算过程,注意格式)








