-
工业上常用电解饱和食盐水的方法制取烧碱,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
(1)取少量样品于烧杯中,向其中加入过量稀盐酸,观察到有气泡产生,说明样品中含有 ,该反应的化学方程式为 ,接着又向烧杯中继续加入硝酸银溶液,出现了白色沉淀,甲同学立刻得出结论:样品中还含有氯化钠,乙同学对该结论提出了质疑,认为不一定含有氯化钠,理由是 ;
(2)丙同学认为除了需要确认是否含有氯化钠外,还需要确认样品中是否含有氢氧化钠,于是,大家又进行了以下实验:
①另取少量样品溶解于水,向其中加入过量硝酸钙溶液,产生白色沉淀,然后过滤、洗涤;
②向滤液中加入足量稀硝酸,再滴入硝酸银溶液后产生白色沉淀;
③向滤渣中加少量水后滴入酚酞,溶液变红.
由此判断,滤渣中的物质是 (填化学式).
(3)根据以上经验,得出的结论正确的是 (填序号)
A.样品中无NaCl
B.样品中只有NaOH和Na2CO3
C.样品中无NaOH
D.样品中有Na2CO3、NaOH和NaCl.
九年级化学填空题中等难度题查看答案及解析
-
工业上常用电解饱和食盐水的方法制取烧碱,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
(1)取少量样品于烧杯中,向其中加入过量稀盐酸,观察到有气泡产生,说明样品中含有____,该反应的化学方程式为____,接着又向烧杯中继续 加入硝酸银溶液,出现了白色沉淀,甲同学立刻得出结论:样品中还含有氯化钠,乙同学对该结论提出了质疑,认为不一定含有氯化钠,理由是____;
(2)丙同学认为除了需要确认是否含有氯化钠外,还需要确认样品中是否含有氢氧化钠,于是, 大家又进行了以下实验:
①另取少量样品溶解于水,向其中加入过量硝酸钙溶液,产生白色沉淀,然后过滤、洗涤;
②向滤液中加入足量稀硝酸,再滴入硝酸银溶液后产生白色沉淀;
③向滤渣中加少量水后滴入酚酞,溶液变红. 由此判断,滤渣中的物质是____(填化学式).滤液pH____(填:<7或=7或>7)
(3)根据以上经验,得出的结论正确的是____填序号)
A 样品中无NaCl B 样品中只有NaOH和Na2CO3 C 样品中无NaOH D 样品中有Na2CO3、NaOH和NaCl.
九年级化学实验题困难题查看答案及解析
-
工业上常用电解饱和食盐水的方法制取烧碱,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
(1)甲同学取少量样品于烧杯中,向其中加入过量稀盐酸,观察到有气泡产生,说明样品中含有_____,他接着又向烧杯中继续加入硝酸银溶液, 出现了白色沉淀(已知氯化银是白色沉淀),得出结论:样品中___ (填“一定”或“不一定”)含有氯化钠。
(2)乙同学认为除了需要确认是否含有氯化钠外,还需要确认样品中是否含有氢氧化钠,于是,大家又进行了以下实验:
①另取少量样品溶解于水,向其中加入过量硝酸钙溶液,过滤,得到滤液和滤渣,滤渣的成分是_______(填化学式) ;
②取少量滤液滴入酚酞,溶液变红;
③向滤液中加入足量稀硝酸,再滴入硝酸银溶液后产生白色沉淀;
(3)根据以上实验,得出的结论正确的是_____ (填序号) 。
A 样品中无NaCl
B 样品中只有NaOH和Na2CO3
C 样品中无NaOH
D 样品中有Na2CO3、NaOH 和NaCl
九年级化学实验题中等难度题查看答案及解析
-
工业上常用电解饱和食盐水的方法制取烧碱,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
(1)取少量样品于烧杯中,向其中加入过量稀盐酸,观察到有气泡产生,说明样品中含有_________,接着又向烧杯中继续加入硝酸银溶液,出现了白色沉淀(已知氯化银是白色沉淀),得出结论:样品中____________(填“一定”或“不一定”)含有氯化钠。
(2)丙同学认为除了需要确认是否含有氯化钠外,还需要确认样品中是否含有氢氧化钠,于是,大家又进行了以下实验:
①另取少量样品溶解于水,向其中加入过量硝酸钙溶液,产生白色沉淀,然后过滤、洗涤;
②取少量滤液滴入酚酞,溶液变红;
③向滤液中加入足量稀硝酸,再滴入硝酸银溶液后产生白色沉淀;
由此判断,实验中滤渣的成分是_________(填化学式)。
(3)根据以上实验,得出的结论正确的是________(填序号)。
A、样品中无NaCl
B、样品中只有NaOH和Na2CO3
C、样品中无NaOH
D、样品中有Na2CO3、NaOH和NaCl
(4)配制100mL质量分数10%的氢氧化钠溶液(密度1.11g/mL),需要质量分数40%的氢氧化钠溶液(1.43g/mL)_________mL,水________mL。(计算结果精确到0.1)
九年级化学综合题困难题查看答案及解析
-
酸、碱、盐在生产和生活中具有广泛的用途。工业上常用电解饱和食盐水的方法制取烧碱,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
(1)取少量样品于烧杯中,向其中加入过量稀盐酸,观察到有气泡产生,说明样品中含有____________________(填化学式) ,接着又向烧杯中继续加入硝酸银溶液,出现了白色沉淀,于是同学们得出结论:样品中____________________(填“一定"或“不一定” )含有氯化钠。
(2)除了需要确认是否含有氯化钠外,还需要确认样品中是否含有氢氧化钠。于是,大家又进行了下列实验:
①另取少量样品溶解于水,向其中加入过量硝酸钙溶液,产生白色沉淀,然后过滤、洗涤;
②取少量滤液滴入酚酞溶液,溶液变红;
③向滤液中加入足量稀硝酸,再滴入硝酸银溶液后产生白色沉淀。
由此判断,实验①中滤渣的成分是____________________(填化学式)。
(3)根据以上实验,得出的结论正确的是___________________(填字母)。
A.样品中无NaCl
B.样品中只有NaOH和Na2CO3
C.样品中无NaOH
D.样品中有Na2CO3、NaOH和NaCl
(4)该兴趣小组的同学通过查阅资料得知:电解饱和食盐水,除了生成烧碱以外,还生成了氢气和氯气。请写出该反应的化学方程式____________________。
九年级化学科学探究题困难题查看答案及解析
-
工业上常用电解饱和食盐水的方法制取烧碱,其反应原理为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
①取少量样品于烧杯中,加入过量稀盐酸,观察到有气泡产生,说明样品中含有________。
②继续向烧杯中加入硝酸银溶液,出现白色沉淀,甲同学得出结论:样品中还含有氯化钠,乙同学对该结论提出了质疑,认为不一定含有氯化钠,其理由是________;丙同学提出只需将试剂_____换成______就可以确定氯化钠是否存在。
③丁同学认为还需要确认样品中是否含有氢氧化钠,于是大家取少量样品配成溶液后进行以下实验:
实验操作
现象
结论
___________________________
___________
样品中有氢氧化钠
通过实验,兴趣小组同学得出结论:该工业烧碱中含有Na2CO3、NaCl和NaOH。
④同学们还想测定该烧碱中碳酸钠的质量分数。他们取10克烧碱样品配成溶液,向其中
逐滴加入BaCl2溶液,产生沉淀的量与所加BaCl2的量关系如图所示。(NaOH和BaCl2不反应)
(1)求样品中Na2CO3的质量分数_____。( 写出计算过程)
(2)B点处所得溶液中溶质有________。
九年级化学简答题困难题查看答案及解析
-
某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品,这种工业称为“氯碱工业”。 某研究性学习小组对该厂生产的烧碱样品进行如下探究:电解饱和食盐水的化学方程式为
+____↑。
(提出问题)烧碱样品中可能含有哪些杂质?
(猜想)猜想1:只含有Na2CO3 ;
猜想2:只含有NaCl;
猜想3:含有______。
作出猜想1的依据是_____(用化学方程式表示)。
(设计实验)
实验步骤
实验现象
解释或结论
Ⅰ.取适量烧碱样品于试管中,加水溶解,并用手触摸试管外壁
试管外壁发热
原因是____。
Ⅱ.向Ⅰ所得的溶液中逐滴加入稀硝酸至过量
刚开始_____,一段时间后产生能使澄清石灰水变浑浊的气体
猜想2不成立
Ⅲ.向Ⅱ所得的溶液中___。
产生白色沉淀
结合实验Ⅱ,猜想3成立
(交流与讨论)小坚同学提出:“上述实验Ⅱ中稀硝酸也可以用稀盐酸代替”。你认为他的观点________(选填“正确”或“不正确”),理由是_____。
九年级化学科学探究题中等难度题查看答案及解析
-
某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品,反应的化学方程式为:
2NaCl+2H2O═2NaOH+H2↑+Cl2↑.某研究性学习兴趣小组对该厂生产的烧碱样品进行如下探究.
[提出问题]:烧碱样品中含有哪些杂质?
[猜想]:
(1)可能含有NaCl,作出此猜想的依据是电解的过程中氯化钠没有完全反应.
(2)可能含有碳酸钠,做出此猜想的理由是________(用化学方程式表示).
[实验设计]
[反思]:小明认为上述实验不能说明样品中含有氯化钠,理由是________.实验步骤 实验现象 解释或结论 ①取适量的烧碱样品置于试管中加水溶解,用手触摸试管外壁. 试管外壁发热 原因是________ ②向①所得的溶液中加入盐酸至过量. 开始时无明显现象,过一段时间后有气泡产生. 说明样品中含有杂质________ ③向②所得的溶液中加入硝酸银溶液. 有白色沉淀产生. AgNO3+NaCl═AgCl↓+NaNO3
说明样品中含有杂质氯化钠九年级化学填空题中等难度题查看答案及解析
-
某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品,反应的化学方程式为:
2NaCl+2H2O
2NaOH+H2↑+Cl2↑。某研究性学习兴趣小组对该厂生产的烧碱样品进行如下探究。
[提出问题]:烧碱样品中含有哪些杂质?
[猜想]:
(1)可能含有NaCl,作出此猜想的依据是电解的过程中氯化钠没有完全反应。
(2)可能含有碳酸钠,做出此猜想的理由是________(用化学方程式表示)。
[实验设计]
实验步骤
实验现象
解释或结论
①取适量的烧碱样品置于试管中加水溶解,用手触摸试管外壁。
试管外壁发热。
原因是________
②向①所得的溶液中加入盐酸至过量。
开始时无明显现象,过一段时间后有气泡产生。
说明样品中含有杂质
③向②所得的溶液中加入硝酸银溶液。
有白色沉淀产生。
AgNO3+NaCl=AgCl↓+NaNO3
说明样品中含有杂质氯化钠
[反思]:小明认为上述实验不能说明样品中含有氯化钠,理由是________。
九年级化学探究题困难题查看答案及解析
-
某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O
2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究。
I.定性探究
(提出问题)烧碱样品中含有哪些杂质?
(猜想)猜想一:可能含有Na2CO3;
猜想二:可能含有NaCl,作出此猜想的依据______(用简洁的文字表述)。
(设计实验)
实验步骤
实验现象
解释或结论
①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁。
试管外壁发热
原因是 ______
②向①所得的溶液中加入稀硝酸至过量,将产生的气体通入澄清石灰水
有气体产生,澄清石灰水浑浊
样品中含有的杂质是 ______
③向②所得的溶液中滴加几滴硝酸银溶液。
无现象
猜想二 ______ (填“正确”或“错误”)
(交流与讨论)小明同学提出:“上述实验中稀硝酸也可以用稀盐酸代替”,你同意他的观点吗?若不同意,写出理由______。
Ⅱ.定量探究
(提出问题)烧碱样品中氢氧化钠的质量分数是多少呢?
(设计实验)小丽同学设计探究方案①、②进行实验并测得数据如下:
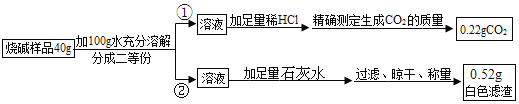
(交流与反思)
(1)小强同学认为方案②因缺少______(填操作名称),导致测得的氢氧化钠的质量分数偏小。
(2)请你利用方案①测得的数据计算烧碱样品中氢氧化钠的质量分数______(请在答题纸上写出计算过程)。
九年级化学科学探究题困难题查看答案及解析