保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定:在NaCl存在下,Na2S2O4在水中溶解度显著下降。Na2S2O4制备流程如图:
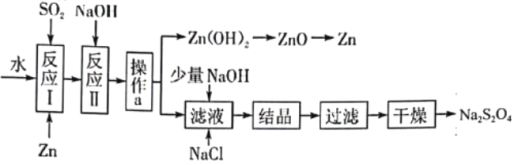
(1)反应I的原理为,该反应的基本反应类型为______。
(2)反应II为复分解反应,该反应的化学方程式为______。
(3)氢氧化锌在加热的条件下分解生成两种氧化物,发生反应的化学方程式为____。
九年级化学流程题中等难度题
保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定:在NaCl存在下,Na2S2O4在水中溶解度显著下降。Na2S2O4制备流程如图:

(1)反应I的原理为,该反应的基本反应类型为______。
(2)反应II为复分解反应,该反应的化学方程式为______。
(3)氢氧化锌在加热的条件下分解生成两种氧化物,发生反应的化学方程式为____。
九年级化学流程题中等难度题
保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定,在NaCl存在下,Na2S2O4在水中溶解度显著下降.制备流程如图:
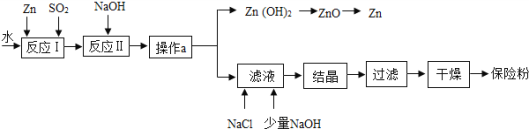
(1)反应Ⅰ的原理为:Zn+2SO2═ZnS2O4,该反应中将锌研磨成粉末的目的:_____;该反应的基本反应类型为_____.
(2)反应Ⅱ为复分解反应,该反应的化学方程式为_____.
(3)操作a得到的滤液有些浑浊,可能的原因_____.
(4)滤液中含有Na2S2O4,为使Na2S2O4结晶析出还需要加入少量NaOH的原因是_____,加入NaCl的原因是_____.
(5)氢氧化锌在加热的条件下分解成两种氧化物,写出氢氧化锌分解的化学方程式:_____
(6)198gZn(OH)2理论上能得到Zn的质量为_____g.
九年级化学流程题中等难度题查看答案及解析
保险粉(化学式 Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4 在碱性溶液中稳定,在中性和酸性溶液中极不稳定;在 NaCl 存在下,Na2S2O4 在水中溶解度显著下降。Na2S2O4 制备流程如下:
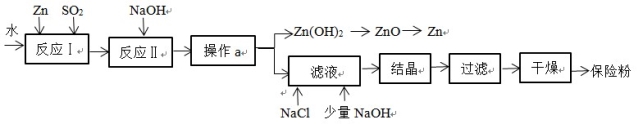
(1)反应Ⅰ的原理为:Zn + 2SO2 == ZnS2O4,该反应类型为 。
(2)反应Ⅱ为复分解反应,该反应的化学方程式为 。
(3)操作a的名称为 。
(4)滤液中含有 Na2S2O4,为使 Na2S2O4 结晶析出还需要加入少量 NaOH 的原因是 , 加入 NaCl 的原因是 。
(5)198g Zn(OH)2 理论上能得到 Zn 的质量为 。
九年级化学填空题中等难度题查看答案及解析
保险粉(化学式 Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定;在 NaCl 存在下,Na2S2O4 在水中溶解度显著下降。Na2S2O4制备流程如下:

(1)反应Ⅰ的原理为:Zn + 2SO2 == ZnS2O4,该反应类型为___________。
(2)操作a的名称为_________,用到的玻璃仪器有烧杯、漏斗、___________ 。
(3)在此流程中用到的物质,属于氧化物的是_________。
(4)该流程中能再次循环利用的物质是_________
九年级化学流程题中等难度题查看答案及解析
保险粉(化学式 Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定;在 NaCl 存在下,Na2S2O4 在水中溶解度显著下降。Na2S2O4制备流程如下:

(1)反应Ⅰ的原理为:Zn + 2SO2 == ZnS2O4,ZnS2O4中硫元素的化合价为_____。
(2)操作a的名称为________,用到的玻璃仪器有烧杯、漏斗、_________。
(3)在此流程中用到的物质,属于氧化物的是________。
(4)该流程中能再次循环利用的物质是______
九年级化学流程题中等难度题查看答案及解析
保险粉(化学式Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定;在NaCl存在下,Na2S2O4在水中溶解度显著下降。Na2S2O4制备流程如下:
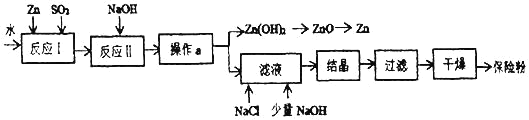
(1)反应I的原理为:Zn+2SO2═ZnS2O4,该反应基本类型为_______;
(2)反应Ⅱ为复分解反应,该反应的化学方程式为________________;
(3)操作a的名称为______;
(4)滤液中含有Na2S2O4,为使Na2S2O4结晶析出还需要加入少量NaOH的原因是____________,加入NaCl的原因是______________。
九年级化学流程题中等难度题查看答案及解析
保险粉(化学式Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定;在NaCl存在下,Na2S2O4在水中溶解度显著下降。Na2S2O4制备流程如下:(已知:常温下Zn(OH)2的溶解度为1.42×10−5g)
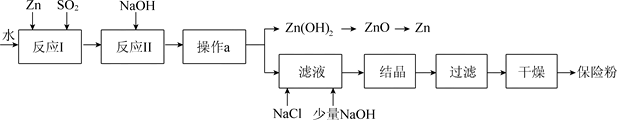
(1)反应I的原理为:Zn+2SO2===ZnS2O4,该反应的基本类型为___________。
(2)反应II为复分解反应,该反应的化学方程式为_________________________________。
(3)操作a的名称为__________。
(4)滤液中含有Na2S2O4,为使Na2S2O4结晶析出加入NaCl的原因是___________。
九年级化学信息分析题中等难度题查看答案及解析
保险粉(化学式Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定;在NaCl存在的条件下,Na2S2O4在水中的溶解度显著下降。Na2S2O4 制备流程如下图所示:
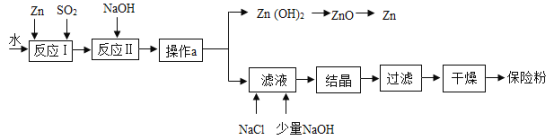
(1)反应I的原理为: , 该反应类型为_____。
(2)操作a的名称为_____。
(3)滤液中含有Na2S2O4, 往滤液中加入NaCl和少量NaOH的原因分别是_____。
九年级化学流程题中等难度题查看答案及解析
保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定:在NaCl存在下,Na2S2O4在水中溶解度显著下降。Na2S2O4制备流程如图:

(1)反应I的原理为,该反应的基本反应类型为______。
(2)反应II为复分解反应,该反应的化学方程式为______。
(3)氢氧化锌在加热的条件下分解生成两种氧化物,发生反应的化学方程式为____。
九年级化学流程题中等难度题查看答案及解析
科学探究是学习化学的重要途径。某化学兴趣小组的同学进行了以下几个探究实验。
(1)氨气(NH3)在生产、生活中有广泛的用途。氨气极易溶于水,其水溶液叫作氨水,呈碱性,是农业上常用的速效肥料。
①加热氯化铵和消石灰可制取氨气,同时产生氯化钙和水,写出反应的化学方程式__________。
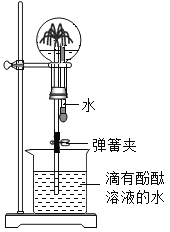
②如图是氨气性质的趣味实验:圆底烧瓶中充满氨气,当挤压胶头滴管并打开止水夹时,可观察到什么现象__________?
(2)在探究稀盐酸的化学性质时,该小组的同学做了如图一所示的两个实验。实验结束后,将A、B两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液中溶质的成分进行探究。
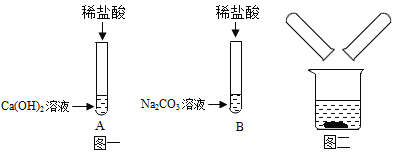
①对于滤液的成分,有下列猜想:I.NaCl;I.NaCl、CaCl2;Ⅲ.NaCl、CaCl2、HCl。指出以上不合理的猜想并说出理由__________。
②你认为滤液的成分还可能是__________;请设计实验证明你的猜想正确,简要写出实验步骤、现象__________。
(3)利用下图微型实验装置可制取CO,然后用CO还原Fe3O4并检验气体产物。已知草酸在浓硫酸作用下受热分解生成二氧化碳、一氧化碳和水。

①浓硫酸的作用是______________。
②写出B处Fe3O4发生反应的化学方程式__________。
(4)为测定一瓶过氧化氢溶液中溶质的质量分数取该溶液34.0g,加入二氧化锰1.0g,待完全反应不再有气体逸出时,称得剩余物质的总质量为34.2g。计算:该过氧化氢溶液中溶质的质量分数__________。
九年级化学科学探究题困难题查看答案及解析
九年级化学填空题中等难度题查看答案及解析