-
9.电动自行车使用蓄电池供电驱动,具有噪音低,无尾气污染等优点.铅酸蓄电池工作的化学方程式为:PbO2+2H2SO4+Pb═2PbSO4+2H2O,其中PbSO4中铅元素的化合价为.欲用浓硫酸配制该电池中的稀硫酸溶液,应把慢慢倒入盛有的烧杯中,并用玻璃棒不断搅拌,以防意外;铅蓄电池报废后,不能随意丢弃,原因是(任写一点).
九年级化学填空题中等难度题查看答案及解析
-
(3分)电动自行车、小汽车等交通工具中都有为其提供电能的铅蓄电池(又称“电瓶”),它的优点是可以充电循环使用,电瓶内发生的化学反应是:
PbO2(固)+ 2H2SO4 + Pb = 2PbSO4↓+ 2H2O
某电瓶中装有36%的稀硫酸1200 g,电瓶工作时有310.5 g的铅参加反应。试计算:
(1)原稀硫酸中所含溶质的质量是 g。
(2)电瓶工作时消耗硫酸的质量。
(3)反应后硫酸溶液中溶质的质量分数。(最后结果精确到0.01%)
九年级化学计算题困难题查看答案及解析
-
电动汽车所用电池生产和回收的管理不当也会污染环境,处理不当会导致人体血铅超标。化学电池是一类重要的能源,铅酸蓄电池是一种可充电的二次化学电池,其反应的原理用化学方程式表示为Pb+PbO2+2H2SO4
2PbSO4+2H2O。则回答:
(1)铅酸蓄电池放电时能量转变是化学能转变成____能。
(2)某铅酸电池厂生产电池用的28%的稀硫酸,将98%浓硫酸稀释配制成该稀硫酸时,正确的操作是_____________,并不断搅拌以防液体飞溅。
(3)使用铅酸蓄电池的电动车与使用汽油燃料的轻便摩托车相比,电动车的突出优点是不会产生____等温室气体,但电池对土壤和水体的污染也是不容忽视,因此要回收再利用废旧电池。
九年级化学填空题中等难度题查看答案及解析
-
最早使用的充电电池是铅蓄电池。已知电动车铅蓄电池充电时反应的化学方程式为:2PbSO4+2H2O==Pb+PbO2+2X,则X的化学式为( )
A. SO2 B. SO3 C. H2SO3 D. H2SO4
九年级化学单选题困难题查看答案及解析
-
(2010浙江嘉兴39)电动自行车、小汽车等交通工具中都有为其提供电能的铅蓄电池(又称“电瓶”),它的优点
是可以充电循环使用。电瓶的正极材料是二氧化铅(PbO2),负极材料是金属铅(Pb),电瓶内所加液体是溶质质量分数为36%的稀硫酸,放电(为外界供电)时发生反应的化学方程式如下:
PbO2 (固)+ 2H2SO4 + Pb = 2PbSO4 ↓+ 2H2O
当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
(1)电瓶在放电时,▲ 能转化为电能。
(2)假如某个电瓶中铅的质量为1800克,内装36%的稀硫酸1200克,当有310.5克的铅参加反应时,需消耗稀硫酸中溶质多少克?此时电瓶中硫酸溶液溶质的质量分数是多少?
(最后结果保留两位小数)
九年级化学计算题中等难度题查看答案及解析
-
(2010•嘉兴)电动自行车、小汽车等交通工具中都有为其提供电能的铅蓄电池(又称“电瓶”),它的优点是可以充电循环使用.电瓶的正极材料是二氧化铅(PbO2),负极材料是金属铅(Pb),电瓶内所加液体是溶质质量分数为36%的稀硫酸,放电(为外界供电)时发生反应的化学方程式如下:PbO2 (固)+2H2SO4+Pb=2PbSO4↓+2H2O
当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电.
(1)电瓶在放电时,______能转化为电能.
(2)假如某个电瓶中铅的质量为1800克,内装36%的稀硫酸1200克,当有310.5克的铅参加反应时,需消耗稀硫酸中溶质多少克?此时电瓶中硫酸溶液溶质的质量分数是多少?(最后结果保留两位小数)九年级化学解答题中等难度题查看答案及解析
-
电动车已经走进了千家万户.许多电动车使用的电池为铅蓄电池,它的两极是铅Pb和氧化铅PbO2,电解液是溶质质量分数为20%的稀H2SO4,总的电池反应是:Pb+PbO2+2H2SO4=2PbSO4+2H2O
(1)该反应中,PbO2中Pb的化合价由________变为________.
(2)在实验室把100克溶质质量分数为98%的浓硫酸稀释成20%的稀硫酸,需用________毫升的蒸馏水,稀释时需要的仪器有烧杯和________.稀释时应该注意的事项是:________.
(3)说出废旧的铅蓄电池不能随意丢弃的一点原因________.九年级化学填空题中等难度题查看答案及解析
-
汽车是重要的交通工具.
(1)汽车使用天然气作燃料,排放污染较低.天然气的主要成分为________.
(2)完成车用铅酸电池充电的反应:2PbSO4+2H2OPb+2H2SO4+________.
九年级化学填空题中等难度题查看答案及解析
-
铅蓄电池在生产、生活中使用广泛。其构造示意图如图1,回答下列问题:
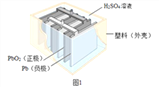
(1)图1铅蓄电池放电过程中,反应的化学方程式为 Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断_____(填“增大”、“减小”或“不变”)。
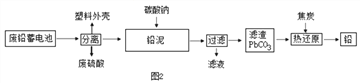
(2)如图2是回收废铅蓄电池的一种工艺流程。
①写出焦炭热还原生成铅的化学方程式: ________________________
②将流程图中的废硫酸和滤液按一定比例混合,再将所得的混合液经____、降温结晶、过滤等操作,可以析出Na2SO4·10H2O晶体。
③如表是一些金属熔点的数据:
金属
锡
铅
铋
镉
熔点∕℃
231.9
327.5
271.3
320.9
日常所用保险丝由铋、铅、锡、镉等金属组成,其熔点约为________________。
A. 231.9-327.5℃ B.271.3-320.9℃ C.60-80℃ D.20-40℃
④废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
物质
CaCO3
NH3
Ca(OH)2
市场参考价(元/kg )
1.8
6.5
2.0
已知:2NH3+H2SO4═(NH4)2SO4,如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择_________ 。
九年级化学综合题困难题查看答案及解析
-
铅蓄电池在生产、生活中使用广泛。其构造示意图如图,回答下列问题:

①铅蓄电池充电时是将电能转化为_____能。
②铅蓄电池放电过程中,反应的化学方程式为Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断_____(填“增大”、“减小”或“不变”)。
③稀释浓硫酸时必须非常小心,正确的操作是_____。
④废硫酸直接排放会污染环境,可以用熟石灰中和硫酸,写出该反应的化学方程式_____。
九年级化学简答题中等难度题查看答案及解析