-
工业生产常用“苛化法”制取氢氧化钠其原料为碳酸钠、石灰乳[由Ca(OH)2和水组成的混合物],大致流程如下。
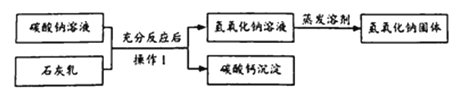
科学兴趣小组模拟上述流程,在实验室中制备氢氧化钠。
(1)实验室进行“操作1”时,需要用到下列器材中的_______(可多选).
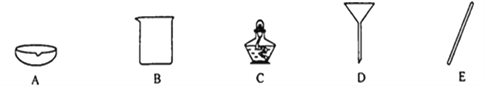
(2)制备氢氧化钠的化学方程式为,Na2CO3+Ca(OH)2=2NaOH+CaCO3↓.将53克溶质质量分数为20%的碳酸钠溶液与17克石灰乳混合,若二者恰好完全反应出计算所得氢氧化钠溶液的溶质质量分数_______。(写出计算过程,计算结果精确到0.1%)
-
工业生产常用“苛化法”制取氢氧化钠其原料为碳酸钠、石灰乳[由Ca(OH)2和水组成的混合物],大致流程如下。
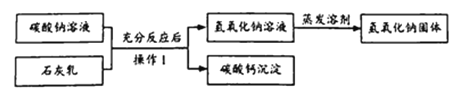
科学兴趣小组模拟上述流程,在实验室中制备氢氧化钠。
(1)实验室进行“操作1”时,需要用到下列器材中的_______(可多选).
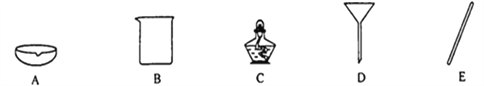
(2)制备氢氧化钠的化学方程式为,Na2CO3+Ca(OH)2=2NaOH+CaCO3↓.将53克溶质质量分数为20%的碳酸钠溶液与17克石灰乳混合,若二者恰好完全反应出计算所得氢氧化钠溶液的溶质质量分数_______。(写出计算过程,计算结果精确到0.1%)
-
氢氧化钙 [Ca(OH)2] 是重要的建筑材料,工业上常以石灰石(主要成分为CaCO3)为原料生产氢氧化钙,主要流程如下:
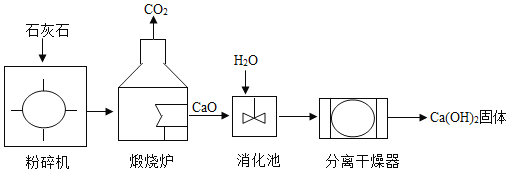
(1)粉碎石灰石的目的是____。
(2)碳酸钙相对分子质量的计算式____。
(3)氢氧化钙常用作建筑材料,因为其吸收二氧化碳会转化为坚固的碳酸钙。该反应的化学方程式为 ______ 。
(4)钙元素对人类生命和生活具有重要意义。氧化钙能与水反应,此反应可用于______(填字母序号)。
A某些食品干燥剂 B制熟石灰 C加热食物
-
氢氧化钙 [Ca(OH)2] 是重要的建筑材料,工业上常以石灰石(主要成分为CaCO3)为原料生产氢氧化钙,主要流程如下:

(1)氢氧化钙[Ca(OH)2]的组成元素中,属于金属元素的是_______________。
(2)粉碎石灰石的目的是_____________。
(3)煅烧炉中,发生的反应为CaCO3 CaO + CO2↑,此反应属于基本反应类型中________反应。
CaO + CO2↑,此反应属于基本反应类型中________反应。
(4)消化池中发生的反应为CaO +H2O = Ca(OH)2 ,若56t CaO参加反应,可产生的Ca(OH)2 质量为________t。
-
小慧同学以碳酸钙、碳酸钠和水为原料制取氢氧化钠,设计出如下反应流程:
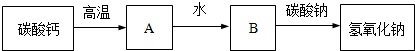
则流程图中B物质的化学式是( )
A.CO2
B.CaO
C.Ca(OH)2
D.H2CO3
-
小慧同学以碳酸钙、碳酸钠和水为原料制取氢氧化钠,设计出如下反应流程:
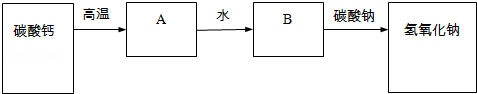
则流程图中B物质的化学式是( )
A.CO2 B.CaO C.Ca(OH)2 D.H2CO3
-
小慧同学以碳酸钙、碳酸钠和水为原料制取氢氧化钠,设计出如下反应流程:
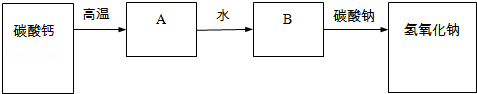
则流程图中B物质的化学式是( )
A.CO2 B.CaO C.Ca(OH)2 D.H2CO3
-
某兴趣小组对氯酸钾(KClO3)展开如下探究:
(探究一)工业制备KClO3
以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:
(资料卡片):氯化时,主要反应为6Ca(OH)2 + 6X ═ Ca(ClO3)2 + 5CaCl2 + 6H2O,少量 X与Ca(OH)2反应生成Ca(ClO)2、CaCl2和H2O,Ca(ClO)2 分解为CaCl2和O2。
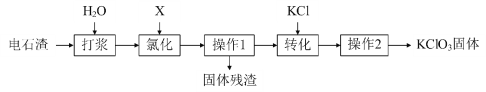
(1)根据资料,X的化学式为______,写出氯化时,X和Ca(OH)2反应生成Ca(ClO)2的化学方程式______。
(2)氯化时,为提高X转化为Ca(ClO3)2的转化率,下列措施可行的是______(填序号)。
A.充分搅拌浆料 B.加足量水使Ca(OH)2完全溶解 C.缓缓通入X
(3)操作1在实验室中的名称是______,需要用到的玻璃仪器有______、______和玻璃棒,玻璃棒的作用是______。氯化过程控制电石渣过量,固体残渣的主要成分为______和______(填化学式)。
(4)操作1后得到溶液中Ca(ClO3)2与CaCl2的化学计量数之比______1:5(填“>”、“<”或“=”)。转化时,加入KCl发生反应的化学方程式为______。
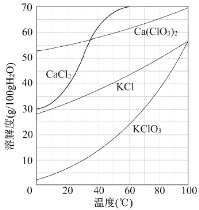
(5)操作2包含一系列实验操作,结合如图分析,主要操作为蒸发浓缩 →______→过滤→洗涤→低温烘干。
(探究二)探究KClO3制氧气
某小组利用如图所示装置对KClO3制氧气进行了探究:

(资料卡片):
①KClO3的熔点约为356℃,MnO2在加热条件下不分解。
②KClO3分解时,传感器得到氧气浓度随温度的变化示意图及使用不同催化剂时的固体残留率示意图如下:
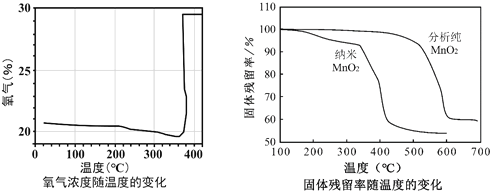
(6)由图可知KClO3分解温度______(填“高于”、“等于”或“低于”)其熔点。
(7)图中,在KClO3分解前,传感器测得氧气浓度降低的原因可能是______。
(8)分析图中,对KClO3分解催化效果更好的催化剂是______。
(9)将3.06gKClO3和MnO2混合物以4:1配比加热至完全反应,可得氧气体积约为多少升____?(写出计算过程,计算时精确到小数点后两位。已知氧气密度约为1.43g / L。)
-
某科学兴趣小组利用牙膏中的摩擦剂(由碳酸钙、氢氧化铝组成)选取如下图所示装置(图中夹持仪器略去)模拟工业炼铁。
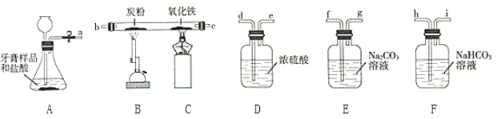
(1)请写出A装置中产生气体的化学方程式____________。
(2)若要制取纯净、干燥的CO2并用于炼铁,所选用装置的导管接口从左到右的正确连接顺序为____________________。
(3)请写出装置C玻璃管中的实验现象_______________。
(4)进行实验时,小组成员发现该套装置有一个明显的不足,应如何改进___________?
(5)A中制取的CO2可用于“侯氏制碱法”,其关键一步的反应原理为:NH3+CO2+H2O+NaCl NaHCO3↓+X,以下说法不正确的是__________。
NaHCO3↓+X,以下说法不正确的是__________。
A.侯氏制碱法的工艺流程应用了物质溶解度的差异
B.生成物X在农业上可用作复合肥
C.NaHCO3在医疗上可用于治疗胃酸过多
(6)将C处中得到的铁加入到硝酸铜和硝酸银的混合溶液中,充分反应后过滤,得到滤渣和滤液。
①滤渣中一定有:__________(填化学式)。
②请写出该过程中可能发生的化学方程式__________。
(7)某同学用足量的一氧化铁还原100g赤铁矿。充分反应后,剩余固体的质量为76g,求100g该赤铁矿中所含氧化铁的质量______________(杂质与一氧化碳不反应)。
-
某兴趣小组利用海水(含 NaCl、MgCl2 和 CaCl2 等可溶性杂质及泥沙等难溶性杂质)和石灰石为原料制取漂白粉,流程如下:
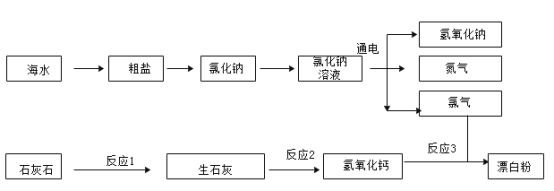
①海水暴晒得到粗盐,利用了氯化钠的溶解度随温度升高而______(选填“变大”、“变小”或“变化不大”)的 性质。
②粗盐提纯得到固体氯化钠,发生了______(填编号)。
A物理变化 B化学变化
③提纯操作中,过滤时用到了铁架台、烧杯、______(填仪器名称)。
④氯化钠溶液通电后发生的不是分解反应,判断的依据是______。
⑤反应1中的化学方程式______。
⑥设计实验方案证明石灰石已完全分解。
| 实验 | 现象 | 结论 |
| ______ | ________ | 石灰石已完全分解 |
⑦实际工业生产中,反应3化学方程式:2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2X,X 的化学式为______,Ca(ClO)2中氯元素的化合价为______,反应物氢氧化钙最好用______(填“饱和石灰水”或“石灰乳”)并不断搅拌。














