-
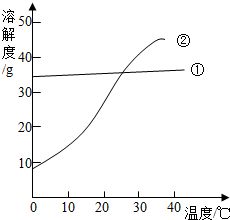
(2008•梅州)我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如下图所示,据图回答下列问题:
(1)t1℃时,溶解度较大的物质是.
(2)等质量Na2CO3、NaCl饱和溶液分别从t2℃降温到t1℃,析出晶体较多的是.
(3)冬天捞碱的原因是由于Na2CO3的溶解度随温度降低而(填“增大”、“减小”或“不变”).
(4)夏天晒盐是利用(填序号)的方法,使NaCl晶体析出.
①升高温度,使NaCl溶解度增大 ②风吹日晒.使溶剂蒸发.
-
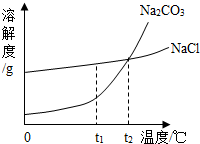
我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如图所示.据图回答下列问题:
(1)t1℃时,溶解度较大的物质是________.
(2)t1℃时把10g Na2CO3固体放入100g水中,充分溶解后,可制得________的碳酸钠溶液(填“饱和”或“不饱和”).
(3)人们冬天捞碱的原因是________(4)将75克20%的NaCl溶液稀释成15%的NaCl溶液,需要加水________mL(水的密度为1g/cm3).在用量筒量取水的体积时,如采用图所示的方法读取数据(其它操作均正确),则所得溶液中溶质的质量分数________15%(选填“<”、“>”或“=”).


-
我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如图所示.据图回答下列问题:
(1)t1℃时,溶解度较大的物质是________.
(2)t1℃时把10g Na2CO3固体放入100g水中,充分溶解后,可制得________的碳酸钠溶液(填“饱和”或“不饱和”).
(3)人们冬天捞碱的原因是________(4)将75克20%的NaCl溶液稀释成15%的NaCl溶液,需要加水________mL(水的密度为1g/cm3).在用量筒量取水的体积时,如采用图所示的方法读取数据(其它操作均正确),则所得溶液中溶质的质量分数________15%(选填“<”、“>”或“=”).


-
我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如图所示.据图回答下列问题:
(1)t1℃时,溶解度较大的物质是________.
(2)t1℃时把10g Na2CO3固体放入100g水中,充分溶解后,可制得________的碳酸钠溶液(填“饱和”或“不饱和”).
(3)人们冬天捞碱的原因是________(4)将75克20%的NaCl溶液稀释成15%的NaCl溶液,需要加水________mL(水的密度为1g/cm3).在用量筒量取水的体积时,如采用图所示的方法读取数据(其它操作均正确),则所得溶液中溶质的质量分数________15%(选填“<”、“>”或“=”).


-
我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如图所示.据图回答下列问题:
(1)t1℃时,溶解度较大的物质是________.
(2)t1℃时把10g Na2CO3固体放入100g水中,充分溶解后,可制得________的碳酸钠溶液(填“饱和”或“不饱和”).
(3)人们冬天捞碱的原因是________(4)将75克20%的NaCl溶液稀释成15%的NaCl溶液,需要加水________mL(水的密度为1g/cm3).在用量筒量取水的体积时,如采用图所示的方法读取数据(其它操作均正确),则所得溶液中溶质的质量分数________15%(选填“<”、“>”或“=”).


-
我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl).Na2CO3和NaCl的溶解度曲线如下图所示,据图回答下列问题:
(1)t1℃时,溶解度较大的物质是________.
(2)等质量Na2CO3、NaCl饱和溶液分别从t2℃降温到t1℃,析出晶体较多的是________.
(3)冬天捞碱的原因是由于Na2CO3的溶解度随温度降低而________(填“增大”、“减小”或“不变”).
(4)夏天晒盐是利用________(填序号)的方法,使NaCl晶体析出.
①升高温度,使NaCl溶解度增大 ②风吹日晒.使溶剂蒸发.

-
(5分)我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl ,那里的人们习惯“夏天晒盐 (NaCl)、冬天捞碱(Na2CO3)”。Na2CO3和NaCl两物质的溶解度曲线如下图所示,据图回答下列问题:

(1)t1℃时,Na2CO3的溶解度 NaCl的溶解度(填“大于”“小于”“等于”之一)。
(2)夏天晒盐是利用___ __(填序号)的方法,使NaCl晶体析出。
①风吹日晒,使溶剂蒸发
②升高温度,使NaCl溶解度增大
(3)等质量的Na2CO3、NaCl饱和溶液分别从t2℃时降温到t1℃,析出晶体后,得到的溶液质量较大的物质是________ _____。
(4)人们习惯“冬天捞碱”的原因是 。
(5)检验“夏天晒盐”所得的食盐中是否混有碳酸钠杂质的方法是 。
-
我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3), 夏天晒盐(NaCl)。Na2CO3和NaCl的溶解度曲线如下图所示。据图回答下列问题:
(1)t1℃时,溶解度较大的物质是__ ①______。
(2)t1℃时把10g Na2CO3固体放入100g水中,充分溶解后,可制得__②___的碳酸钠溶液(填“饱和”或“不饱和”)。
(3)人们冬天捞碱的原因是___ ③____________ 。(4)将3克 NaCl固体配成15%的NaCl溶液,
需要加水④ mL(水的密度为1g/cm3)。在用量筒
量取水的体积时,如采用右图所示的方法读取数据
(其它操作均正确),则所得溶液中溶质的质量分数
________⑤ 15%(选填“<”、“>”或“=”)。
-
我国北方有许多盐湖,湖水中溶有大量的碳酸钠和氯化钠,合理利用自然资源,冬天捞碱(Na2CO3),夏天晒盐(NaCl)。Na2CO3和NaCl的溶解度曲线如图所示,据图回答下列问题:
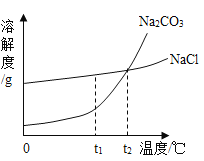
(1)在____℃时,碳酸钠和氯化钠两种物质的溶解度相同。
(2)等质量Na2CO3、NaCl饱和溶液分别从t2℃降温到t1℃,析出晶体较多的是_________。
(3)从湖水中得到的碳酸钠常含有少量的氯化钠,可以采用_____(选填“降温结晶”、“蒸发结晶”或“过滤”)的方法得到较纯净的碳酸钠。
-
(2007•山西)我国北方有许多盐湖,湖水中溶有大量的碳酸钠和氯化钠,那里的农民冬天捞碱(碳酸钠),夏天晒盐(氯化钠).
(1)右图是碳酸钠和氯化钠在不同温度下的溶解度曲线,其中表示碳酸钠溶解度曲线的是______
(2)从湖水中得到的碳酸钠中常含有少量的氯化钠,可以用的方法得到较纯净的碳酸钠______.
(3)20℃时,两物质的溶解度大小关系为A______B.