-
海盐中常含有泥沙,CaCl2MgCI2等杂质,为得到纯净的氯化钠,设计了如下实验,请你帮助完成探究
(1)将海盐加入适量的水,充分搅拌.
(2)加入过量的NaOH溶液和Na2CO3溶液,目的是______.
(3)过滤,用到的仪器是玻璃棒,______,______,______.玻璃棒的作用是______.
(4)加入过量的稀盐酸,目的是______,写出化学方程式:①______,②______.
(5)接下来的操作是______,用到的仪器是玻璃棒______,______,玻璃棒的作用是______.九年级化学解答题中等难度题查看答案及解析
-
某粗盐中含有杂质氯化镁、泥沙、氯化钙、硫酸钠,要得到纯净的氯化钠,某同学设计如下实验:

回答下列问题:
(1)经过操作①后,过滤得到滤渣,滤渣中除了泥沙外,还含有__________(化学式)。
(2)写出加入过量碳酸钠溶液后,发生反应的化学方程式_____________。(任写一个)
(3)若加入的试剂a为稀硫酸,则会引起的后果是什么_____________?
九年级化学流程题中等难度题查看答案及解析
-
实验室有一瓶除去难溶性杂质的粗盐样品,其中还含有少量的氯化镁和氯化钙。为了得到较纯净的食盐晶体,同学们设计如下实验方案,请你参与他们的实验探究。
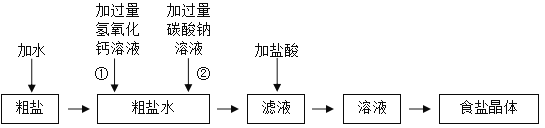
(1)实验过程中,向粗盐水中先加入过量的氢氧化钙溶液,再加入过量的碳酸钠溶液,依次加入的目的是_____,写出两种盐之间发生反应的化学方程式_____。
(2)实验过程中,用到的操作有_____,得到食盐晶体时,应在_____中进行。
九年级化学流程题中等难度题查看答案及解析
-
(2010•金山区二模)粗食盐中含有少量氯化镁、硫酸钠等可溶性杂质和泥沙等难溶性杂质.某研究小组设计了如下的实验,以便从粗食盐中提取纯净的氯化钠.先后加入的两种试剂都恰好完全反应.已知白色沉淀A能溶于酸,而白色沉淀B不溶于硝酸.
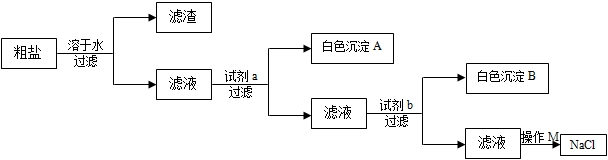
①试剂a是一种可溶性碱,那么白色沉淀A是______;
②加入试剂b发生反应的化学方程式是______
③操作M是______.九年级化学解答题中等难度题查看答案及解析
-
粗盐中含有氯化镁、硫酸钠等可溶性杂质和泥沙等难溶性杂质.某研究小组为了从粗盐中提取纯净的食盐,设计了如下的实验:为了使粗盐中的氯化镁、硫酸钠等杂质完全转化为沉淀,所有加入的每种试剂均过量;已知白色沉淀A能溶于酸,而白色沉淀B不溶于稀硝酸.
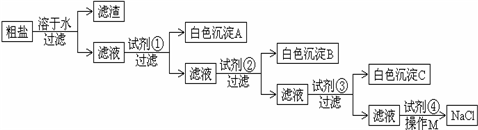
(1)试剂①是一种可溶性碱,那么白色沉淀A是________.
(2)试剂③是________.
(3)加入试剂④发生的反应中属于中和反应的化学方程式是:________.
(4)操作M是________.九年级化学填空题中等难度题查看答案及解析
-
粗盐中含有氯化镁、硫酸钠等可溶性杂质和泥沙等难溶性杂质.某研究小组为了从粗盐中提取纯净的食盐,设计了如下的实验:为了使粗盐中的氯化镁、硫酸钠等杂质完全转化为沉淀,所以加入的每种试剂均过量;已知白色沉淀A能溶于酸,而白色沉淀B不溶于硝酸.
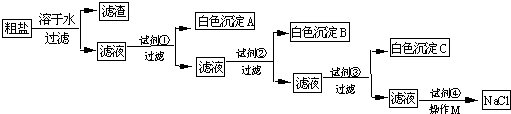
(1)试剂①是一种可溶性碱,那么白色沉淀A是______,试剂②是______,
(2)加入试剂④发生反应的化学方程式是:______.
(3)操作M是______.九年级化学解答题中等难度题查看答案及解析
-
某粗盐中含有杂质氯化镁、氯化钙、硫酸铵、泥沙,要得到纯净的氯化钠,某同学涉及如下实验:
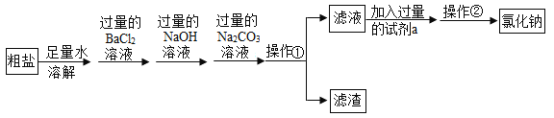
(1)写出加入过量碳酸钠的化学方程式_________。(任写一个)
(2)若加入的试剂a为稀硫酸,则会引发的后果是什么_________?
九年级化学流程题中等难度题查看答案及解析
-
某粗盐中含有杂质氯化镁、氯化钙、硫酸铵、泥沙,要得到纯净的氯化钠,某同学涉及如下实验:

(1)写出加入过量碳酸钠的化学方程式_________。(任写一个)
(2)若加入的试剂a为稀硫酸,则会引发的后果是什么_________?
九年级化学流程题中等难度题查看答案及解析
-
某粗盐中除含泥沙外,还含有 CaCl2 和 Na2SO4 等可溶性杂质,为得到纯净的氯化钠,进行如下操作:①加过量的 Na2CO3 溶液;②加过量的 BaCl2 溶液;
③蒸发结晶;④过滤;⑤加适量的盐酸至溶液呈中性;⑥取适量粗盐溶解。上述操作的正确顺序为(每项操作只能选择一次)_______________(填序号);操作①的目的是_______________;操作④需要用到的玻璃仪器有________。
九年级化学实验题简单题查看答案及解析
-
某化学课外活动小组欲从含少量泥沙、氯化镁、氯化钙等杂质的粗盐中得到精盐,设计了如下方案:
方案l:溶解→过滤→加入过量Na2CO3→过滤→加入适量HCl,调节pH→蒸发
方案2:溶解→过滤→加入过量NaOH→加入过量Na2CO3→过滤→加入适量HCl,调节pH→蒸发
方案3:溶解→过滤→加入过量石灰乳→加入过量Na2CO3→过滤→加入适量HCl,调节pH→蒸发
相关信息
信息一:石灰乳中含有较多未溶解的Ca(OH)2
信息二:部分物质溶解性:MgCO3微溶、CaCO3难溶、Mg(OH)2难溶、Ca(OH)2微溶
信息三:部分化学试剂的市场价格
请根据题目要求及以上信息,回答下列问题:试剂 NaOH Ca(OH)2 价格 2305.00 1200.00
(1)上述每个方案都设计了两次过滤,第一次过滤的作用是______;每个方案中都设计要调节pH,其值为______.
(2)通过分析,活动小组的同学认为上述方案3设计是最合理的.那么方案3优于方案2的理由是______,
方案l的不足之处是______.
方案3中发生反应的化学方程式为______;______.(写出其中两个)
(3)方案3中选用石灰乳而不选用澄清石灰水的原因是______.
A.澄清石灰水中含Ca(OH)2较少,石灰乳中含Ca(OH)2较多
B.澄清石灰水中Ca(OH)2的浓度较小,选用澄清石灰水稀释了原溶液,使蒸发时间延长
C.石灰乳中溶解了的Ca(OH)2不断参与反应,未溶解的Ca(OH)2不会溶解补充
D.石灰乳中溶解了的Ca(OH)2不断参与反应,未溶解的Ca(OH)2不断溶解补充.九年级化学解答题中等难度题查看答案及解析