-
为了测定某含杂质7%的黄铜样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:
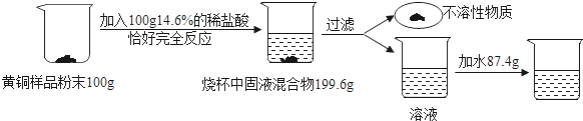
(1)配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是 _______.
(2)发生反应的化学方程式为________.
(3)根据已知条件列出求解100g该黄铜样品中锌的质量(X)的比例式为________.
(4)该黄铜样品中铜的质量分数是________ .
(5)向过滤后所得滤液中加入87.4g水,则最终所得溶液之中溶质的质量分数是 ________ .
(6)欲将黄铜样品中的铜转化为铜盐,可将过滤后所得的不溶性物质洗涤、烘干.然后在空气中加热,充分反应,则可得到含杂质的氧化铜的质量是_______,再经过某些反应操作就得到了所需铜盐.
-
(6分)为了测定某含杂质7%的黄铜样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:
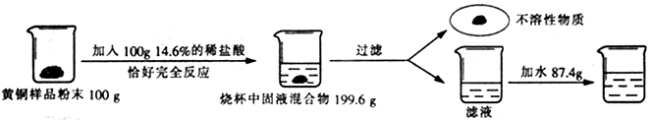
(1)配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是______;
(2)发生反应的化学方程式为____________________________________________;
(3)根据已知条件列出求解100g该黄铜样品中锌的质量(x)的比例式为__________;
(4)该黄铜样品中铜的质量分数是__________;
(5)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数是__________;
(6)欲将黄铜样品中的铜转化为铜盐,可将过滤后所得的不溶性物质洗涤、烘干,然后在空气中加热,充分反应,则可得到含杂质的氧化铜的质量是__________,再经过某些反应及操作就得到了所需铜盐。
-
为了测定某含杂质5%的黄铜样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:
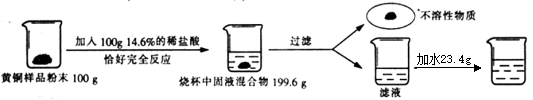
(1)配制上述质量分数为14.6%的稀盐酸,需质量分数为36.5%的浓盐酸质量是_ ;
(2)发生反应的化学方程式为___________________;
(3)根据已知条件列出求解100g该黄铜样品中锌的质量(x)的比例式为_____ ;
(4)该黄铜样品中铜的质量分数是__________ ;
(5)向过滤后所得滤液中加入23.4g水,则最终所得溶液中溶质的质量分数是___ 。
-
为了测定某含杂质的黄铜(铜锌合金)样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应),某化学小组进行了如下实验:
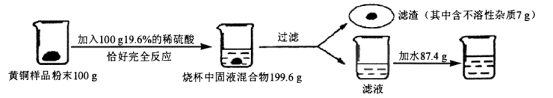
(1)配制100 g19.6%的稀硫酸,需要溶质质量分数为98%的浓硫酸的质量是 ;
(2)该黄铜样品中铜的质量分数是 ;
(3)向过滤后所得滤液中加入87.4g水,计算最终所得溶液的溶质质量分数。(计算结果精确至0.1% )
-
为了测定某氧化铁样品中氧化铁的质量分数,某化学小组设计了如图所示装置进行实验。

已知:样品中的杂质不含铁元素,且不溶于水和酸;草酸在浓硫酸作用下受热分解生成CO2、CO和H2O;碱石灰主要成分为生石灰与氢氧化钠固体。请回答:
(问题讨论)
(1)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是________(填序号)。
①浓硫酸 ②氢氧化钠溶液 ③澄清石灰水
(2)B中发生反应的化学方程式为___________。
(3)C装置的作用是_________。
(数据处理)
(4)称取样品5.0 g,用上述装置进行实验,充分反应后称量F装置,发现比反应前增重3.3 g。则样品中氧化铁的质量分数为_______。
(实验反思)
(5)该实验装置有一明显缺陷是_______。
(6)如果没有G装置,则测得的样品中氧化铁的质量分数_______(填“偏大”、“偏小”或“无影响”)。
-
为了测定某氧化铁样品中氧化铁的质量分数,某化学小组设计了如图所示装置进行实验。
已知:样品中的杂质不含铁元素,且不溶于水和酸;草酸(H2C2O4)在浓硫酸作用下受热分解生成CO2、CO和H2O,碱石灰主要成分为生石灰与氢氧化钠固体。请回答:

(问题讨论)
(1)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是_____(填序号)。
①浓硫酸 ②氢氧化钠溶液 ③澄清石灰水
(2)B中发生反应的化学方程式为_____。
(3)C和G装置的作用分别是_____。
(数据处理)称取样品5.0g,用上述装置进行实验,充分反应后称量F装置,发现比反应前增重3.3g,则样品中氧化铁的质量分数为_____。
(实验反思)(1)该实验装置有一明显缺陷是_____。
(2)如果没有G装置,则测得的样品中氧化铁的质量分数_____(填“偏大”、“偏或“无影响”)。
(迁移应用)试计算,加热分解90t质量分数为20%的草酸溶液,能制得多少一氧化碳?_____
-
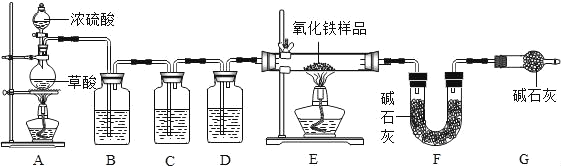
为了测定某氧化铁样品中氧化铁的质量分数,某化学小组设计了如图所示装置进行实验。
已知:样品中的杂质不含铁元素,且不溶于水和酸;草酸(H2C2O4)在浓硫酸作用下受热分解生成CO2、CO和H2O,碱石灰主要成分为生石灰与氢氧化钠固体。请回答:
(问题讨论)
(1)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是_____(填序号)。
①浓硫酸 ②氢氧化钠溶液 ③澄清石灰水
(2)B中发生反应的化学方程式为_____。
(3)C和G装置的作用分别是_____。
(数据处理)称取样品5.0g,用上述装置进行实验,充分反应后称量F装置,发现比反应前增重3.3g,则样品中氧化铁的质量分数为_____。
(实验反思)(1)该实验装置有一明显缺陷是_____。
(2)如果没有G装置,则测得的样品中氧化铁的质量分数_____(填“偏大”、“偏或“无影响”)。
(迁移应用)试计算,加热分解90t质量分数为20%的草酸溶液,能制得多少一氧化碳?_____
-
(10分)为了测定某样品中氧化铁(Fe2O3)的质量分数(杂质不含铁元素,且不溶于水和酸),化学兴趣小组的同学进行了如下的实验。
【查阅资料】
1.草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为:
H2C2O4  CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
2.碱石灰能吸收二氧化碳和水蒸气
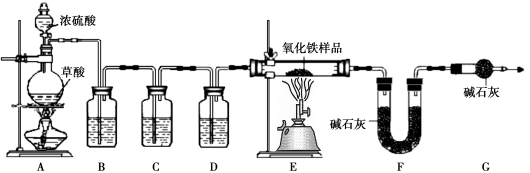
【实验设计及操作】用下图所示装置进行实验:
【问题讨论】
(1)装药品前应先 ,实验中观察到E中现象是:固体颜色 ;
(2)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是 (填序号)。
① 浓硫酸、石灰水、氢氧化钠溶液
② 石灰水、氢氧化钠溶液、浓硫酸
③ 氢氧化钠溶液、石灰水、浓硫酸
(3)G的作用是 ;E中反应的化学方程式是 ;
(4)当E中固体完全反应后, 处应先停止加热(填序号A或E);
(5)上述实验装置的一处明显缺陷是: 。
【数据处理】
称取样品8.0g,用上述装置进行实验,充分反应后称量F装置增重4.4g。则样品中氧
化铁质量分数为 。
【实验反思】
当观察到E中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数
(填“偏大”,“偏小”,“无影响”)。
-
为了测定某样品中氧化铁(Fe2O3)的质量分数(杂质不含铁元素,且不溶于水和酸),化学兴趣小组的同学进行了如下的实验。
(查阅资料)
1.草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为:
H2C2O4  CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
2.碱石灰能吸收二氧化碳和水蒸气
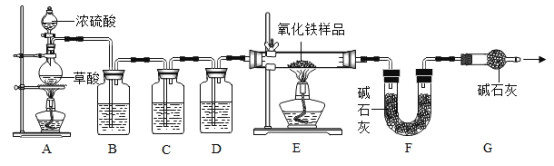
(实验设计及操作)用下图所示装置进行实验:
(问题讨论)
(1)装药品前应先 ,实验中观察到E中现象是:固体颜色 ;
(2)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是 (填序号)。
① 浓硫酸、石灰水、氢氧化钠溶液
② 石灰水、氢氧化钠溶液、浓硫酸
③ 氢氧化钠溶液、石灰水、浓硫酸
(3)G的作用是 ;E中反应的化学方程式是 ;
(4)当E中固体完全反应后, 处应先停止加热(填序号A或E);
(5)上述实验装置的一处明显缺陷是: 。
(数据处理)
称取样品8.0g,用上述装置进行实验,充分反应后称量F装置增重4.4g。则样品中氧
化铁质量分数为 。
(实验反思)
当观察到E中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数
(填“偏大”,“偏小”,“无影响”)。
-
普通食盐的主要成份是NaCl和杂质,假设杂质不溶于水、受热不分解、与AgNO3不反应。王华同学测定普通食盐样品中氯化钠的质量分数时所进行的实验操作流程和实验数据如下图所示。
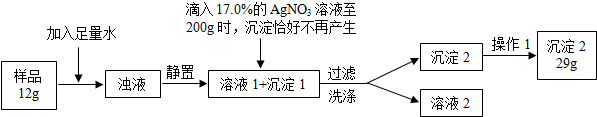
(实验中发生的化学反应方程式为:AgNO3+NaCl=AgCl↓+NaNO3)
请你完成空格和计算:
(1)王华进行操作1的目的是 ________ _;
(2)求算样品中氯化钠的质量分数。(结果保留小数点后1位)









