-
(10湛江15).电子工业制作电路板的过程中,用FeCl3溶液来溶解电路板中多余的铜,反应如下: 2FeCl3+Cu==2FeCl2+CuCl2。FeCl3溶液也可跟铁发生反应:2FeCl3+Fe==3FeCl2。现向FeCl3溶液中加入一定量的铁粉和铜粉,充分反应后,发现有固体剩余。下面有关说法正确的是
A.向剩余的固体加入稀盐酸,若无气体放出,说明反应后的溶液中没有Cu2+
B.若剩余固体是铜与铁的混合物,则说明两种金属都有部分溶解
C.剩余固体可能只含有铜
D.剩余固体中如果有铁,一定也有铜
九年级化学选择题中等难度题查看答案及解析
-
(2010•湛江)电子工业制作电路板的过程中,用FeCl3溶液来溶解电路板中多余的铜,反应如下:2FeCl3+Cu═2FeCl2+CuCl2.FeCl3溶液也可跟铁发生反应:2FeCl3+Fe═3FeCl2.现向FeCl3溶液中加入一定量的铁粉和铜粉,充分反应后,发现有固体剩余.下面有关说法正确的是( )
A.向剩余的固体加入稀盐酸,若无气体放出,说明反应后的溶液中没有Cu2+ B.若剩余固体是铜与铁的混合物,则说明两种金属都有部分溶解 C.剩余固体可能只含有铜 D.剩余固体中如果有铜,一定也有铁 九年级化学选择题中等难度题查看答案及解析
-
电子工业制作电路板的过程中,用FeCl3溶液来溶解电路板中多余的铜,反应如下:2FeCl3+Cu═2FeCl2+CuCl2.FeCl3溶液也可跟铁发生反应:2FeCl3+Fe═3FeCl2.现向FeCl3溶液中加入一定量的铁粉和铜粉,充分反应后,发现有固体剩余.下面有关说法正确的是( )
A.向剩余的固体加入稀盐酸,若无气体放出,说明反应后的溶液中没有Cu2+
B.若剩余固体是铜与铁的混合物,则说明两种金属都有部分溶解
C.剩余固体可能只含有铜
D.剩余固体中如果有铜,一定也有铁九年级化学选择题中等难度题查看答案及解析
-
电子工业制作电路板的过程中,用FeCl3溶液来溶解电路板中多余的铜,反应如下:2FeCl3+Cu═2FeCl2+CuCl2.FeCl3溶液也可跟铁发生反应:2FeCl3+Fe═3FeCl2.现向FeCl3溶液中加入一定量的铁粉和铜粉,充分反应后,发现有固体剩余.下面有关说法不正确的是( )
A.向剩余的固体加入稀盐酸,若无气体放出,说明反应后的溶液中没有Cu2+
B.若剩余固体是铜与铁的混合物,则说明反应后的溶液中只有Fe2+
C.剩余固体可能只含有铜
D.剩余固体中如果有铁,一定也有铜九年级化学选择题中等难度题查看答案及解析
-
制印刷电路时,常用氯化铁溶液作为腐蚀液,将铜腐蚀掉。其反应方程式为:FeCl3+Cu→2FeCl2+CuCl2。现向氯化铁溶液中加入a g铜,完全溶解后,再加入b g铁,充分反应后得到c g残余固体,且a>c。则下列说法正确的是
A.c g残余固体全部是铜
B.c g残余固体可能为铁和铜的混合物
C.最后得到的溶液中可能含有+3价Fe元素
D.溶液中一定不含Cu元素
九年级化学选择题中等难度题查看答案及解析
-
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(主要含有FeCl2和CuCl2)处理和资源回收的工业流程如下:
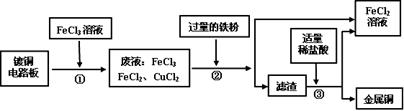
试回答下列问题:
(1)过程①中Cu和FeCl3反应的化学方程式:________;过程②加入铁屑后发生的置换反应的化学方程式:________;
(2)步骤②得到滤渣的成分是________;步骤③的操作是过滤、________、干燥等。
(3)Fe(OH)2与O2和H2O反应生成________色Fe(OH)3。写出相关的化学方程式为:________。
九年级化学填空题困难题查看答案及解析
-
在电子工业上,常用氯化铁溶液来腐蚀铜,制造电路板.据报道,通常状况下,铜与氯化铁溶液反应转化为氯化铜(氯化铜能溶于水).
(1)请完成该反应的化学方程式:Cu+2FeCl3═CuCl2+2______,该反应______(填“属于”或“不属于”)置换反应.
(2)若把一块铜板(足量)放入1000g溶质质量分数为16.25%的氯化铁溶液中,充分反应,待反应停止后取出铜片(假设无其它反应发生,操作过程中无损耗).
求:
①反应前溶液中溶质的质量.
②反应后所得溶液的质量.九年级化学解答题中等难度题查看答案及解析
-
(2008•烟台)印刷铜制电路板的“腐蚀液”为FeCl3溶液.已知铜、铁均能与FeCl3溶液反应,反应方程式为:Cu+2FeCl3=2FeCl2+CuCl2;Fe+2FeCl3=3FeCl2.现将一包铜、铁的混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,关于烧杯中物质组成的说法正确的是( )
A.溶液中一定含有FeCl3,固体一定是Fe和Cu B.溶液中一定含有FeCl2,固体一定含Cu C.溶液中一定含有FeCl2,固体可能含Fe D.溶液中可能含有FeCl3,固体可能含Cu 九年级化学选择题中等难度题查看答案及解析
-
印刷铜制电路板的“腐蚀液”是FeCl3溶液。已知铜铁均能与FeCl3溶液反应,反应的化学方程式分别为Cu+2FeCl3===2FeCl2+CuCl2,Fe+2FeCl3===3FeCl2。现将一包铜铁的混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后,烧杯中仍有少量固体,关于烧杯中物质组成的说法中正确的是( )
A. 溶液中一定含有FeCl3,固体一定是铁和铜
B. 溶液中一定含FeCl2,固体一定含铜
C. 溶液中一定含FeCl2、CuCl2,固体一定含铜
D. 溶液中一定含有FeCl2,固体一定是铁和铜
九年级化学单选题中等难度题查看答案及解析
-
印刷铜制电路板的“腐蚀液”是FeCl3溶液。已知铜铁均能与FeCl3溶液反应,反应的化学方程式分别为Cu+2FeCl3===2FeCl2+CuCl2,Fe+2FeCl3===3FeCl2。现将一包铜铁的混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后,烧杯中仍有少量固体,关于烧杯中物质组成的说法中正确的是( )
A.溶液中一定含有FeCl3,固体一定是铁和铜
B.溶液中一定含FeCl2,固体一定含铜
C.溶液中一定含FeCl2、CuCl2,固体一定含铜
D.溶液中一定含有FeCl2,固体一定是铁和铜
九年级化学单选题中等难度题查看答案及解析