-
质量守恒定律的发现,对化学的发展作出了重要贡献。
(1)通过分别称量下列两组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是__(填标号)。
a.大理石和稀盐酸 b.NaOH溶液和Na2SO4溶液
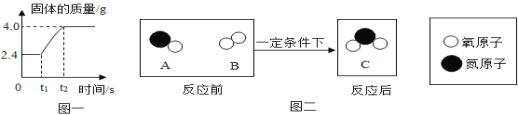
(2)在足量氧气中点燃镁条的实验过程中,固体质量变化如图一。
①从燃烧条件分析,固体质量在t1前没有发生变化的原因是__。
②该反应的化学方程式为__;
③参加反应的氧气质量为__g。
(3)在一定条件下,A和B反应生成C,微观示意图如图二。回答下列问题:
①一个A分子由__个原子构成;
②C分子中元素的质量比N:O=__;
③该反应的化学基本反应类型为__;
④上述反应中一定发生改变的是__(填标号)。
a.元素种类 b.原子种类 c.分子种类
-
质量守恒定律的发现,对化学的发展作出了重要贡献。
(1)通过分别称量下列两组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是__(填标号)。
a.大理石和稀盐酸 b.NaOH溶液和Na2SO4溶液
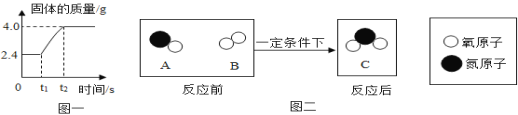
(2)在足量氧气中点燃镁条的实验过程中,固体质量变化如图一。
①从燃烧条件分析,固体质量在t1前没有发生变化的原因是__。
②该反应的化学方程式为__;
③参加反应的氧气质量为__g。
(3)在一定条件下,A和B反应生成C,微观示意图如图二。回答下列问题:
①一个A分子由__个原子构成;
②C分子中元素的质量比N:O=__;
③该反应的化学基本反应类型为__;
④上述反应中一定发生改变的是__(填标号)。
a.元素种类 b.原子种类 c.分子种类
-
质量守恒定律的发现,对化学的发展做出了重要贡献。

(1)通过分别称量下列两组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是______(填标号)。
a、大理石和稀盐酸 b、食盐和水
(2)在足量氧气中点燃镁条的实验过程中,固体质量变化如图一。
①从燃烧条件分析,固体质量在 前没有发生变化的原因是______;
前没有发生变化的原因是______;
②该反应的化学方程式为______;
③参加反应的氧气质量为______g。
(3)在一定条件下,A和B反应生成C,微观示意图如图二。回答下列问题:
①一个A分子由______个原子构成;
②C分子中元素的质量比 ______;
______;
③该反应的化学基本反应类型为______:
④上述反应中一定发生改变的是______(填标号)。
a、元素种类 b、原子种类 c、分子种类
-
质量守恒定律的发现,对化学的发展做出了重要贡献。

(1)通过分别称量下列两组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是____(填标号)。
a大理石和稀盐酸 bNaOH溶液和Na2SO4溶液
(2)在足量氧气中点燃镁条的实验过程中,固体质最变化如图一。
①从燃烧条件分析,固体质量在t1前没有发生变化的原因是___________。
②该反应的化学方程式为__________。
③参加反应的氧气质量为__________g。
(3)在一定条件下,A和B反应生成C,微观示意图如图二。回答下列问题:
①一个A分子由____个原子构成。
②C分子中元素的质量比N:O=____。
③上述反应中一定发生改变的是___________(填标号)。
a元素种类b原子种类c分子种类
-
质量守恒定律是自然界的普遍规律,它的发现对化学的发展做出了重要贡献。
(1)下列各组试剂中,通过称量在密闭容器内混合前后的总质量,不能验证质量守恒定律的是____(填字母)。
A.碘和酒精 B.碳酸钠粉末和少量稀盐酸
C.铁和氯化铜溶液 D.氢氧化钠溶液和硫酸铜溶液
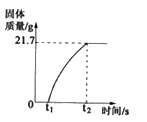
(2)1774年,拉瓦锡用精确的定量实验研究了汞和氧气反应的质量关系。若用一定质量的汞和足量氧气充分反应,生成固体的情况如图所示,则有关反应的化学方程式为__________;参加反应的氧气质量为__________g。
(3)如图是某反应的微观示意图。
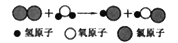
①该反应类型______(填“属于”或“不属于”)置换反应;其中化合价发生改变的元素是_____。
②已知:Cl2+2NaOH=NaCl+NaClO+H2O。氯气和熟石灰反应可以制得漂白粉,该反应的化学方程式为____________;Ca(ClO)2在空气中与二氧化碳和水反应会转化为CaCO3和HClO,该反应的化学方程式为____________。
(4)实验室取34g过氧化氢溶液和1g二氧化锰混合制取氧气,充分反应后,称量剩余溶液和滤渣为34. 2g。则所取过氧化氢溶液中溶质的质量分数是多少?______
-
Ⅰ质量守恒定律的发现对化学的发展做出了重要贡献。
(1)通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是 (填标号)。
A.蔗糖和水 B.氯化钠溶液和硝酸钾溶液 C.铁和氯化铜溶液
(2)在氧气中点燃红磷的实验过程,固体变化如图所示。

①从燃烧条件分析,固体质量在t1前没有发生变化的原因是 。
②该反应的化学方程式为 。
③参加反应的氧气质量为 g。
(3)某反应的微观示意图如图所示:

①该反应所属的基本反应类型为 。
②参加反应的甲物质和生成的丙物质分子数目比为 。
Ⅱ.甲和乙两种固态物质的饱和溶液中溶质质量分数与温度的关系如图所示。
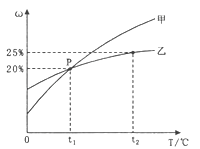
(1)甲和乙两种物质的溶解度随温度的升高而 (填“增大”或“减小”)。
(2)下列对P点的含义叙述正确的是 (填标号)。
A.t1℃时,甲和乙两种物质的溶解度相等
B.t1℃时,甲和乙两种物质溶液的溶质质量分数相等
C.t1℃时,甲和乙两种物质的饱和溶液中溶质的质量相等
(3)25g乙物质完全溶于100g水中所需的最低温度是 ℃。
(4)t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是 (填“甲”或“乙”)物质饱和溶液。
-
质量守恒定律的发现对化学的发展做出了重要贡献。
(1)通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是__(填标号)
A.蔗糖和水 B.氯化钠溶液和硝酸钾溶液 C.信和氯化铜溶液
(2)在氧气中点燃红磷的实验过程中,固体质量变化如图1所示:
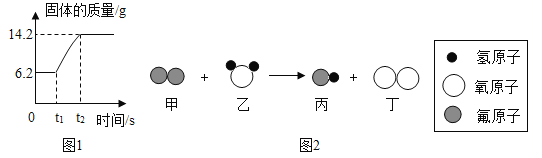
①利用燃烧条件分析,固体质量在t1前没有发生变化的原因为_______________
②参加反应的氧气质量为__________________________________________g
(3)某反应的微观示意图如图2所示:
参加反应的甲物质和生成物丙物质的分子数目之比为__________________________________。
-
Ⅰ.质量守恒定律的发现对化学的发展做出了重要贡献。
(1)通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的
是____________(填数字序号)。
① 食盐和水 ② 氯化钠溶液和硝酸钾溶液 ③ 铁和氯化铜溶液
(2)某反应的微观示意图如下图所示:
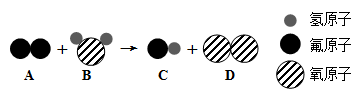
① A的化学式为_________。
② 该反应所属的基本反应类型为___________________反应。
③ 参加反应的A物质和生成的C物质分子数目比为____________________。
Ⅱ.甲和乙两种固态物质的饱和溶液中溶质质量分数与温度的关系如右图所示:
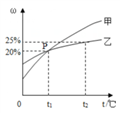
(1)甲和乙两种物质的溶解度随温度的升高而___________(填“增大”或“减小”)。
(2)下列对P点的含义叙述正确的是_____________(填字母序号)。
A.t1℃时,甲和乙两种物质的溶解度相等
B.t1℃时,甲和乙两种物质溶液的溶质质量分数相等
C.t1℃时,甲和乙两种物质的饱和溶液中溶质的质量相等
(3)25 g乙物质完全溶于100g水中所需的最低温度是________℃。
(4)t2℃时,若甲和乙两种物质的饱和溶液中析出等量的固体须蒸发掉较多水的是_________(填“甲”或“乙”)物质饱和溶液。
-
Ⅰ、质量守恒定律的发现对化学的发展做出了重要贡献。
⑴通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是________(填标号),有关反应的化学方程式为_______________。
A.蔗糖和水 B.氯化钠溶液和硝酸钾溶液 C.铁和氯化铜溶液
⑵在氧气中点燃红磷的实验过程,固体变化如图所示。

①燃烧条件分析,固体质量在t1前没有发生变化的原因是____________________。
②该反应的化学方程式为_____________________。
③参加反应的氧气质量为_________g。
⑶某反应的微观示意图如图所示:
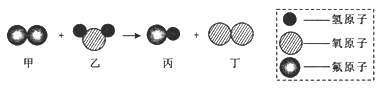
①该反应所属的基本反应类型为______________。
②参加反应的甲物质和生成的丙物质分子数目比为__________。
Ⅱ、甲和乙两种固态物质的饱和溶液中溶质质量分数与温度的关系如图所示。
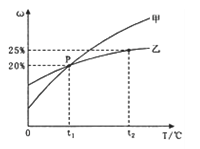
⑴ 甲和乙两种物质的溶解度随温度的升高而______(填“增大”或“减小”)。
⑵ 下列对P点的含义叙述正确的是______(填标号)。
A.t1℃时,甲和乙两种物质的溶解度相等
B.t1℃时,甲和乙两种物质溶液的溶质质量分数相等
C.t1℃时,甲和乙两种物质的饱和溶液中溶质的质量相等
⑶ 25g乙物质完全溶于100g水中所需的最低温度是______℃。
⑷ t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是________(填“甲”或“乙”)物质饱和溶液。
-
Ⅰ、质量守恒定律的发现对化学的发展做出了重要贡献。
⑴通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是______(填标号),有关反应的化学方程式为_______________。
A.蔗糖和水 B.氯化钠溶液和硝酸钾溶液 C.铁和氯化铜溶液
⑵在氧气中点燃红磷的实验过程,固体变化如图6所示。

①燃烧条件分析,固体质量在t1前没有发生变化的原因是_______________________。
②该反应的化学方程式为_____________________。
③参加反应的氧气质量为_________g。
⑶某反应的微观示意图如图7所示:
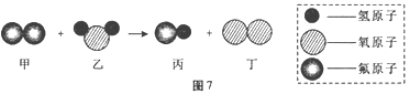
①该反应所属的基本反应类型为_________________。
②参加反应的甲物质和生成的丙物质分子数目比为__________。
Ⅱ、甲和乙两种固态物质的饱和溶液中溶质质量分数与温度的关系如图8所示。

⑴ 甲和乙两种物质的溶解度随温度的升高而____(填“增大”或“减小”)。
⑵ 下列对P点的含义叙述正确的是__________(填标号)。
A.t1℃时,甲和乙两种物质的溶解度相等
B.t1℃时,甲和乙两种物质溶液的溶质质量分数相等
C.t1℃时,甲和乙两种物质的饱和溶液中溶质的质量相等
⑶ 25g乙物质完全溶于100g水中所需的最低温度是______℃。
⑷ t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是_________(填“甲”或“乙”)物质饱和溶液。

















