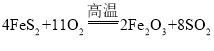-
硫酸是一种重要的化工原料,也是实验室中常用的化学试剂。下面是对硫酸的性质、制取、用途等方面的探究,请你共同参与并回答有关问题。
(探究一)硫酸的性质
(1)探究浓硫酸的某些特性。
①用小木棍蘸取少量浓硫酸,放置一会后,可观察到___。
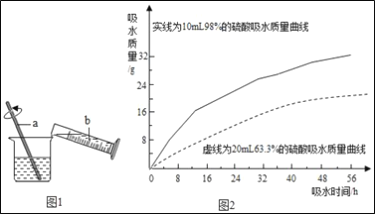
②浓硫酸的稀释:浓硫酸稀释过程如图1所示,b中盛放的物质是___,a的作用是___。
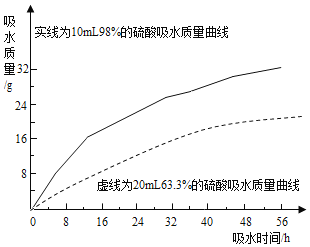
③兴趣小组把98%的浓硫酸10ml和63.3%的硫酸溶液约20mL分别放入两个相同的小烧杯中,称量、观察、记录、分析,根据室温环境下实验的数据绘成的曲线如图2.由图2曲线你能得到的实验结论:_____(写两点)。
(2)探究稀硫酸的化学性质。
如图3将适量的稀硫酸分别加入A~E的五只烧杯中。
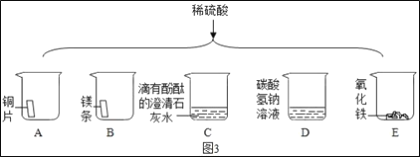
①有产生气泡的是___(填序号,下同);有白色沉淀生成的是___。
②能证明C中发生化学反应的现象是___。
(3)请写出稀硫酸的一种用途___。
(探究二)硫酸的工业制法。
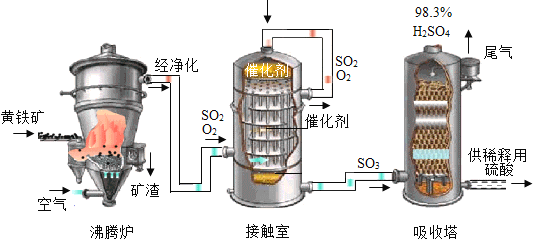
工业上以黄铁矿为原料生产硫酸的工艺流程如图4所示。
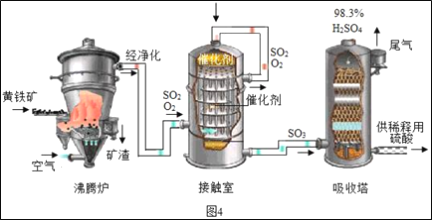
(1)接触室中发生的化学方程式为___。
(2)依据生产硫酸的工艺流程图,下列说法正确的是___(填字母序号)。
A 为使黄铁矿充分燃烧,需将其粉碎 B 催化剂能够提高SO2的反应速率和产量
C 吸收塔中得到的产品为混合物 D 沸腾炉排出的矿渣可供炼铁
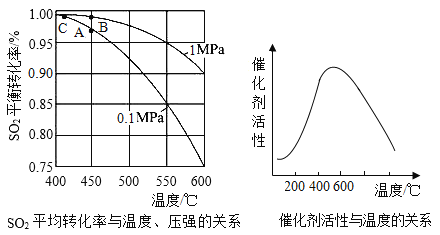
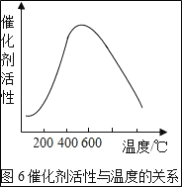
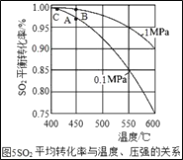
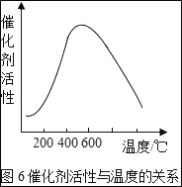
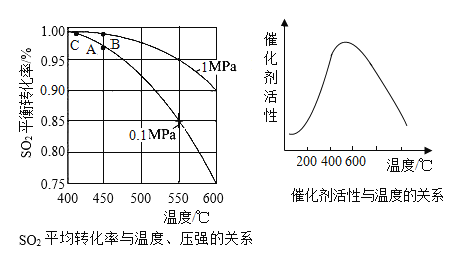
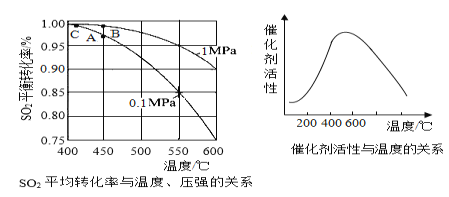
(3)接触室中的SO2平衡转化率与温度及压强的关系如图5所示。催化剂活性与温度的关系见图6.在实际生产中,SO2催化氧化反应的条件选择常压和450℃(对应图中A点),而没有选择SO2转化率更高的B或C点对应的反应条件,其原因分别是___;___。

(探究三)探究某黄铁矿中FeS2的含量。
同学们进行了如下实验探究。
(查阅资料)①4FeS2 +11O2  2Fe2O3+8SO2
2Fe2O3+8SO2
②Na2SO3 +H2O2 =Na2SO4 +H2O
(实验探究)
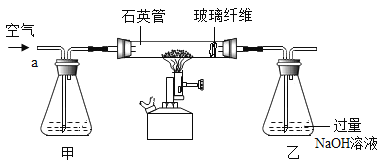
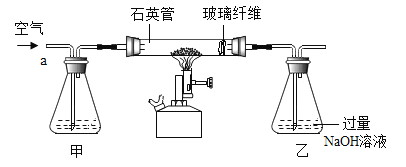
Ⅰ称取1.60g黄铁矿样品放入如图7所示装置(夹持装置省略)的石英管中,从a处不断地缓缓通入空气、高温灼烧石英管中的黄铁矿样品至完全反应。
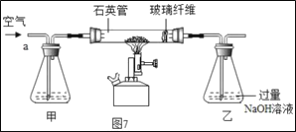
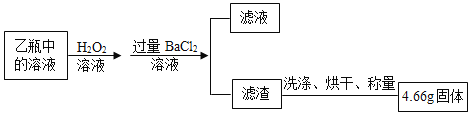
Ⅱ反应结束后,将乙瓶中的溶液进行如图8处理

(问题讨论)
(1)I中装置甲瓶内盛放的试剂是氢氧化钠溶液,其作用是___;II中滤液所含的溶质一定有___。
(含量测定)
(2)II中最终得到的4.66g固体是___(填化学式)。
(3)计算该黄铁矿中FeS2的质量分数为___。(写出计算过程)
(交流反思)
(4)如果缺少甲装置,则最终测得FeS2的质量分数将会___(填“偏大”“偏小”“不变”)
(5)如何证明II中所加BaCl2溶液已过量(请简要写出操作方法及现象)___。
-
硫酸是一种重要的化工原料,也是实验室中常用的化学试剂。下面是对硫酸的性质、制取、用途等方面的探究,请你共同参与并回答有关问题。
(探究一)硫酸的性质
(1)探究浓硫酸的某些特性。
①用小木棍蘸取少量浓硫酸,放置一会后,可观察到___。
②浓硫酸的稀释:浓硫酸稀释过程如图1所示,b中盛放的物质是___,a的作用是___。
③兴趣小组把98%的浓硫酸10ml和63.3%的硫酸溶液约20mL分别放入两个相同的小烧杯中,称量、观察、记录、分析,根据室温环境下实验的数据绘成的曲线如图2.由图2曲线你能得到的实验结论:_____(写两点)。

(2)探究稀硫酸的化学性质。
如图3将适量的稀硫酸分别加入A~E的五只烧杯中。
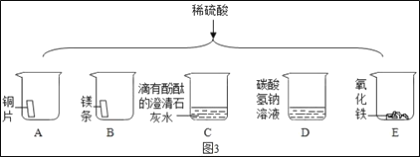
①有产生气泡的是___(填序号,下同);有白色沉淀生成的是___。
②能证明C中发生化学反应的现象是___。
(3)请写出稀硫酸的一种用途___。
(探究二)硫酸的工业制法。
工业上以黄铁矿为原料生产硫酸的工艺流程如图4所示。
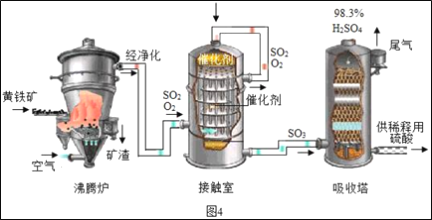
(1)接触室中发生的化学方程式为___。
(2)依据生产硫酸的工艺流程图,下列说法正确的是___(填字母序号)。
A 为使黄铁矿充分燃烧,需将其粉碎 B 催化剂能够提高SO2的反应速率和产量
C 吸收塔中得到的产品为混合物 D 沸腾炉排出的矿渣可供炼铁
(3)接触室中的SO2平衡转化率与温度及压强的关系如图5所示。催化剂活性与温度的关系见图6.在实际生产中,SO2催化氧化反应的条件选择常压和450℃(对应图中A点),而没有选择SO2转化率更高的B或C点对应的反应条件,其原因分别是___;___。
(探究三)探究某黄铁矿中FeS2的含量。
同学们进行了如下实验探究。
(查阅资料)①4FeS2 +11O2  2Fe2O3+8SO2
2Fe2O3+8SO2
②Na2SO3 +H2O2 =Na2SO4 +H2O
(实验探究)
Ⅰ称取1.60g黄铁矿样品放入如图7所示装置(夹持装置省略)的石英管中,从a处不断地缓缓通入空气、高温灼烧石英管中的黄铁矿样品至完全反应。

Ⅱ反应结束后,将乙瓶中的溶液进行如图8处理

(问题讨论)
(1)I中装置甲瓶内盛放的试剂是氢氧化钠溶液,其作用是___;II中滤液所含的溶质一定有___。
(含量测定)
(2)II中最终得到的4.66g固体是___(填化学式)。
(3)计算该黄铁矿中FeS2的质量分数为___。(写出计算过程)
(交流反思)
(4)如果缺少甲装置,则最终测得FeS2的质量分数将会___(填“偏大”“偏小”“不变”)
(5)如何证明II中所加BaCl2溶液已过量(请简要写出操作方法及现象)___。
-
硫酸是一种重要的化工原料,也是实验室中常用的化学试剂。下面是对硫酸的性质、制取、用途等方面的探究,请你共同参与并回答有关问题。
(探究一)硫酸的性质
(1)浓硫酸稀释过程如图1所示,b中盛放的物质是_______。
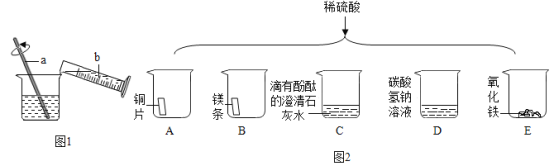
(2)如图2将适量的稀硫酸分别加入A~E五只烧杯中。有气泡产生的是_____,证明C中发生化学反应的现象是__________。
(探究二)硫酸的工业制法
工业上以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程如图所示,其中沸腾炉内发生的主要反应是:4FeS2 +11O2  2Fe2O3 +8SO2 。
2Fe2O3 +8SO2 。
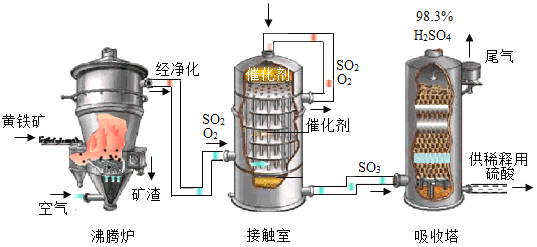
(1)接触室中发生的化学方程式为___________。
(2)依据生产硫酸的工艺流程图,下列说法正确的是_____(填字母序号)。
A 为使黄铁矿充分燃烧,需将其粉碎
B 沸腾炉排出的矿渣可供炼铁
C 催化剂能够提高SO2的反应速率和产量
D 吸收塔中98.3%的硫酸从顶部喷洒,增大接触面积,有利于吸收SO3
(3)接触室中的SO2平衡转化率与温度及压强的关系如图所示,催化剂活性与温度的关系如图所示。在实际生产中,SO2催化氧化反应的条件选择常压和450℃(对应图中A点),而没有选择SO2转化率更高的C点对应的反应条件,其原因是_________。
(探究三)探究某黄铁矿中FeS2的含量。
同学们进行了如下实验探究。
(查阅资料)Na2SO3 +H2O2 =Na2SO4 +H2O
(实验探究)
Ⅰ称取1.60g黄铁矿样品放入如图所示装置(夹持装置省略)的石英管中,从a处不断地缓缓通入空气、高温灼烧石英管中的黄铁矿样品至完全反应(同工业上沸腾炉内的反应)。
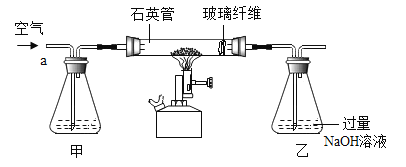
Ⅱ反应结束后,将乙瓶中的溶液进行如图处理。
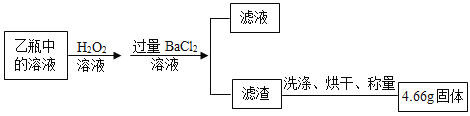
(问题讨论)I中装置甲瓶内盛放的试剂是氢氧化钠溶液,其作用是_____。
(含量测定)计算该黄铁矿中FeS2的质量分数为_____。(写出计算过程)
-
硫酸是一种重要的化工原料,也是实验室中常用的化学试剂,下面是对硫酸的组成、性质、制取、用途等方面的探究,请你共同参与并回答有关问题
探究一、检测硫酸溶液中所含的离子
以下试剂能用来检测硫酸溶液中所含的阴阳离子的组合是____________(填序号)
①石蕊试液 氯化钡溶液 ②PH试纸、硝酸钡溶液 ③石蕊试液 稀盐酸、氯化钡溶液 ④硝酸钡溶液、稀硝酸 ⑤氯化钡溶液稀硝酸
探究二、硫酸的性质
由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异:
(1)探究浓硫酸的某些特征作了如下一些实验:
①用小木棍蘸取少量浓硫酸,放置一会后,可观察到________________
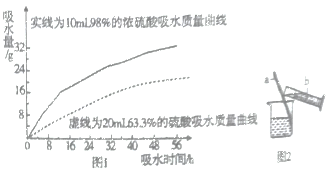
②兴趣小组把98%的浓硫酸10ml和63.3%的硫酸溶液(用10ml98%的浓硫酸与10ml水配成)约20ml分别放入两个相同的小烧杯中,称量、观察、记录、分析;根据室温环境下实验的数据绘成的曲线如图1;
由如图1曲线你能得到的实验结论有哪些?(写两点)_________________________
(2)浓硫酸的稀释;实验室用98%的浓硫酸(密度1.84g/cm3)配制100g溶质质量分数为20%的稀硫酸,需要水的体积为__________ml(精确到0.1);浓硫酸稀释过程如图2所示,b中盛放的物质是__________(填物质名称),a的作用是______________。
(3)探究稀硫酸的化学性质;
如图选择不同类别的物质与稀硫酸反应发生了如下颜色变化;
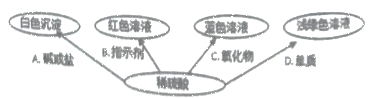
①请在编号C处填一种物质,则C是________________________________(写化学式)
②请写出B体现了稀硫酸的性质是__________________
③请写出符合编号A的一个化学反应方程式__________________
探究三、硫酸的工业制法
工业上黄铁矿为原料生产硫酸的工艺流程如图所示;
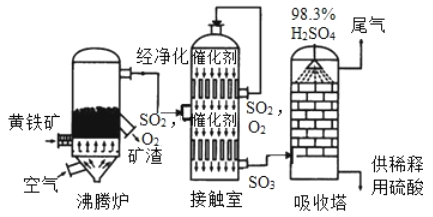
(1)接触室中发生的化学方程式为____________________________________________________ 硫酸是一种重要的化工产品,用途十分广泛,请写出稀硫酸的一种用途_____________________
(2)依据生产硫酸的工艺流程图,下列说法正确的是_____________填字母序号)
为使黄铁矿充分燃烧,需将其粉碎
催化剂能够提高SO2的反应速率和产量
吸收塔中得到的产品为混合物
沸腾炉排除的矿渣可供炼铁
(3)探究某黄铁矿中FeSO2的含量:
同学们进行了如下实验探究(假设每步反应均完全)。
【查阅资料】
①4FeS2+11O2 2Fe2O3+8SO2 ②Na2SO3+H2O2=Na2SO4+H2O
2Fe2O3+8SO2 ②Na2SO3+H2O2=Na2SO4+H2O
【实验探究】
I称取1.60g黄铁矿样品放入如图所示装置(夹持装置省略)的石英管中,从a处不断地缓缓通入空气、高温灼烧石英管中的黄铁矿样品至完全反应。
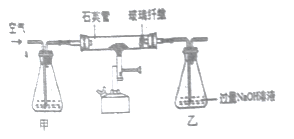
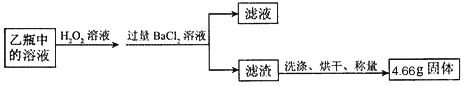
II反应结束后,将乙瓶中的溶液进行如图处理
【问题讨论】
①I中装置甲瓶内盛放的试剂是氢氧化钠溶液,其作用是____________________;II中滤液所含的溶质一定有__________________________________。
【含量测定】
②II中最终得到的4.66g固体是_______填物质的化学式);
③计算该黄铁矿中FeS2的质量分数为______________;
【交流反思】
④如果缺少甲装置,则最终测得FeS2的质量分数将会__________________填“偏大”“偏小”“不变”
⑤如何证明II中所加BaCl2溶液已过量(请简要写出操作方法及现象_________________
-
硫酸是一种重要的化工原料,也是实验室中常用的化学试剂。某兴趣小组对硫酸的性质、制取、用途等方面的探究,请你共同参与并回答有关问题。
(探究一)硫酸的性质
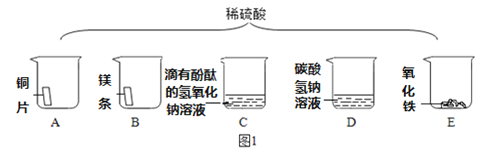
(1)如图1将足量的稀硫酸分别加入A~E五只烧杯中。无现象的是_____________(填序号)。
(2)烧杯C中的现象是红色褪去,反应后溶液中溶质是什么呢?(无色酚酞不考虑)
(猜 想)猜想一:只有Na2SO4 ; 猜想二:有_________________ ;
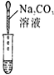
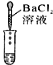
(3)为了验证猜想,小组同学取烧杯中的溶液,并选用老师提供的pH试纸、BaC12溶液、Na2CO3溶液,分别进行如下三组探究实验。
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 
| 
| 
|
| 实验现象 | 试纸变色,比照比色卡,pH<7 | ____________ | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
(得出结论)通过探究,小组同学一致确定猜想二是正确的。
(评价反思)老师指出上述三个实验探究中存在两处明显错误,请大家反思。同学们经过反思发现了这两处错误:
①实验操作中明显的一处错误是_________________________________________;
②实验探究方案中也有一个是不合理的,不合理的原因是____________________________。
(探究二)硫酸的工业制法
工业上以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程如图所示,其中沸腾炉内发生的主
要反应是:
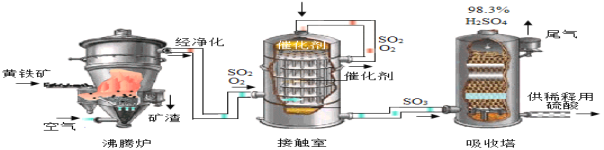
(1)接触室中发生的化学方程式为_________________________________________。
(2)接触室中的SO2平衡转化率与温度及压强的关系如下图所示,催化剂活性与温度的关系如图所示。在实际生产中,SO2催化氧化反应的条件选择常压和450℃(对应图中A点),而没有选择SO2转化率更高的C点对应的反应条件,其原因是___________________________________。
(探究三)探究某黄铁矿中FeS2的含量。
(查阅资料)
(实验探究)Ⅰ称取1.60g黄铁矿样品放入如图所示装置(夹持装置省略)的石英管中,从a处不断地缓缓通入空气、高温灼烧石英管中的黄铁矿样品至完全反应(同工业上沸腾炉内的反应)。
Ⅱ反应结束后,将乙瓶中的溶液进行如下图处理。
(问题讨论)I中装置甲瓶内盛放的试剂是氢氧化钠溶液,其作用是_____________________。
(含量测定)计算该黄铁矿中FeS2的质量分数为_______________。(写出计算过程)
-
硫酸是一种重要的化工原料,也是实验室中常用的化学试剂,下面是对硫酸 的组成、性质、制取等方面的探究,请你共同参与并回答有关问题。
(探究一)硫酸的组成
(1)在溶液中解离出的阳离子全部是氢离子的物质统称为酸,检验硫酸中的阴 离子可选择的试剂为_____。
(探究二)硫酸的性质
(2)浓硫酸的特性:用小木棍蘸取少量浓硫酸,放置一会后,可观察到_____。
(3)浓硫酸的稀释:实验室用 98%的浓硫酸配制 100 g 溶质质量分数为 20%的 稀硫酸,应加水的质量为_____g(结果精确到 0.1 g)。
(4)稀硫酸的化学性质:如图为某同学进行的相关实验:
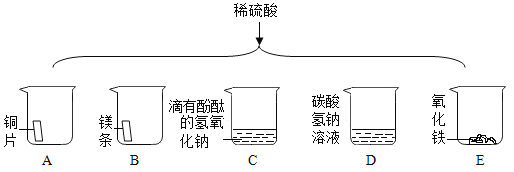
①有气泡产生的是_____(填字母序号)。
②写出烧杯 C 中发生反应的化学方程式_____。
(探究三)硫酸的工业制法
工业上以黄铁矿(主要成分为 FeS2)为原料生产硫酸的工艺流程如图所示:

(5)黄铁矿在加入沸腾炉前要进行粉碎,其目的是_____ 。
(6)接触室中发生反应的化学方程式为_____。
(7)依据生产硫酸的工艺流程图,下列说法中正确的是_____ (填字母序号)。
A 吸收塔中得到的产品为混合物
B 催化剂能够加快 SO2 的反应速率和增大 SO3 的产量
C 沸腾炉排出的矿渣可供炼铁
-
(2011年湖南株洲,29题) H2是一种重要化工生产原料,也是一种极具开发前景的清洁能源。实验室常用锌粒与稀硫酸来制取H2,以便研究H2的性质,下面是—些常见的化学仪器或装置,请按要求填空:

(1)写出上述仪器的名称:b________,f________;
(2)选取上述仪器中的________(填字母代号)组装成制备和收集H2的装置;
(3)为安全起见,在点燃氢气之前,必须进行的操作是________;
(4)此套制备H2的装置________(填“能”或“不能”)制备O2,如果能,请写出用其制备O2反应的化学方程式;如果不能,说明理由:________。
-
(7分)H2是一种重要化工生产原料,也是一种极具开发前景的清洁能源。实验室常用锌粒与稀硫酸来制取H2,以便研究H2的性质,下面是一些常见的化学仪器或装置,请按要求填空:
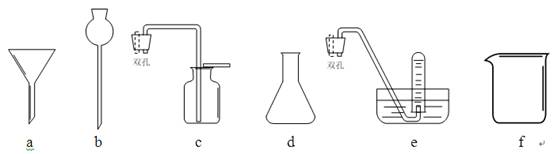
(1)写出上述仪器的名称:b________,f________;
(2)选取上述仪器中的________(填字母代号)组装成制备和收集H2的装置;
(3)为安全起见,在点燃氢气之前,必须进行的操作是________;
(4)此套制备H2的装置________(填 “能”或“不能”)制备O2,如果能,请写出用其制备O2反应的化学方程式;如果不能,说明理由:________。
-
H2是一种重要化工生产原料,也是一种极具开发前景的清洁能源.实验室常用锌粒与稀硫酸来制取H2,以便研究H2的性质.下面是一些常见的化学仪器或装置,请按要求填空.
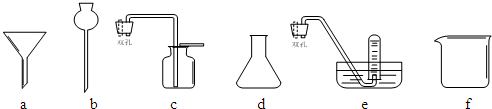
(1)写出上述仪器的名称:b______,f______;
(2)选取上述仪器中的______(填字母代号)组装成制备和收集H2的装置;
(3)为安全起见,在点燃氢气之前,必须进行的操作是______;
(4)此套制备H2的装置______(填“能”或“不能”)制备CO2,其理由是:______.
-
H2是一种重要化工生产原料,也是一种极具开发前景的清洁能源.实验室常用锌粒与稀硫酸来制取H2,以便研究H2的性质,下面是一些常见的化学仪器或装置,请按要求填空:

(1)写出上述仪器的名称:b______,f______;
(2)选取上述仪器中的______(填字母代号)组装成制备和收集H2的装置;
(3)为安全起见,在点燃氢气之前,必须进行的操作是______;
(4)此套制备H2的装置______(填“能”或“不能”)制备O2,如果能,请写出用其制备O2反应的化学方程式______ 2H2O+O2↑