氢气作为新能源的优点有_____(写一点),低成本制取氢气是目前研究的热点。利用铁酸锌(ZnFe2O4)循环制氢的反应可表示为:①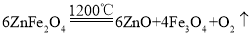 ;②
;②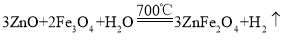 。请回答:
。请回答:
(1)该循环制氢的过程中需要不断补充的物质是_____(填化学式)。
(2)你认为该循环法制氢的不足之处是_____。
九年级化学填空题简单题
氢气作为新能源的优点有_____(写一点),低成本制取氢气是目前研究的热点。利用铁酸锌(ZnFe2O4)循环制氢的反应可表示为:①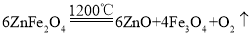 ;②
;②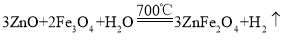 。请回答:
。请回答:
(1)该循环制氢的过程中需要不断补充的物质是_____(填化学式)。
(2)你认为该循环法制氢的不足之处是_____。
九年级化学填空题简单题
氢气作为新能源的优点有_____(写一点),低成本制取氢气是目前研究的热点。利用铁酸锌(ZnFe2O4)循环制氢的反应可表示为:①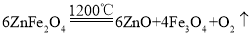 ;②
;②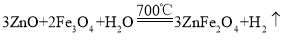 。请回答:
。请回答:
(1)该循环制氢的过程中需要不断补充的物质是_____(填化学式)。
(2)你认为该循环法制氢的不足之处是_____。
九年级化学填空题简单题查看答案及解析
氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
制氢:铁酸锌( ZnFe2O4)可用于循环分解水制氢,其反应可表示为:
;
(1) ZnFe2O4中Fe的化合价为_____。
(2)该循环制氢的过程中,不断被消耗的物质是_____(填化学式)。
(3)氢气作为新能源的优点有_____(任写一点),该循环法制氢的不足之处是_____。
(4)下列说法正确的是_____(填序号)。
A 能源结构向多元、清洁、低碳转型
B 科技进步会促进能源的利用
C 石油和太阳能属于可再生能源
D 生活中的废热可转化为电能
九年级化学填空题简单题查看答案及解析
氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
Ⅰ.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为:6ZnFe2O46ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
3ZnFe2O4+H2↑
(1)ZnFe2O4中Fe的化合价为_____。
(2)该循环制氢中不断消耗的物质是_____(填化学式),得到H2和O2的质量比为_____。
Ⅱ.贮氢:合金Mg2Cu是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得。该合金在一定条件下完全吸氢生成氢化物和另一种合金,其化学方程式为:2Mg2Cu+3H23MgH2+MgCu2。
(1)熔炼制备Mg2Cu合金时,通入氩气的目的是_____。
(2)氢化物MgH2与水反应生成一种碱,并释放出H2。其化学反应方程式为_____。
(3)11.2gMg2Cu完全吸氢后所得混合物与过量盐酸反应,放出H2的质量为_____g。
九年级化学综合题困难题查看答案及解析
氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
Ⅰ.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为:6ZnFe2O46ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
3ZnFe2O4+H2↑
(1)ZnFe2O4中Fe的化合价为_____。
(2)该循环制氢中不断消耗的物质是_____(填化学式),得到H2和O2的质量比为_____。
Ⅱ.贮氢:合金Mg2Cu是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得。该合金在一定条件下完全吸氢生成氢化物和另一种合金,其化学方程式为:2Mg2Cu+3H23MgH2+MgCu2。
(1)熔炼制备Mg2Cu合金时,通入氩气的目的是_____。
(2)氢化物MgH2与水反应生成一种碱,并释放出H2。其化学反应方程式为_____。
(3)11.2gMg2Cu完全吸氢后所得混合物与过量盐酸反应,放出H2的质量为_____g。
九年级化学综合题困难题查看答案及解析
氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为: 6ZnFe2O46ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
3ZnFe2O4+H2↑
(1)ZnFe2O4中Fe的化合价为_______________。
(2)该循环制氢中不断消耗的物质是________(填化学式),得到H2和O2的质量比为__________。
(3)氢气作为新能源的优点有________(任写一点)。该循环法制氢的不足之处是________。
Ⅱ.贮氢:合金Mg2Cu是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得。该合金在一定条件下完全吸氢生成氢化物和另一种合金,其化学方程式为: 2Mg2Cu+ 3H23MgH2+MgCu2
(4)熔炼制备Mg2Cu合金时,通入氩气的目的是_________________。
(5)氢化物MgH2与水反应生成一种碱,并释放出H2。 其化学反应方程式为________。
(6)11.2g Mg2Cu完全吸氢后所得混合物与过量盐酸反应,放出H2的质量为________g。
九年级化学综合题困难题查看答案及解析
氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为: 6ZnFe2O46ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
3ZnFe2O4+H2↑
(1)ZnFe2O4中Fe的化合价为_______________。
(2)该循环制氢中不断消耗的物质是________(填化学式),得到H2和O2的质量比为__________。
(3)氢气作为新能源的优点有________(任写一点)。该循环法制氢的不足之处是________。
Ⅱ.贮氢:合金Mg2Cu是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得。该合金在一定条件下完全吸氢生成氢化物和另一种合金,其化学方程式为: 2Mg2Cu+ 3H23MgH2+MgCu2
(4)熔炼制备Mg2Cu合金时,通入氩气的目的是_________________。
(5)氢化物MgH2与水反应生成一种碱,并释放出H2。 其化学反应方程式为________。
(6)11.2g Mg2Cu完全吸氢后所得混合物与过量盐酸反应,放出H2的质量为________g。
九年级化学综合题困难题查看答案及解析
氢气作为新能源有很多优点,制取不储存氢气是氢能源利用领域的研究热点。
I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为:
6Zn+Fe2O46ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
3ZnFe2O4+H2↑
(1)ZnFe2O4 中 Fe 的化合价为____。
(2)该循环制氢中不断消耗的物质是____(填化学式),得到H2和O2 的质量比为____。
(3)氢气作为新能源的优点有____(任写一点)。该循环法制氢的不足之处是____。
Ⅱ.贮氢:合金 Mg2Cu 是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu 单质熔炼获得。该合金在一定条件下完全吸氢生成氢化物和另一种合金,其化学 方程式为: 2Mg2Cu+ 3H23MgH2+MgCu2
(4)熔炼制备 Mg2Cu 合金时,通入氩气的目的是____。
(5)氢化物 MgH2 不水反应生成一种碱,并释放出 H2。 其化学反应方程式为____。
九年级化学简答题简单题查看答案及解析
氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
Ⅰ.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为:
3ZnO + 2Fe3O4 + H2O3ZnFe2O4 + H2↑;6ZnFe2O4
6ZnO + 4Fe3O4 + O2↑
(1)ZnFe2O4中Fe的化合价为________。
(2)该循环制氢中不断消耗的物质是_______(填化学式)。
Ⅱ.贮氢:合金Mg2Cu是一种贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得。该合金在一定条件下完全吸氢生成氢化物和另一种合金,其化学方程式为:2Mg2Cu + 3H2 3MgH2 + MgCu2
(3)熔炼制备Mg2Cu合金时,通入氩气的目的是_______。
(4)氢化物MgH2中氢元素的质量分数为______(精确到0.1% )。
九年级化学计算题简单题查看答案及解析
氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。铁酸锌(ZnFe2O4)可用于循环分解水制取氢气,下列关于铁酸锌的说法正确的是()
A. 含有2个氧分子
B. 由两种金属和一种非金属组成
C. 铁元素的化合价为+3
D. Zn、Fe、O三种元素的质量比为1:2:4
九年级化学单选题简单题查看答案及解析
氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
Ⅰ.制氢:铁酸锌()可用于循环分解水制气,其反应可表示为:
;
(1)中
的化合价为_____。
(2)该循环制氢中不断消耗的物质是_____(填化学式),得到和
的质量比为_____.
(3)氢气作为新能源的优点有_____(任写一点)该循环法制氢的不足之处是_____.
Ⅱ.贮氢:合金是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的
单质熔炼获得。该合金在一定条件下完全吸氢生成氢化物和另一种合金,其化学方程式为:
(4)熔炼制备合金时,通入氩气的目的是_____。
(5)氢化物与水反应生成一种碱,并释放出
其化学反应方程式为_____。
九年级化学简答题中等难度题查看答案及解析