-
为测定二氧化碳与氢氧化钠反应的产物,某化学学习小组的同学向一定量的NaOH溶液中通入一定量的CO2充分反应后,低温蒸发结晶,得到白色固体,对该白色固体的成分.
[资料卡]当二氧化碳过量时,碳酸钠也会与二氧化碳反应Na2CO3+CO2+H2O=2NaHCO3
Na2CO3+HCl=NaHCO3+NaCl; NaHCO3+HCl=NaCl+H2O+CO2↑;
NaHCO3+NaOH=Na2CO3+H2O; 2NaHCO3 Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
Na2CO3和NaOH的热稳定性都较好.
[猜想与假设]该小组的同学进行了猜测:
(1)甲同学认为该白色固体可能是NaOH与Na2CO3的混合物.你认为该固体还可能是Na2CO3或______或______.
[实验设计]
(2)
| 实验操作 | 实验现象 | 结论 |
| (1)取一定质量的样品,加热 | 固体质量减少 | 一定有______
一定无______
可能有______ |
| (2)另取样品,向其中滴加稀盐酸 | 有气体产生 |
-
某学习小组的同学向100g8%的NaOH溶液中通入CO2一段时间后,低温蒸发结晶,得到白色固体,该小组的同学决定对白色固体进行探究.
【提出问题】白色粉末中有哪些成分
【收集资料】CO2+2NaOH═Na2CO3+H2O,CO2+Na2CO3+H2O═2NaHCO3
【提出猜想】猜想一:白色固体可能是NaOH与Na2CO3的混合物,
猜想二:白色固体可能是Na2CO3和______.猜想三:白色固体可能是NaHCO3.
(2)如果猜想一的结论是正确的,请你设计实验证明白色固体中存在NaOH,请将方案填入下表中
(3)乙同学称量所得白色固体的质量为13.7g,则白色固体的成分是______.
-
某学习小组的同学向100g8%的NaOH的溶液中通入CO2一段时间后,低温蒸发结晶,得到白色固体,对该白色固体成分,该小组的同学进行了猜测:
(1)甲同学认为该白色固体可能是NaOH与Na2CO3的混合物.你认为该固体还可能是______或______或______.
(2)如果甲同学的结论是正确的,请你设计实验证明白色固体中存在NaOH,请将方案填入下表中:
(3)乙同学称量所得白色固体的质量为13.7g则白色固体的成分是______.
-
化学兴趣小组的同学在探究CO2通入 NaOH溶液是否发生了反应,设计了下列两组实验。请你和同学一起探究井回答问题:
(设计与实验)
| 步骤一 | 步骤二 |
| 实验Ⅰ | 往氢氧化钠溶液中通入CO2 | 往步骤一所得溶液中滴加足量稀盐酸 |
| 实验Ⅱ | 往氢氧化钠溶液中通入CO2 | 往步骤一所得溶液中滴加CaCl2溶液 |
(探究与结论)
(1)实验I中步骤一看不到明显的现象,步骤二产生的现象是_____,说明CO2与NaOH发生了反应,请写出步骤二产生上述现象对应的化学方程式_____。
(2)实验Ⅱ中步骤二看到有白色沉淀析出,反应原理可以用字母表示:AB+CD=AD+CB,则该反应的化学方程式为_____。
(拓展延伸)表格中给出了20℃时NaOH和Na2CO3在乙醇中的溶解度。
| 物质 | 溶解度(s)/g |
| NaOH | 17.3 |
| Na2CO3 | <0.01 |
根据表格,可以设计实验Ⅲ,操作为:将CO2通入NaOH的乙醇饱和溶液中,看到的现象是_____,证明CO2与NaOH发生了反应。
(反思)检验二氧化碳不用氢氧化钠溶液,而用澄清石灰水的原因_____。
-
实验中学某化学兴趣小组,用氢氧化钠(NaOH)吸收二氧化硫的方法,通过计算测定县城空气中二氧化硫的含量,反应的化学方程式为2NaOH+SO2═NaSO3+H2O.现用足量的氢氧化钠溶液充分吸收1000L空气中的二氧化硫(假设该空气中的其它成分与氢氧化钠溶液不反应,也不会引起溶液增重),发现氢氧化钠溶液增重0.64g.若该空气的平均密度为1.28g/L,试计算:
(1)参加反应的氢氧化钠的质量.
(2)该空气中二氧化硫的质量分数.
-
该小组同学将一定量CO2分别通入澄清石灰水和氢氧化钠溶液中(如图所示),他们观察到前者变浑浊,后者无明显现象。

猜想:CO2和NaOH是否发生了化学反应?
实验:设计了甲、乙两个实验来验证CO2与NaOH发生了化学反应,如图所示。甲中现象为软塑料瓶变瘪,乙中现象“瓶吞鸡蛋”。

讨论:认为上述实验是可行的,其共同原理是____。但是有同学提出质疑,认为上述实验还不足以说明CO2和NaOH发生了反应。其理由是___。于是他们又补充了一个对照实验,这个实验是___;他们还发现将二氧化碳通入紫色石蕊溶液中,石蕊溶液变成红色,请用化学方程式说明原因_____。
-
为测定某赤铁矿石中氧化铁的质量分数,某化学兴趣小组的同学用过量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用100g氢氧化钠溶液恰好完全吸收,形成不饱和溶液.该溶液总质量与反应时间的变化关系如图.试分析解答:
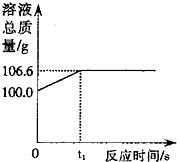
(1)赤铁矿石中所含主要物质的颜色为: ________ .
(2)实验中多余的一氧化碳能否用水吸收? ________ .
(3)上述反应中产生二氧化碳的质量为 ________ g.
(4)计算实验结束后所得不饱和溶液中所含溶质的质量.
-
为测定某赤铁矿石中氧化铁的质量分数,某化学兴趣小组的同学用过量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用100g氢氧化钠溶液恰好完全吸收,形成不饱和溶液.该溶液总质量与反应时间的变化关系如图.试分析解答:
(1)赤铁矿石中所含主要物质的颜色为:______.
(2)实验中多余的一氧化碳能否用水吸收?______.
(3)上述反应中产生二氧化碳的质量为______g.
(4)计算实验结束后所得不饱和溶液中所含溶质的质量.

-
(8分)某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下充分反应生成CO2来进行分析测定。

(1)仪器①的名称是 。如果该实验选择图(一)装置来制取氧气,该反应的化学方程式为 。
(2)用图(二)装置可用于收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从 (填“a”或“b”,下同)端通入;若在烧瓶内装入浓硫酸进行干燥气体,气体应从 端通入。
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰(生石灰与固体氢氧化钠的混合物),其作用是防止空气中 进入②中(填写化学式)。
(4)为验证图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为 (填字母)。
A.NaOH溶液 B.澄清石灰水 C.浓硫酸
(5)称取5.0g二氧化锰样品进行实验,图(三)中装置②反应前后的质量差为1.1g,则样品中二氧化锰的质量分数为 (填计算结果)。
-
碳酸氢钠是化学实验中常见的药品,在工业上有很多制取方法。重庆一中兴趣小组的同学 们查询资料发现了一种“气相固碳法”:向氢氧化钠溶液中通入过量的CO2气体。
整理资料:Ⅰ、过量CO2通入NaOH溶液,发生两步反应:
①_________________________________(写出化学方程式);
②Na2CO3 +H2O + CO2=2NaHCO3
Ⅱ、碳酸钠和碳酸氢钠的溶解度表(部分)
| 温度/℃ | 0 | 15 | 20 | 30 |
| Na2CO3 溶解度/g | 7.1 | 13.25 | 21.8 | 39.7 |
| NaHCO3 溶解度/g | 6.9 | 8.72 | 9.6 | 11.1 |
15℃时,将10g氢氧化钠固体完全溶解溶于100g水中(如图1),而后匀速的通入二氧化碳气体,同时用pH计测定溶液的pH值变化(如图2)。

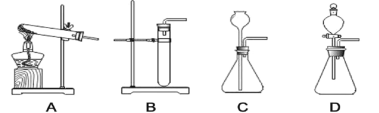
(1)图 1 所示实验中,产生 CO2 的装置应该选择:_____(填序号);
(2)为了确定M处溶液的溶质成分,取少量样品于试管中,进行如下实验:
| 步骤 | 加入试剂 | 实验现象 | 实验结论 |
| ① | 加入_______溶液 | 溶液变红 | NaOH和Na2CO3 |
| ② | 加入过量_______溶液 | ______ |
(3)实验中,t2后溶液的pH基本不变,则此时烧杯中观察到的现象是_____。






