-
(11分)实验设计中常通过放大、转化等方式使化学反应现象显现出来,从而达到实验目的。
【问题提出】怎样证明NaOH溶液与稀盐酸能发生化学反应?
【查阅资料】根据化学反应的本质:有新物质生成。可从两个方面设计实验证明:一是设计实验证明反应物的消失;二是设计实验证明有新物质生成。
【实验探究】方案一:在NaOH溶液中滴入几滴酚酞后再滴加盐酸,当观察到 时,即可确定二者发生了化学反应。其中和反应方程式为 。
方案二:在NaOH溶液滴加盐酸的过程中,用pH试纸不断测量溶液的酸碱度,当pH <7即可确定二者发生了化学反应。实验测得其图象如下图。
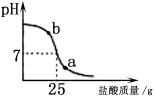
(1)测定pH的操作方法为 。
(2) b点表示溶液中的溶质是
(3)强调“pH <7时”作为判断的理由是
方案三:NaOH溶液与稀盐酸反应放热,若混合前后温度有变化,则证明发生了化学反应。某同学将不同溶质质量分数的盐酸和NaOH溶液各10 mL混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如表1)
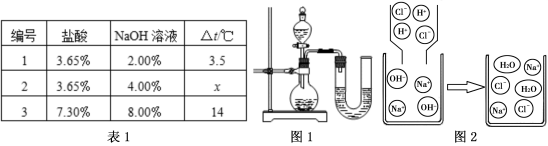
(1)表中x约为 。
(2)某同学在没使用温度计的情况下,通过图1所示装置完成了实验。则该同学根据 判断NaOH溶液与稀盐酸发生了中和反应。但有同学认为单凭此现象不足以说明该反应放热,其理由是 。
(3)对上述过程采用微观模型加以认识,如图2:当滴加盐酸过程中,氢氧化钠溶液中减少的离子是 (填离子符号)。
【拓展应用】下列几个方案中一定能证明CO2与NaOH溶液反应的是 。
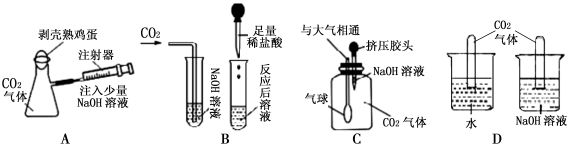
-
实验小组的同学将CO2通入氢氧化钠溶液时,没有观察到明显现象。为了能通过实验现象证明二氧化碳与氢氧化钠确实发生了反应,进行了以下探究。
(提出问题)如何能观察到反应的变化过程?
(查阅资料)
NaOH、Na2CO3在水中的溶解度
| 温度/℃ | 0 | 10 | 20 | 30 |
| NaOH | 42 | 51 | 109 | 119 |
| Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
NaOH、Na2CO3在乙醇中的溶解度
| 温度/℃ | NaOH | Na2CO3 |
| 18.5~25 | 17.3 | 不溶 |
(进行实验)注:乙醇在实验中只作为溶剂,不参与化学反应。
| 实验 | 实验装置 | 实验操作 | 实验现象 |
| 1 | 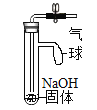
| 打开止水夹,通入 CO2,气球明显鼓起后关闭止水夹 | 一段时间后,气球明显变瘪 |
| 2 | 
| 室温下,向10mL澄清饱和的NaOH溶液中通入适量CO2 | 试管内壁出现白色固体 |
| 3 | 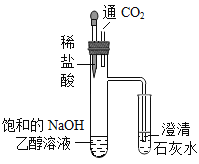
| ① 室温下,向10mL饱和的NaOH乙醇溶液中缓慢通入适量CO2 | 甲中出现白色沉淀,乙中无明显现象 |
| ② 滴入稀盐酸 | 甲中有气泡生成,乙中澄清石灰水变浑浊 |
(解释与结论)
(1)二氧化碳与氢氧化钠反应的化学方程式为_______。
(2)实验1中,气球明显变瘪的原因是_______。
(3)实验2中,试管内壁上出现白色固体的原因是_______。
(4)实验3甲中出现白色沉淀的原因是_______。
(5)实验3中操作②的目的是_______。
(反思与评价)
(6)实验1是从________(填“反应物消耗”或“新物质生成”)角度证明化学反应发生。
-
(8分)NaOH能与CO2发生化学反应,其反应的化学方程式为________。然而,在化学课上老师向NaOH溶液通入CO2后无明显现象。提出问题:如何通过实验证明CO2与NaOH发生了反应。
【查阅资料】
①CaCl2溶液可与Na2CO3溶液发生复分解反应。
②向CaCl2溶液中通入CO2,无明显现象;在水溶液中CaCl2不与CO2、H2CO3等物质反应。
【实验一】证明反应物之一CO2消失了
(1)同学门设计了如图所示的实验,打开分液漏斗活塞。向充满CO2的广口瓶中滴入NaOH溶液。一会儿后可观察到的实验现象是___________________。并据此现象判断NaOH与CO2发生了化学反应。

(2)老师提出上述实验不足以证明NaOH与CO2发生了化学反应。其理由是____________________。据此,你认为上述实验应做的改进是_____________________ 。
【实验二】证明有新物质Na2CO3生成
同学们经过思考、讨论,分别设计了以下两个实验方案:
方案一:打开瓶塞,向实验一所得的溶液中加入饱和的石灰水,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
 方案二:打开瓶塞,向实验一所得的溶液中加入CaCl2溶液,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
方案二:打开瓶塞,向实验一所得的溶液中加入CaCl2溶液,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
(1)写出方案二发生反应的化学方程式:___________________________。
(2)你认为上述实验方案不可行的是________,理由是______________________________。
-
在化学课上老师向NaOH溶液通入CO2后无明显现象。提出问题:如何通过实验证明CO2与NaOH发生了反应。
【查阅资料】
①CaCl2溶液可与Na2CO3溶液发生复分解反应。
②向CaCl2溶液中通入CO2,无明显现象;在水溶液中CaCl2不与CO2、H2CO3等物质反应。
【实验一】证明反应物之一CO2消失了
(1)同学门设计了如图所示的实验,打开分液漏斗活塞。向充满CO2的广口瓶中滴入NaOH溶液。一会儿后可观察到的实验现象是___________________。并据此现象判断NaOH与CO2发生了化学反应。

(2)老师提出上述实验不足以证明NaOH与CO2发生了化学反应。其理由是____________________。据此,你认为上述实验应做的改进是_____________________ 。
【实验二】证明有新物质Na2CO3生成
同学们经过思考、讨论,分别设计了以下两个实验方案:
方案一:打开瓶塞,向实验一所得的溶液中加入饱和的石灰水,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
方案二:打开瓶塞,向实验一所得的溶液中加入CaCl2溶液,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
(1)写出方案二发生反应的化学方程式:___________________。
(2)你认为上述实验方案不可行的是________,理由是__________________。
-
实验是学习化学的重要手段。下列实验设计不能达到实验目的的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 确定NaOH溶液是否变质 | 滴加澄清石灰水观察现象 |
| B | 区别稀盐酸和稀硫酸 | 滴加氯化钡溶液观察现象 |
| C | 除去MnO2粉末中的KCl杂质 | 溶解、过滤、洗涤、干燥 |
| D | 检验Na2CO3溶液中是否含有NaCl杂质 | 滴加稀盐酸观察现象 |
-
实验是学习化学的重要手段。下列实验设计不能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 确定NaOH溶液是否变质 | 滴加澄清石灰水观察现象 |
| B | 区别稀盐酸和稀硫酸 | 滴加氯化钡溶液观察现象 |
| C | 除去MnO2粉末中的KCl杂质 | 溶解、过滤、洗涤、干燥 |
| D | 检验Na2CO3溶液中是否含有NaCl杂质 | 滴加稀盐酸观察现象 |
-
下列实验操作不能达到实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别 H2SO4 溶液和 NaOH 溶液 | 取样,滴加酚酞溶液,观察现象 |
| B | 证明氢氧化钠溶液与稀盐酸能反应 | 取氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,振荡,再滴入稀盐酸至溶液变为无色 |
| C | 除去CaCl2溶液中的少量盐酸 | 加入适量的铁粉 |
| D | 除去CO中含有的少量CO2 | 通入氢氧化钠溶液中,再通过浓硫酸干燥 |
A.A B.B C.C D.D
-
分离、除杂、提纯和检验是化学实验的重要环节。下面实验设计能够达到目的的是
| 实验内容 | 实验设计 |
| A | 除去H2中少量水蒸气、HCl | 先通过浓H2SO4,再通过NaOH溶液 |
| B | 提纯久置变质的NaOH溶液 | 加入足量CaCl2溶液,充分反应后,过滤 |
| C | 验证某溶液为稀盐酸 | 先测溶液的pH﹤7,再加入锌粒 |
| D | 分离CO2、CO混合物 | 先用NaOH溶液吸收掉CO2分离出CO,再向该NaOH溶液加足量稀盐酸“释放”出CO2 |
-
分离、除杂、提纯和检验是化学实验的重要环节。下面实验设计能够达到目的的是
实验内容 实验设计
A 除去H2中少量水蒸气、HCl 先通过浓H2SO4,再通过NaOH溶液
B 提纯久置变质的NaOH溶液 加入足量CaCl2溶液,充分反应后,过滤
C 验证某溶液为稀盐酸 先测溶液的pH﹤7,再加入锌粒
D 分离CO2、CO混合物 先用NaOH溶液吸收掉CO2分离出CO,再向该NaOH溶液加足量稀盐酸“释放”出CO2
-
分离、除杂、提纯和检验是化学实验的重要环节。下面实验设计能够达到目的的是( )
| 实验内容 | 实验设计 |
| A | 除去H2中少量水蒸气、HCl | 先通过浓H2SO4,再通过NaOH溶液 |
| B | 提纯久置变质的NaOH溶液 | 加入足量CaCl2溶液,充分反应后,过滤 |
| C | 验证某溶液为稀盐酸 | 先测溶液的pH﹤7,再加入锌粒,观察 |
| D | 分离CO2、CO混合物 | 先用NaOH溶液吸收掉CO2分离出CO,再向该NaOH溶液加足量稀硫酸“释放”出CO2 |
A.A B.B C.C D.D






