A.CaCO3和Mg(OH)2难溶于水
B.Ca(HCO3)2和Mg(HCO3)2能溶于水
C.经煮沸发生的反应属于分解反应
D.CaCO3和Mg(OH)2受热能分解
九年级化学选择题中等难度题
九年级化学选择题中等难度题
九年级化学选择题中等难度题查看答案及解析
某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分。
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是 。
Ⅰ.CaO Ⅱ.Ca(OH)2 Ⅲ.CaCO3 Ⅲ.Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是 。
【实验与事实】
| 实验 | 现象 | 解释或结论 | |
| 实验一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | Ca(OH)2微溶于水,其水溶液显碱性,能使紫色石蕊溶液变蓝色,不 变色说明水垢中一定没有 |
| 实验二 | 按如图所示方案进行实验
| 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 石灰水变浑浊,说明有CO2生成, 则水垢中一定含有 |
【原理与呈现】请用化学方程式表示实验二中有关反应的化学反应原理: , 。
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用 来检测饮用水是硬水还是软水。
九年级化学探究题困难题查看答案及解析
某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分。
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是 。
Ⅰ.CaO Ⅱ.Ca(OH)2 Ⅲ.CaCO3 Ⅲ.Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是 。
【实验与事实】
| 实验 | 现象 | 解释或结论 | |
| 实验一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | Ca(OH)2微溶于水,其水溶液显碱性,能使紫色石蕊溶液变蓝色,不 变色说明水垢中一定没有 |
| 实验二 | 按如图所示方案进行实验
| 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 石灰水变浑浊,说明有CO2生成, 则水垢中一定含有 |
【原理与呈现】请用化学方程式表示实验二中有关反应的化学反应原理: , 。
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用 来检测饮用水是硬水还是软水。
九年级化学探究题困难题查看答案及解析
“硬水”是指含有较多可溶性钙镁化合物的水,硬水会给生产、生活带来许多不便。
(1)生活中常用______方法降低水的硬度,此过程中发生的化学反应之一是:碳酸氢钙[Ca(HCO3)2]受热分解生成碳酸钙、二氧化碳和水,写出该反应的表达式为___,该反应属于______反应(填“分解”或“化合”)。所以长期烧水的水壶内会有水垢,水垢中常含有碳酸钙、硫酸镁(MgSO4)等。
(2)试根据硫酸镁的化学式计算:
①相对分子质量_______;
②各元素的质量比 (请写出计算过程,下同)_______;
③240g硫酸镁中含镁元素的质量_______。
九年级化学计算题中等难度题查看答案及解析
浴室喷头长时间使用会有白色固体附着,俗称水垢。这是因为硬水中含有较多的可溶性的碳酸氢钙【Ca(HCO3)2】,还含有可溶性的碳酸氢镁【Mg(HCO3)2】。查阅资料,加热时会产生难溶性的固体。其中碳酸氢钙【Ca(HCO3)2】受热易分解,生成难溶性的化合物、气体等物质。某小组想探究碳酸氢钙受热分解后产物的成分。
【提出猜想】猜想1.难溶性化合物可能是CaCO3;猜想2.气体可能是H2、CO、CO2 。
【方案设计】请你设计实验,帮助该组同学确定难溶物的成分。
| 实验步骤 | 实验现象 | 结论 |
| _____ | _______ | 难溶物是CaCO3 |
【实验探究】该组同学设计如图实验,继续探究气体的成分。
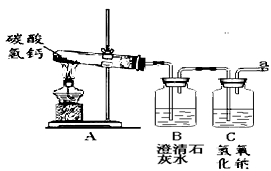
操作1.加热A装置,一段时间后,B装置中的澄清石灰水变浑浊。
操作2.在a处用燃着的木条检验,无明显现象。
【实验结论】结论1.碳酸氢钙分解产生的气体是____________;
结论2.碳酸氢钙受热分解的化学方程式为_____________________________。
【反思评价】有同学提出:硬水中可溶性的碳酸氢镁【Mg(HCO3)2】受热也会产生不溶性的固体,那水垢的成分中还有什么物质?根据上述探究,该组同学设计如下图装置进一步实验。(已知碱石灰主要成分为CaO和NaOH)
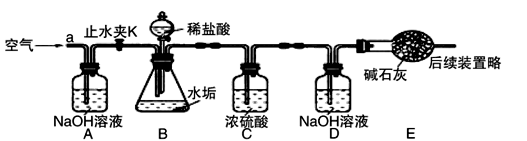
【实验测定】 步骤如下:
①按图组装仪器,先_____________,再将50g水垢样品放入锥形瓶中。
②打开止水夹K,从导管a处缓缓鼓入一定量的空气。
③逐滴加入足量稀盐酸,待锥形瓶中出现气泡不再产生现象时,停止滴加稀盐酸。
④打开止水夹K,从导管a处缓缓鼓入一定量的空气;
⑤称量D瓶内物质增加的质量,直至D瓶内物质质量不变;
⑥测量滴加稀盐酸体积与D瓶内物质增加质量的关系如下图曲线所示。
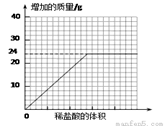
【讨论交流】
①A装置中的NaOH溶液的作用是____________________,若没有A装置,D装置中的质量将_______________(填“偏大”、“不变”或“偏小”)。
②C装置中浓硫酸的作用是__________________,E装置的作用是____________________。
③分析曲线图,通过计算可知:水垢中一定含有(化学式)________,理由是________________。
④查阅资料:水垢的主要成分有CaCO3、MgCO3和Mg(OH)2三种成分,三种物质加热后均能生成两种氧化物。小组同学提出探究水垢中氢氧化镁的质量分数:另取质量为50g的水垢试样,放入试管中加热至质量不再减少为止,测得二氧化碳24 g,残留固体25.1g。结合以上数据,确定水垢样品中氢氧化镁的质量分数为_______________。(结果保留小数点后一位)
九年级化学探究题极难题查看答案及解析
兴趣小组的同学通过实验探究热水壶底部水垢的主要成分。
(提出问题)硬水煮沸后的白色固体(水垢)中含有什么物质?
(查阅资料)
Ⅰ.硬水中含有一定量的 Ca(HCO3)2 和 Mg(HCO3)2,加热时趋于生成溶解度更小的物质。 有关物质的溶解性:
| 物 质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
Ⅱ. Mg(OH)2 和 MgCO3 受热分解均分别生成对应的两种氧化物。
(猜想)水垢的主要成分一定含有不溶的Mg(OH)2 和________,可能含有微溶的Ca(OH)2和______。
(实验)
(1)初步探究白色固体成分
①甲同学取白色固体少许,加入适量水充分溶解,在上层清液中滴加________溶液(选 填序号),没有白色沉淀生成,说明水垢中无 Ca(OH)2;
A 碳酸钠 B 氯化钾 C 碳酸钾
②另取白色固体加入稀盐酸,观察到有气泡产生,甲同学认为还含有 MgCO3,其他同学否定了他的结论,理由是__________。
③已知Ca(HCO3)2 受热分解与碳酸氢钠受热分解类似,请写出Ca(HCO3)2 受热分解的化学方程式___________________。
(2)为进一步确定白色固体的成分,乙同学称取 20g 白色固体,设计如下实验:
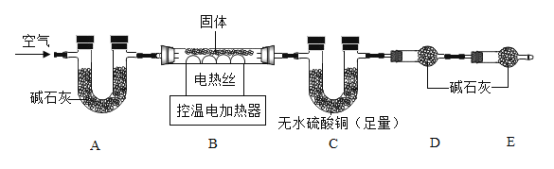
碱石灰的主要成分是固体 CaO 和 NaOH 的混合物。
①反应前,先通一段时间的空气,目的是______________。
②实验中 E 装置的作用是____________________。
③充分反应后,测得 C 增重 1.8g,D 中增重 6.6g。20g 白色固体中 Mg(OH)2 的质量是___________________g。
(结论)该白色固体中氢氧化镁与碳酸钙的质量比为_________。
九年级化学综合题困难题查看答案及解析
硬水中含有一定量的Ca(HCO3)2和Mg(HCO3)2,某兴趣小组的同学将一定量的硬水煮沸后出现白色固体,该小组的同学探究其成分。
查阅资料:已知可溶性的Ca(HCO3)2加热会分解,出现白色沉淀和能使澄清石灰水变浑浊的气体,分解的化学方程式为_________
【提出问题】硬水煮沸后的白色固体中还含有什么物质?
【猜想】 甲:MgCO3; 乙:Mg(OH)2; 丙:MgO
【实验】
(1)甲同学取白色固体,加入适量的稀盐酸,观察到有气泡产生,认为自己的猜想正确,其他同学否定了他的结论,理由是_______
(2)乙同学称取10.8g白色固体,设计如下实验确定固体组成:
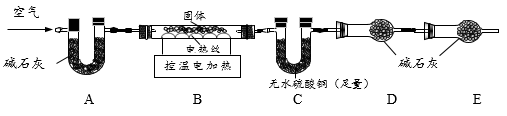
①反应前,先通一段时间的空气,目的是_____________。
②加热一段时间后,装置C中可观察到_______(填实验现象),证明乙同学的猜想成立。
③实验中E装置的作用是___________________。
④充分反应后,测得C增重1.8g,D中增重4.4g。
【结论】(1)白色固体中各成分的质量比为______。
(2)写出Mg(HCO3)2受热分解的化学方程式_____________。
九年级化学信息分析题困难题查看答案及解析
九年级化学填空题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
取只含碳酸氢钙的硬水a g,充分加热,发生如下反应:Ca(HCO3)2CaCO3↓+CO2↑+H2O,得到沉淀1.0g.回答下列问题:
(1)碳酸氢钙中钙元素与氧元素的质量比为_____.
(2)计算此硬水中碳酸氢钙的质量是多少_____?
九年级化学计算题中等难度题查看答案及解析