-
高粱、玉米和薯类等经过发酵、蒸馏,可得到乙醇,乙醇属于可再生能源。乙醇的化学式为〔C2H5OH〕,请你计算:
(1)乙醇的相对分子质量 ;
(2)乙醇中碳、氢、氧三种元素的质量比 ;(最简整数比)
(3) 克的乙醇中含有3克氢元素;
(4)5.4克的水与 克乙醇含有相等质量的氢元素。
九年级化学计算题中等难度题查看答案及解析
-
我国的一些地区正在逐步推广使用乙醇汽油.下列说法不正确的是( )
A.乙醇汽油是一种新型化合物
B.乙醇属于可再生能源
C.高粱、玉米和薯类等经过发酵、蒸馏,可得到乙醇
D.使用乙醇汽油可以节省石油资源和有效地减少汽车尾气的污染九年级化学选择题中等难度题查看答案及解析
-
乙醇(C2H5OH)是以高粱、玉米、薯类等为原料,经发酵、蒸馏而制得,属于可再生能源.乙醇完全燃烧时生成二氧化碳和水.如果氧气不充足,乙醇燃烧可能还有CO生成.现用下图装置进行实验,确证乙醇燃烧产物中有CO、CO2和H2O.请回答下列问题:

(1)写出乙醇完全燃烧化学方程式______ 2CO2+3H2O九年级化学解答题中等难度题查看答案及解析
-
乙醇是以高粱、玉米、薯类等为原料,经发酵、蒸馏而制得,属于可再生能源。在汽油中加入适量乙醇作为汽油燃料,可节省石油资源,减少汽车尾气的污染。乙醇(C2H5OH)完全燃烧时生成CO2和H2O。如果氧气不充足,乙醇燃烧可能还生成CO。现用以下装置进行实验,验证乙醇燃烧产物中有CO、CO2和H2O。请回答下列问题:
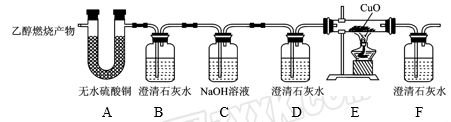
(1)能验证产物中有H2O的现象是无水CuSO4变蓝;能验证产物中有CO的现象是_____________。
(2)实验时,可观察到装置B中石灰水变浑浊,D中石灰水无变化。B装置的作用是____________;C装置的作用是________________;D装置的作用是____________________。
(3)若乙醇燃烧产物中CO和CO2的总质量为25.2 g,其中碳元素与氧元素的质量比为2∶5,则参加化学反应的乙醇的质量为________,反应产物中H2O的质量为________。
九年级化学简答题中等难度题查看答案及解析
-
日常生活中的柴、米、油、盐、酱、醋蕴含着许多化学知识,请填空:
(1) 你家里现在所用的“柴”是.
(2) 高粱、玉米和薯类等经过、蒸馏,可得到乙醇,乙醇属于(填“可再生”或“不可再生”)能源.
(3) 花生油属于下列营养素中的(填序号).
①蛋白质 ②维生素 ③油脂 ④糖类
(4) 不能用工业用盐NaNO2代替食盐用于烹调,原因是.
(5) 市面上的酱油常添加含铁元素的物质,目的是为了防止.
(6)家庭生活中常用食醋(溶质为醋酸,化学式为CH3COOH)洗去水壶内壁附着的水垢(主要成分为氢氧化镁和碳酸钙).已知醋酸与氢氧化镁反应的化学方程式为:Mg(OH)2+2CH3COOH=(CH3COO)2Mg+2H2O,仿照上述反应的化学方程式,写出醋酸与碳酸钙发生反应的化学方程式:.九年级化学填空题中等难度题查看答案及解析
-
高粱、玉米和薯类等经过发酵、蒸馏,可得到乙醇,乙醇属于________能源,俗称________,化学式为________,完全燃烧的化学方程式为________,如若在汽油中加入适量的________作为汽车燃料,可节省________,促进________,也可减少________.
九年级化学填空题中等难度题查看答案及解析
-
高粱、玉米和薯类经过发酵,可得到酒精,酒精属于(“再生”或“非再生”)能源.它是的俗称.化学式为,燃烧方程式为.
九年级化学填空题中等难度题查看答案及解析
-
酒精是________的俗称,可通过高粱、玉米和薯类等发酵蒸馏而得到,属于________(填“可再生“或”不可再生“)能源,酒精燃烧的化学方程式为________.
九年级化学填空题中等难度题查看答案及解析
-
图中A是高粱、玉米和薯类等经过发酵、蒸馏得到的一种可再生能源,现已在汽油中加入一定量的A,可节省石油资源,减少汽车尾气的污染,G是常见白色难溶盐。
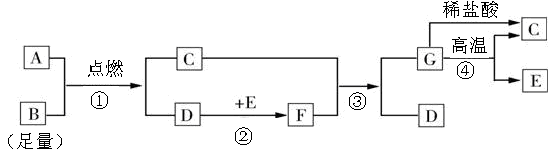 (1)物质A俗称________;物质E的化学式是________
(1)物质A俗称________;物质E的化学式是________(2)反应①的化学方程式是:________;
(3)反应②的基本反应类型是________;反应④的基本反应类型是________;
(4)反应③的化学方程式是:________.
九年级化学探究题极难题查看答案及解析
-
(2002•天津)乙醇是以高粱、玉米、薯类等为原料,经发酵、蒸馏而制得,属于可再生能源.在汽油中加入适量乙醇作为汽油燃料,可节省石油资源,减少汽车尾气的污染.2001年4月2日国家技术监督局发布《车用乙醇汽油》国家标准,并于同年4月15日开始实施.乙醇______完全燃烧时生成CO2和H2O.如果氧气不充足,乙醇燃烧可能还有CO生成.现用以下装置进行实验,确证乙醇燃烧产物中有CO、CO2和H2O.
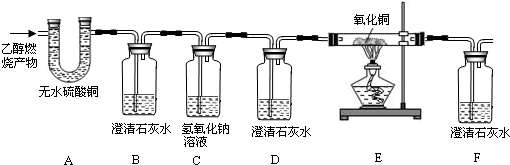
请回答下列问题:
(1)能确证产物中有H2O的现象是______;能确证产物中有CO的现象是______、______.
(2)实验时,可观察到装置B中石灰水变浑浊,D中石灰水无变化.B装置的作用是______;C装置的作用是______;D装置的作用是______.
(3)若乙醇燃烧产物中CO和CO2的总质量为25.2g,其中碳元素与氧元素的质量比为2:5,则参加反应的乙醇的质量为______g,产物中H2O的质量为______g.
(4)科学家发现海底埋藏着大量的“可燃冰”--甲烷的水合物.质量相等的甲烷和乙醇在氧气充足的条件下完全燃烧,产生CO2的质量较多的是______.九年级化学解答题中等难度题查看答案及解析