氯酸钾(KClO3)可用于生产火柴、烟花等,工业制备的主要流程如下:

已知:80℃时,氯化钠的溶解度为38.4g,且KCl、KClO3均易溶于水。
(1)生产中所需的NaCl溶液是在80℃时,按每100 g水中加入35 g NaCl配制而成,该溶液是 (填“饱和”或“不饱和”)溶液。
(2)溶液A中除NaCl外,一定存在的溶质是________。
九年级化学填空题简单题
氯酸钾(KClO3)可用于生产火柴、烟花等,工业制备的主要流程如下:

已知:80℃时,氯化钠的溶解度为38.4g,且KCl、KClO3均易溶于水。
(1)生产中所需的NaCl溶液是在80℃时,按每100 g水中加入35 g NaCl配制而成,该溶液是 (填“饱和”或“不饱和”)溶液。
(2)溶液A中除NaCl外,一定存在的溶质是________。
九年级化学填空题简单题
氯酸钾(KClO3)可用于生产火柴、烟花等,工业制备的主要流程如下:

已知:80℃时,氯化钠的溶解度为38.4g,且KCl、KClO3均易溶于水。
(1)生产中所需的NaCl溶液是在80℃时,按每100 g水中加入35 g NaCl配制而成,该溶液是 (填“饱和”或“不饱和”)溶液。
(2)溶液A中除NaCl外,一定存在的溶质是________。
九年级化学填空题简单题查看答案及解析
氯酸钾KClO3可用于生产火柴、烟花等。在工业上,通过如下转化可制得KClO3晶体。
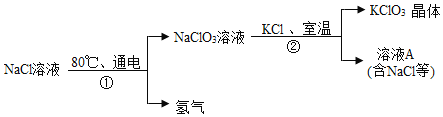
(1)NaClO3中氯元素的化合价是______,通过海水晒盐可以得到NaCl,其包含蒸发、______等过程;写出NaCl的一种用途______。
(2)溶液A中除NaCl外,一定存在的溶质是______和______填名称
。
(3)反应②属于复分解反应,写出该反应的化学方程式______。
九年级化学流程题简单题查看答案及解析
工业上常利用石灰浆(主要成分为Ca(OH)2)制备化工原料KClO3,流程如下:
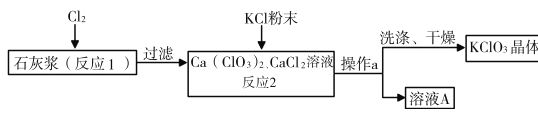
(资料)有关物质在20摄氏度时的溶解度如下:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(1)操作a的名称是_____,在实验室中完成此操作需要的玻璃仪器有烧杯、玻璃棒、_____,玻璃棒是作用是_____。
(2)反应1向石灰浆中通入Cl2,得到Ca(ClO3)2、CaCl2的混合溶液。化学方程式中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此化学方程式_____。
(3)提高Cl2转化为Ca(ClO3)2的转化率的可行措施有_____(填序号)。
A 适当加大通入Cl2的速率
B 充分搅拌浆料
C 加水使Ca(OH)2完全溶解
D 加热
(4)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和_____(填化学式),你认为该反应能得到KClO3晶体的原因是_____。
(5)洗涤KClO3晶体时,可选用_____(填序号)。
A 饱和KCl溶液
B 饱和CaCl2溶液
C 饱和KClO3溶液
九年级化学流程题困难题查看答案及解析
某兴趣小组对氯酸钾(KClO3)展开如下探究:
(探究一)工业制备KClO3
以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:
(资料卡片):氯化时,主要反应为6Ca(OH)2 + 6X ═ Ca(ClO3)2 + 5CaCl2 + 6H2O,少量 X与Ca(OH)2反应生成Ca(ClO)2、CaCl2和H2O,Ca(ClO)2 分解为CaCl2和O2。
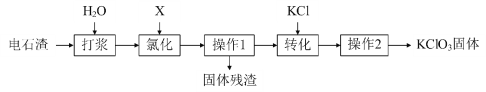
(1)根据资料,X的化学式为______,写出氯化时,X和Ca(OH)2反应生成Ca(ClO)2的化学方程式______。
(2)氯化时,为提高X转化为Ca(ClO3)2的转化率,下列措施可行的是______(填序号)。
A.充分搅拌浆料 B.加足量水使Ca(OH)2完全溶解 C.缓缓通入X
(3)操作1在实验室中的名称是______,需要用到的玻璃仪器有______、______和玻璃棒,玻璃棒的作用是______。氯化过程控制电石渣过量,固体残渣的主要成分为______和______(填化学式)。
(4)操作1后得到溶液中Ca(ClO3)2与CaCl2的化学计量数之比______1:5(填“>”、“<”或“=”)。转化时,加入KCl发生反应的化学方程式为______。
(5)操作2包含一系列实验操作,结合如图分析,主要操作为蒸发浓缩 →______→过滤→洗涤→低温烘干。
(探究二)探究KClO3制氧气
某小组利用如图所示装置对KClO3制氧气进行了探究:

(资料卡片):
①KClO3的熔点约为356℃,MnO2在加热条件下不分解。
②KClO3分解时,传感器得到氧气浓度随温度的变化示意图及使用不同催化剂时的固体残留率示意图如下:
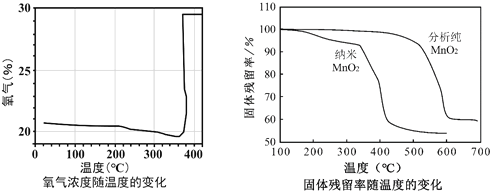
(6)由图可知KClO3分解温度______(填“高于”、“等于”或“低于”)其熔点。
(7)图中,在KClO3分解前,传感器测得氧气浓度降低的原因可能是______。
(8)分析图中,对KClO3分解催化效果更好的催化剂是______。
(9)将3.06gKClO3和MnO2混合物以4:1配比加热至完全反应,可得氧气体积约为多少升____?(写出计算过程,计算时精确到小数点后两位。已知氧气密度约为1.43g / L。)
九年级化学综合题困难题查看答案及解析
高氯酸钾(KClO4)主要用于生产烟花爆竹。以下是工业生产高氯酸钾 的工艺流程图,请回答问题。
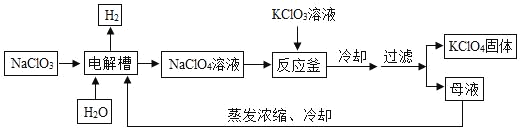
(1)冷却后过滤,说明高氯酸钾的溶解度随温度降低而_____。
(2)母液进入电解槽中需经蒸发浓缩,实验室进行蒸发浓缩时需不停搅拌,其目 的为_____。
(3)反应釜中发生复分解反应,该反应的化学方程式为_____。
(4)流程中可循环利用的物质(除水外)为_____。
九年级化学流程题中等难度题查看答案及解析
高氯酸钾(KClO4)主要用于生产烟花爆竹。以下是工业生产高氯酸钾 的工艺流程图,请回答问题。
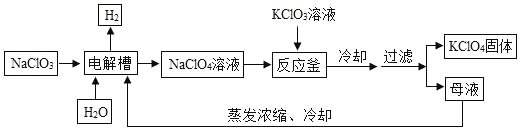
(1)冷却后过滤,说明高氯酸钾的溶解度随温度降低而_____。
(2)母液进入电解槽中需经蒸发浓缩,实验室进行蒸发浓缩时需不停搅拌,其目 的为_____。
(3)反应釜中发生复分解反应,该反应的化学方程式为_____。
(4)流程中可循环利用的物质(除水外)为_____。
九年级化学流程题中等难度题查看答案及解析
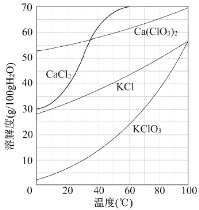
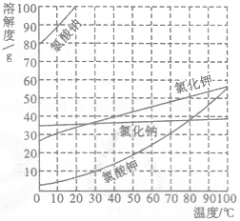
氯酸钾常用于制造火柴盒烟花等。工业上通过如图 1 所示转化可制得氯酸钾晶体。结合图2的溶解度曲线,回答下列问
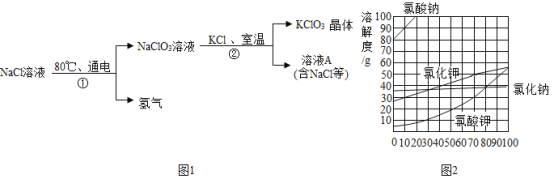
(1)80℃的氯化钠溶液中,氯化钠与水的质量比为 7:20,该溶液是_____(填“饱和溶液”或“不饱和溶液”)。
(2)40℃,氯化钾溶解度为 40g,要配置 70g 该温度的饱和溶液,需要氯化钾_____g, 水_____g。
(3)10℃时,如图中四种物质的饱和溶液,其中_____溶液的溶质质量分数最小。
(4)写出反应①的化学方程式:_____。
(5)反应②能发生的原因是_____。
(6)生成过程中,溶液 A 可循环利用,其优点是_____(写一点)。
九年级化学流程题困难题查看答案及解析
氯酸钾多用来制造火柴盒烟花等。工业上通过如下转化可制得氯酸钾晶体。

结合右下图的溶解度曲线,回答下列问题。
(1)副产品氢气的一种用途: 。
(2)80℃的氯化钠溶液中,氯化钠与水的质量比为7:20,该溶液是 (填“饱和”或“不饱和”)溶液。
(3)10℃时,图中四种物质的饱和溶液,其中溶液的溶质质量分数最小。
(4)配平反应①的化学方程式:

(5)反应②的基本反应类型是 ,该反应能发生的原因是 。
(6)生成过程中,溶液A可循环利用,其优点是 (任写一点)。
九年级化学填空题中等难度题查看答案及解析
工业上常利用石灰浆[主要成分为Ca(OH)2]制备化工原料KClO3,流程如下:
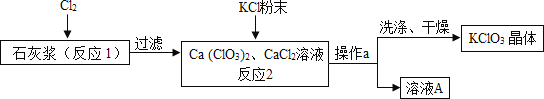
已知:
①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O。
②有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(1)操作a的名称是______,在实验室中完成此操作需要的玻璃仪器有烧杯、玻璃棒、______。
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和______(填化学式),你认为该反应能得到KClO3晶体的原因是______。
(3)洗涤KClO3晶体时,可选用下列______洗涤剂(填字母编号)
A KCl饱和溶液 B 冰水 C 饱和KClO3溶液
九年级化学流程题中等难度题查看答案及解析
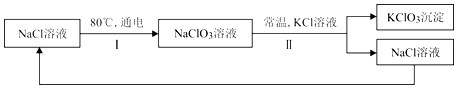
常温下,氯酸钾的溶解度较小,在工业上可通过如下工艺流程制得。
(1)写出实验室加热KClO3和二氧化锰的混合物制备氧气的化学方程式:_____。
(2)反应I中,通电时发生的反应方程式为:NaCl+3XNaClO3+3H2↑,则X的化学式为_____。
(3)反应Ⅱ的反应方程式为:_____。
(4)该流程中可以循环利用的物质是NaCl,从微观角度探析NaCl是由_____ 构成(用化学用语表示)。
九年级化学流程题中等难度题查看答案及解析