-
“潇湘”化学研究性学习小组对铁快速生锈进行了创新实验探究,实验设计如下图.
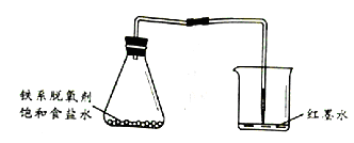
实验操作如下:
①如图所示组装好仪器.
②用锥形瓶收集一瓶氧气,塞上胶塞.在烧杯中倒入少量滴有红墨水的水(水不要加太多,没过导管末端即可).
③打开胶塞,向锥形瓶中快速加入4mL饱和食盐水、2g铁系脱氧剂(主要成分是活性铁粉).塞上胶塞,捏住乳胶管,轻轻摇晃锥形瓶,使悬浊液均匀挂在锥形瓶内壁上.
④将导管放入烧杯中.1分钟后,观察到导管中红色液柱高度超过25mm,锥形瓶内壁呈红褐色.
请回答下列问题:
(1)实验步骤①组装好仪器后,立即需要进行的操作是 。
(2)查资料得知,步骤④中红褐色固体为Fe(OH)3,它由生成的Fe(OH)2与氧气、水反应而来,写出生成红褐色固体的化学反应方程式 。
(3)下列各项是同学们对该创新实验的判断与评价,你认为不太合理的是 。
A.实验中用红墨水是便于观察 B.实验用氧气代替空气,毫无意义
C.实验用铁钉代替系脱氧剂,实验效果会更好 D.加入饱和食盐水可加快铁生锈的速度
-
(4分)为定量研究长期放置氢氧化钠药品变质情况,化学兴趣小组的同学设计了如下实验,其主要实验步骤如下:
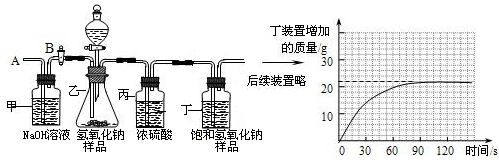
Ⅰ.按图组装仪器,将55.0g试样放入锥形瓶中,加入足量稀硫酸溶液;
Ⅱ.测量一定时间内装置丁内物质增加的质量(见下列曲线);
Ⅲ.待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓鼓入一定量的空气;
Ⅳ.再次称量装置丁内物质增加的质量;
Ⅴ.重复Ⅲ和Ⅳ的操作,直至装置丁内物质质量不变.
请根据实验数据,通过计算分析氢氧化钠变质情况(“全变质”,“部分变质”或“不变质”,要有详细的计算步骤,没有步骤不得分)
-
(13分)某品牌纯碱中含有少量氯化钠.某化学探究小组欲测定该品牌纯碱的纯度(即碳酸钠的质量分数)。
Ⅰ.甲组同学设计如图所示实验:
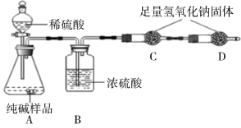
【实验步骤】①组装好如图仪器,并 ;
②称取7.0g样品放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品;
③称量装置C的质量;
④打开分液漏斗旋塞滴入稀硫酸,直到不再产生气泡为止;
⑤再次称量装置C 的总质量; ⑥计算出样品中碳酸钠的质量分数。
【实验分析】(1)A装置中反应的化学方程式为 ;
(2)B装置的作用是 ;
(3)如果没有D装置则所测样品中碳酸钠的质量分数偏大的原因是 ;
(4)称得纯碱样品的质量为7.0g,实验前、后C装置(包含药品)的质量分别为61.2g和63.4g,则该纯碱样品的纯度为 (计算结果精确到0.1%)。
Ⅱ.乙组同学采用生成沉淀的方法来测定样品中纯碱的质量分数,设计了如下实验:

(1)判断加入氯化钡溶液是否过量的合适方法是 (填编号),然后观察现象判断。
A.向混合物X中滴加稀硫酸,若有白色沉淀生成则说明氯化钡已经过量
B.静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量
(2)判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,然后观察现象判断。
(3)根据实验数据,乙组测得样品中碳酸钠的质量分数为多少?(写出计算过程,计算结果精确到0.1%)。
【实验反思】乙组所测实验数据比甲组更准确,你认为甲组存在较大偏差的原因可能是 。
-
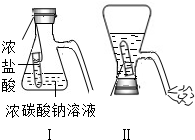
(2010•赤峰)某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究.

[提出问题]
废液中所含溶质是什么物质?
[猜想与假设]
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl.
猜想(二):废液中的溶质只有NaCl.
猜想(三):废液中的溶质是NaCl和HCl.
猜想(四):废液中的溶质是______.
[讨论与交流]
小明认为猜想(一)无需验证就知道是错误的.他的理由是______.
[实验与结论]
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解.于是小强认为猜想(二)正确.小强的实验______(填“能”或“不能”)验证猜想(二)的正确性,原因是______.
(2)小丽为验证猜想(三),选用大理石做试剂.若猜想(三)是正确的,验证时反应的化学方程式为______.
(3)若验证猜想(四)是否正确,下列试剂中可选用的有______(填序号).
①氢氧化钠溶液②氯化钙溶液③稀盐酸④氯化钾溶液
[拓展与应用]
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行______操作即可从废液中得到NaCl固体.此方法的缺点是______.
-
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究.
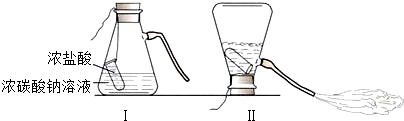
[提出问题]
废液中所含溶质是什么物质?
[猜想与假设]
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl.
猜想(二):废液中的溶质只有NaCl.
猜想(三):废液中的溶质是NaCl和HCl.
猜想(四):废液中的溶质是______.
[讨论与交流]
小明认为猜想(一)无需验证就知道是错误的.他的理由是______.
[实验与结论]
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解.于是小强认为猜想(二)正确.小强的实验______(填“能”或“不能”)验证猜想(二)的正确性,原因是______.
(2)小丽为验证猜想(三),选用大理石做试剂.若猜想(三)是正确的,验证时反应的化学方程式为______.
(3)若验证猜想(四)是否正确,下列试剂中可选用的有______(填序号).
①氢氧化钠溶液②氯化钙溶液③稀盐酸④氯化钾溶液
[拓展与应用]
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行______操作即可从废液中得到NaCl固体.此方法的缺点是______.
-
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究.
【提出问题】
废液中所含溶质是什么物质?
【猜想与假设】
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl.
猜想(二):废液中的溶质只有NaCl.
猜想(三):废液中的溶质是NaCl和HCl.
猜想(四):废液中的溶质是________.
【讨论与交流】
小明认为猜想(一)无需验证就知道是错误的.他的理由是________.
【实验与结论】
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解.于是小强认为猜想(二)正确.小强的实验________(填“能”或“不能”)验证猜想(二)的正确性,原因是________.
(2)小丽为验证猜想(三),选用大理石做试剂.若猜想(三)是正确的,验证时反应的化学方程式为________.
(3)若验证猜想(四)是否正确,下列试剂中可选用的有________(填序号).
①氢氧化钠溶液 ②氯化钙溶液 ③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行________操作即可从废液中得到NaCl固体.此方法的缺点是________.
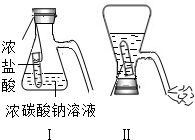
-
(10分)
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究。
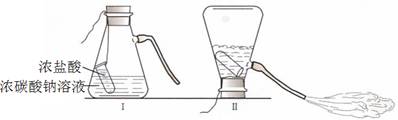
【提出问题】
废液中所含溶质是什么物质?
【猜想与假设】
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl。
猜想(二):废液中的溶质只有NaCl。
猜想(三):废液中的溶质是NaCl和HCl。
猜想(四):废液中的溶质是__________________。
【讨论与交流】
小明认为猜想(一)无需验证就知道是错误的。他的理由是___________________
____________________________________________。
【实验与结论】
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解。于是小强认为猜想(二)正确。小强的实验____________(填“能”或“不能”)验证猜想(二)的正确性,原因是________________。
(2)小丽为验证猜想(三),选用大理石做试剂。若猜想(三)是正确的,验证时反应的化学方程式为____________________________________。
(3)若验证猜想(四)是否正确,下列试剂中可选用的有____________(填序号)。
①氢氧化钠溶液 ②氯化钙溶液 ③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行_______________操作即可从废液中得到NaCl固体。此方法的缺点是________。
-
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究.
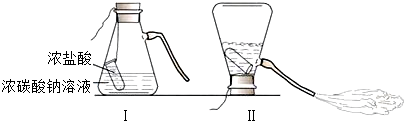
[提出问题]
废液中所含溶质是什么物质?
[猜想与假设]
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl.
猜想(二):废液中的溶质只有NaCl.
猜想(三):废液中的溶质是NaCl和HCl.
猜想(四):废液中的溶质是______.
[讨论与交流]
小明认为猜想(一)无需验证就知道是错误的.他的理由是______.
[实验与结论]
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解.于是小强认为猜想(二)正确.小强的实验______(填“能”或“不能”)验证猜想(二)的正确性,原因是______.
(2)小丽为验证猜想(三),选用大理石做试剂.若猜想(三)是正确的,验证时反应的化学方程式为______.
(3)若验证猜想(四)是否正确,下列试剂中可选用的有______(填序号).
①氢氧化钠溶液②氯化钙溶液③稀盐酸④氯化钾溶液
[拓展与应用]
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行______操作即可从废液中得到NaCl固体.此方法的缺点是______.
-
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究.

[提出问题]
废液中所含溶质是什么物质?
[猜想与假设]
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl.
猜想(二):废液中的溶质只有NaCl.
猜想(三):废液中的溶质是NaCl和HCl.
猜想(四):废液中的溶质是______.
[讨论与交流]
小明认为猜想(一)无需验证就知道是错误的.他的理由是______.
[实验与结论]
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解.于是小强认为猜想(二)正确.小强的实验______(填“能”或“不能”)验证猜想(二)的正确性,原因是______.
(2)小丽为验证猜想(三),选用大理石做试剂.若猜想(三)是正确的,验证时反应的化学方程式为______.
(3)若验证猜想(四)是否正确,下列试剂中可选用的有______(填序号).
①氢氧化钠溶液②氯化钙溶液③稀盐酸④氯化钾溶液
[拓展与应用]
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行______操作即可从废液中得到NaCl固体.此方法的缺点是______.
-
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究.
【提出问题】
废液中所含溶质是什么物质?
【猜想与假设】
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl.
猜想(二):废液中的溶质只有NaCl.
猜想(三):废液中的溶质是NaCl和HCl.
猜想(四):废液中的溶质是.
【讨论与交流】
小明认为猜想(一)无需验证就知道是错误的.他的理由是.
【实验与结论】
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解.于是小强认为猜想(二)正确.小强的实验(填“能”或“不能”)验证猜想(二)的正确性,原因是.
(2)小丽为验证猜想(三),选用大理石做试剂.若猜想(三)是正确的,验证时反应的化学方程式为.
(3)若验证猜想(四)是否正确,下列试剂中可选用的有(填序号).
①氢氧化钠溶液 ②氯化钙溶液 ③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行操作即可从废液中得到NaCl固体.此方法的缺点是.