-
某样品由氧化铜和铜组成。取10.0g该样品于烧杯中,向其中加入192.0g某浓度的稀硫酸,恰好完全反应,最终所得溶液质量为200.0g。(已知:CuO+H2SO4=CuSO4+H20)
(1)所取样品中含铜元素的质量为 g.
(2)计算最终所得溶液中溶质的质量分数。(请写出计算过程)
九年级化学计算题困难题查看答案及解析
-
某样品由氧化铜和铜组成,取10.0g该样品于烧杯中,向其中加入192.0g某浓度的稀硫酸,恰好完全反应,最终所得溶液质量200.0g
已知CuO+H2SO4==CuSO4+H2O)
所取样品中含铜元素的质量为______g。
计算最终所得溶液中溶质的质量分数_____。
请写出计算过程
九年级化学计算题中等难度题查看答案及解析
-
某样品有氧化铜和铜组成。取样品12g于烧杯中,向其中加入192g某浓度的稀硫酸,恰好完全反应,最终所得到的溶液质量为200g。
(1)氧化铜(CuO)中,铜、氧元素的质量比为_______;
(2)所取样品中氧化铜质量为_________ g;
(3)计算所用稀硫酸的溶质质量分数________。(要求写出计算过程)
九年级化学计算题简单题查看答案及解析
-
某样品由氧化铜和铜组成。取10.0g该样品于烧杯中,向其中加入92.0g稀硫酸,恰好完全反应后,过滤,所得滤液质量为100.0g。
(1)所取样品中铜的质量为_____。
(2)从反应后所得的100.0g滤液中取出10.0g溶液,将其稀释为10%的溶液,需要加水多少克___________?
九年级化学计算题中等难度题查看答案及解析
-
已知烧杯中装有200g硫酸和硫酸铜混合溶液,其中含硫酸铜4.8g。向烧杯中逐渐加入氧化铜,烧杯中溶液的质量与加入氧化铜的质量关系如图所示。当恰好完全反应时,所得的溶液为不饱和溶液。
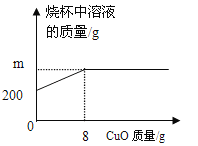
(提示:CuO + H2SO4 = CuSO4 + H2O)请计算:
(1)m=__________g。(1分)
(2)原混合溶液中H2SO4的质量分数。(2分)
(3)若取恰好完全反应时所得溶液10g配制成20%的硫酸铜溶液,需要30%的硫酸铜溶液多少克?(3分)
九年级化学简答题困难题查看答案及解析
-
已知烧杯中装有200g硫酸和硫酸铜混合溶液,其中含硫酸铜4.8g。向烧杯中逐渐加入氧化铜,烧杯中溶液的质量与加入氧化铜的质量关系如图所示。当恰好完全反应时,所得的溶液为不饱和溶液。
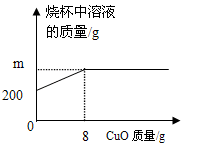
(提示:CuO + H2SO4 = CuSO4 + H2O)请计算:
(1)m=__________g。(1分)
(2)原混合溶液中H2SO4的质量分数。(2分)
(3)若取恰好完全反应时所得溶液10g配制成20%的硫酸铜溶液,需要30%的硫酸铜溶液多少克?(3分)
九年级化学计算题困难题查看答案及解析
-
一包黑色粉末含有氧化铜和炭粉。为了探究该粉末的组成,小夏取粉末10克加入到192克稀硫酸中恰好完全反应后得到残留固体质量为2克。
(1)原粉末中氧化铜的质量分数为 ;
(2)反应后所得溶液的溶质质量分数是多少?
九年级化学简答题中等难度题查看答案及解析
-
某铜矿样品的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3。现称取29.6t纯度为75%的该样品放入烧杯中,加入一定量的稀盐酸,恰好完全反应后,所得氯化铜溶液的溶质质量分数为27 %。
提示: 1.
;
2.铜矿中杂质既不溶于水,也不参与反应;
3.Cu2(OH)2CO3的相对分子质量为222。
求: (1) Cu2(OH)2CO3中质量分数最大的元素是______________。
(2)上述稀盐酸的溶质质量分数是多少?____ 。(写出计算过程,最终结果精确到0.1%)
(3)工业上结合该方法,继续反应可提炼出铜单质。假设提纯时铜元素无损失,每得到1t铜单质的成本为M元,提纯上述样品的成本是______________元。
九年级化学计算题困难题查看答案及解析
-
为研究氧化铁与硫酸的反应,化学实验小组称取8g氧化铁放入烧杯,向其中缓缓加入10%稀硫酸,当烧杯中固体恰好完全溶解时,测得加入稀硫酸质量为147g.
完成实验后将所得溶液回收,通过计算得出试剂瓶标签(如图)上应标明的溶质质量分数是多少?(计算结果取整数).九年级化学解答题中等难度题查看答案及解析
-
氧化亚铜(Cu2O)可用于船底防污漆,防止海生物对船舶设备的污损。某氧化亚铜样品中含有10%的金属铜,现取4.0g该样品放入烧杯中,加入一定溶质质量分数的稀硫酸恰好完全反应,得到27.0g不饱和溶液。发生反应的化学方程式为Cu2O+H2SO4=CuSO4+Cu+H2O
请计算:(1)所取样品中氧化亚铜的质量为________g。
(2)所用稀硫酸溶质的质量分数。
九年级化学计算题困难题查看答案及解析