-
选择“低碳生活”,减少二氧化碳排放,是每位公民应尽的义务和责任.
(1)自然界中消耗二氧化碳的主要途径是________;
(2)请你写出一种日常生活中符合“低碳生活”理念的做法:________.
-
选择“低碳生活”,减少二氧化碳排放,是每位公民应尽的责任和义务.
①生活中少用10个塑料袋可以减少约0.02molCO2排放.CO2的摩尔质量是________;它属于________氧化物(填“酸性”或“碱性”). 0.02molCO2约含有________个CO2分子.
②“低碳交通”鼓励使用新能源,氢能是最清洁的能源,写出氢气燃烧的化学方程式________.
③回收可利用的资源,如旧手机中的金属.手机机芯中含有铜、金、银等.写出银的化学式________.下图是实验室制取金属铜的流程图:

Ⅰ.氧化铜与盐酸反应的化学方程式是________.
Ⅱ.溶液A的溶质组成是________.
Ⅲ.在固体B中加入过量的________溶液,再通过________的分离方法得到金属铜.
-
选择“低碳生活”,减少二氧化碳排放,是每位公民应尽的责任和义务.
①生活中少用10个塑料袋可以减少约0.02molCO2排放.CO2的摩尔质量是________;它属于________氧化物(填“酸性”或“碱性”). 0.02molCO2约含有________个CO2分子.
②“低碳交通”鼓励使用新能源,氢能是最清洁的能源,写出氢气燃烧的化学方程式________.
③回收可利用的资源,如旧手机中的金属.手机机芯中含有铜、金、银等.写出银的化学式________.下图是实验室制取金属铜的流程图:

Ⅰ.氧化铜与盐酸反应的化学方程式是________.
Ⅱ.溶液A的溶质组成是________.
Ⅲ.在固体B中加入过量的________溶液,再通过________的分离方法得到金属铜.
-
选择“低碳生活”,减少二氧化碳排放,是每位公民应尽的责任和义务.
①生活中少用10个塑料袋可以减少约0.02molCO2排放.CO2的摩尔质量是________;它属于________氧化物(填“酸性”或“碱性”). 0.02molCO2约含有________个CO2分子.
②“低碳交通”鼓励使用新能源,氢能是最清洁的能源,写出氢气燃烧的化学方程式________.
③回收可利用的资源,如旧手机中的金属.手机机芯中含有铜、金、银等.写出银的化学式________.下图是实验室制取金属铜的流程图:

Ⅰ.氧化铜与盐酸反应的化学方程式是________.
Ⅱ.溶液A的溶质组成是________.
Ⅲ.在固体B中加入过量的________溶液,再通过________的分离方法得到金属铜.
-
选择“低碳生活”,减少二氧化碳排放,是每位公民应尽的责任和义务。
①生活中少用10个塑料袋可以减少约0.02molCO2排放。CO2的摩尔质量是________(6)________;它属于________(7)________氧化物(填“酸性”或“碱性”)。 0.02molCO2约含有________(8)________个CO2分子。
②“低碳交通”鼓励使用新能源,氢能是最清洁的能源,写出氢气燃烧的化学方程式
________(9)________ 。
③回收可利用的资源,如旧手机中的金属。手机机芯中含有铜、金、银等。写出银的化学式________(10) 。下图是实验室制取金属铜的流程图:

Ⅰ.氧化铜与盐酸反应的化学方程式是________(11)________。
Ⅱ.溶液A的溶质组成是________(12)________。
Ⅲ.在固体B中加入过量的________(13)________溶液,再通过________(14)________的分离方法得到金属铜。
-
“低碳城市”的理念贯穿在上海世博园的建设中
(1)“低碳城市”的建设减少了二氧化碳气体的排放,能减缓________的程度;自然界中消耗二氧化碳的主要途径是________;请你写出一种日常生活中符合“低碳经济”理念的做法:________.
(2)法国化学家PaulSabatier采用“组合转化”技术使CO2和H2在催化剂作用下生成CH4和H2O.试写出该反应的化学方程式________.
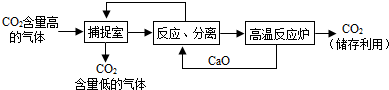
(3)近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用足量的NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).①捕捉室中发生反应的化学方程式为:________.
②把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式:________;利用此反应,氧化钙可用作食品________剂.
③“反应分离”中,得到固体物质的基本操作是________,该固体是碳酸钙.
④整个过程中,可以循环利用的物质有________.
(4)取10g碳酸钙固体高温加热,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%,则下列判断正确的是________.
A.生成了2g二氧化碳
B.剩余固体质量为5g
C.生成了5.6g氧化钙
D.剩余碳酸钙的质量为8g.
-
“低碳城市”的理念贯穿在上海世博园的建设中

(1)“低碳城市”的建设减少了二氧化碳气体的排放,能减缓________的程度;自然界中消耗二氧化碳的主要途径是________;请你写出一种日常生活中符合“低碳经济”理念的做法:________.
(2)法国化学家PaulSabatier采用“组合转化”技术使CO2和H2在催化剂作用下生成CH4和H2O.试写出该反应的化学方程式________.
(3)近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用足量的NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).①捕捉室中发生反应的化学方程式为:________.
②把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式:________;利用此反应,氧化钙可用作食品________剂.
③“反应分离”中,得到固体物质的基本操作是________,该固体是碳酸钙.
④整个过程中,可以循环利用的物质有________.
(4)取10g碳酸钙固体高温加热,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%,则下列判断正确的是________.
A.生成了2g二氧化碳
B.剩余固体质量为5g
C.生成了5.6g氧化钙
D.剩余碳酸钙的质量为8g.
-
“低碳城市”的理念贯穿在上海世博园的建设中。
(1)“低碳城市”的建设减少了二氧化碳气体的排放,能减缓________的程度;自然界中消耗二氧化碳的主要途径是________;请你写出一种日常生活中符合“低碳经济”理念的做法:。
(2)法国化学家PaulSabatier采用“组合转化”技术使CO2和H2在催化剂作用下生成CH4和H2O。试写出该反应的化学方程式________。
(3)近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量。“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用。常利用足量的NaOH溶液来“捕捉”CO2,过程如下图所示(部分条件及物质未标出)。
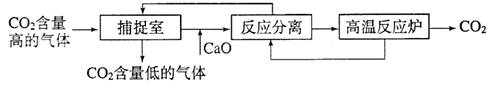
①捕捉室中发生反应的化学方程式为:。
②把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式:________;利用此反应,氧化钙可用作食品________剂。
③“反应分离”中,得到固体物质的基本操作是________,该固体是碳酸钙。
④整个过程中,可以循环利用的物质有________。
(4)取10g碳酸钙固体高温加热,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%,则下列判断正确的是________
A.生成了2g二氧化碳
B.剩余固体质量为5g
C.生成了5.6g氧化钙
D.剩余碳酸钙的质量为8g
-
爱护水资源是每个公民应尽的责任和义务。下列做法你认为不合理的是
A.洗菜、淘米的水用来浇花、冲厕所 B.关闭所有化工厂,堵住污染源
C.生活污水坚持达标排放 D.合理施用农药化肥,以减少水体污染
-
水是生命之源,是人类最宝贵的自然资源,爱惜水、保护水是每个公民的义务和责任。
(1)下列说法错误的是 (填序号)。
①农业和园林浇灌改大水漫灌为喷灌、滴灌
②将生活用水、地表雨水分类处理,可减少污染,保护水资源
③淡水资源很丰富,是取之不尽、用之不竭的
(2)生活中常通过 来降低水的硬度,实验室中常用 的方法除去不溶于水的杂质。






