-
(2011•南开区一模)某同学做了过氧化氢和二氧化锰制氧气的实验后,又设计了几组实验探究影响过氧化氢分解的速率.
(1)实验一:每次均用30mL10%的过氧化氢溶液,采用二氧化锰粉末做催化剂,测定各次收集到500mL氧气所用的时间,记录结果如下:(其他实验条件均相同)
该实验证明了______对反应速率______(填“有”或“无”)影响.实验次序 1 2 3 4 5 6 7 8 9 10 MnO2用量(g) 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1.0 所用时间(s) 17 8 7 5 4 3 2 2 2 2
(2)实验二:每次均取5mL30%的过氧化氢溶液,然后稀释成不同浓度的溶液进行实验.记录数据如下:(其他实验条件均相同)
请分析表中数据回答:实验次序 1 2 3 4 5 6 7 8 过氧化氢溶液的浓度 1% 3% 5% 10% 15% 20% 25% 30% MnO2用量(g) 0.2 0.2 0.2 0.2 0.2 0.2 0.2 0.2 收集到540毫升气体所用时间(s) 660 220 205 80 25 9 4 3
过氧化氢的浓度对反应速率是怎样影响的呢?______.
(3)实验三:探究温度是否对反应速率有影响.以下是设计的实验记录表:
表中①的数据为______;表中②的数据为______.实验次序 1 2 3 过氧化氢溶液的浓度 ① 10% 10% MnO2用量(g) 0.2 0.2 ② 温度(゜C) 20 40 60 收集到相同量气体所用时间(s) 九年级化学解答题中等难度题查看答案及解析
-
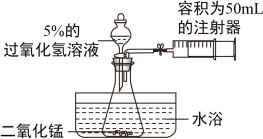
南开中学的牛小政同学为了探究温度对过氧化氢分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
实验1
实验2
二氧化锰质量/g
0.5
0.5
5%的过氧化氢溶液/mL
40
待填
水浴温度/°C
20
80
(1)写出该反应涉及的化学方程式:___________,其中二氧化锰的作用是______。
(2)实验2中应加入5%过氧化氢溶液____________mL。
(3)在两次实验中,可通过___________来比较过氧化氢分解反应速率的大小。
九年级化学实验题中等难度题查看答案及解析
-
某同学做了过氧化氢和二氧化锰制氧气的实验后,又设计了几组实验探究影响过氧化氢分解的速率.
(1)实验一:每次均用30mL10%的过氧化氢溶液,采用二氧化锰粉末做催化剂,测定各次收集到500mL氧气所用的时间,记录结果如下:(其他实验条件均相同)
该实验证明了______对反应速率______(填“有”或“无”)影响.实验次序 1 2 3 4 5 6 7 8 9 10 MnO2用量(g) 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1.0 所用时间(s) 17 8 7 5 4 3 2 2 2 2
(2)实验二:每次均取5mL30%的过氧化氢溶液,然后稀释成不同浓度的溶液进行实验.记录数据如下:(其他实验条件均相同)
请分析表中数据回答:实验次序 1 2 3 4 5 6 7 8 过氧化氢溶液的浓度 1% 3% 5% 10% 15% 20% 25% 30% MnO2用量(g) 0.2 0.2 0.2 0.2 0.2 0.2 0.2 0.2 收集到540毫升气体所用时间(s) 660 220 205 80 25 9 4 3
过氧化氢的浓度对反应速率是怎样影响的呢?______.
(3)实验三:探究温度是否对反应速率有影响.以下是设计的实验记录表:
表中①的数据为______;表中②的数据为______.实验次序 1 2 3 过氧化氢溶液的浓度 ① 10% 10% MnO2用量(g) 0.2 0.2 ② 温度(゜C) 20 40 60 收集到相同量气体所用时间(s) 九年级化学解答题中等难度题查看答案及解析
-
某同学设计以下实验探究氧化铜能否作为过氧化氢分解制取氧气的催化剂,以及影响化学反应速率的因素。
实验序号
H2O2溶液浓度/%
H2O2溶液体积/mL
温度/℃
催化剂种类及用量/g
氧气体积/mL
收集氧气所用时间/s
①
5
10
20
无
100
-
②
5
10
20
二氧化锰1g
100
15
③
5
10
40
二氧化锰1g
100
8
④
10
10
20
二氧化锰1g
100
5
⑤
5
10
20
氧化铜1g
100
22
(1)通过实验____和____对比,说明过氧化氢分解的速率与温度有关。
(2)通过实验____和____对比,说明过氧化氢分解的速率与浓度有关。
(3)通过实验____和____对比,说明氧化铜粉末能加快过氧化氢分解速率。
(4)想要证明氧化铜是该反应的催化剂,还需要验证其在反应前后____和____没有发生改变。
(5)①写出氧化铜催化过氧化氢分解的文字表达式:__________。
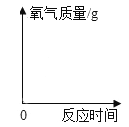
②根据以上实验得出的结论,在下图中画出有、无氧化铜时过氧化氢分解产生氧气的质量与反应时间的关系图____________。
九年级化学实验题中等难度题查看答案及解析
-
某兴趣小组同学对实验室“过氧化氢分解制氧气”的条件进行了如下探究。
[探究活动1]探究催化剂的种类对过氧化氢分解速率的影响。
设计实验:小组同学设计下列对比实验,实验①:将30g10%过氧化氢溶液与1g二氧化锰均匀混合:实验②将xg 10%过氧化氢溶液与1g氧化铜均匀混合。
实验①中反应的化学方程式是_____;实验②中x的值应为_____。
[探究活动2]探究一些因素对过氧化氢分解速率的影响。
收集证据:小组同学通过实验采集到相关实验数据如下表。
过氧化氢溶液的质量
过氧化氢溶液的浓度
二氧化锰的质量
相同时间内产生氧气体积
Ⅰ
50. 0g
1%
0.1g
9mL
Ⅱ
50. 0g
2%
0.1g
16mL
Ⅲ
50. 0g
4%
0.1g
31mL
问题与讨论: (1) 本实验的结论是_____。
(2)实验时,测量氧气体积的装置应选择下图中_____(填编号)。
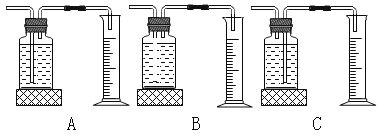
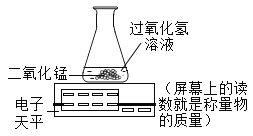
(3)小强同学设计了下图所示装置完成上述实验,通过比较相同时间内_____同样能获取该实验的结论。
九年级化学科学探究题困难题查看答案及解析
-
某小组同学为探究二氧化锰对过氧化氢分解速度的影响,设计了以下实验:
(1)完善实验一、实验二:
实验步骤
实验现象
实验结论
实验一
带火星的木条不复燃
过氧化氢分解的速率较慢
实验二
___________
________
(2)实验三:待实验二结束,剩余的液体化学式为_____,倒出多余液体,继续向其中加入5%的过氧化氢溶液,实验现象为____________,得出结论__________,写出此时的反应方程式__________;
(3)实验四,实验之前称量加入二氧化锰的质量为m1,待实验三结束后,取出二氧化锰,干燥后称量质量为m2,则m1_____m2(填“>”、“<”、“=”),得出结论___________,从液体中取出二氧化锰的操作名称为______;
九年级化学科学探究题困难题查看答案及解析
-
某小组同学为探究二氧化锰对过氧化氢分解速度的影响,设计了以下实验:
(1)完善实验一、实验二:
实验步骤
实验现象
实验结论
实验一
带火星的木条不复燃
过氧化氢分解的速率较慢
实验二
___________
________
(2)实验三:待实验二结束,剩余的液体化学式为_____,倒出多余液体,继续向其中加入5%的过氧化氢溶液,实验现象为____________,得出结论__________,写出此时的反应方程式__________;
(3)实验四,实验之前称量加入二氧化锰的质量为m1,待实验三结束后,取出二氧化锰,干燥后称量质量为m2,则m1_____m2(填“>”、“<”、“=”),得出结论___________,从液体中取出二氧化锰的操作名称为______;
九年级化学科学探究题困难题查看答案及解析
-
某小组同学为探究二氧化锰对过氧化氢分解速度的影响,设计了以下实验:
(1)完善实验一、实验二:
实验步骤
实验现象
实验结论
实验一
带火星的木条不复燃
过氧化氢分解的速率较慢
实验二
___________
________
(2)实验三:待实验二结束,剩余的液体化学式为_____,倒出多余液体,继续向其中加入5%的过氧化氢溶液,实验现象为____________,得出结论__________,写出此时的反应方程式__________;
(3)实验四,实验之前称量加入二氧化锰的质量为m1,待实验三结束后,取出二氧化锰,干燥后称量质量为m2,则m1_____m2(填“>”、“<”、“=”),得出结论___________,从液体中取出二氧化锰的操作名称为______;
九年级化学科学探究题困难题查看答案及解析
-
实验室常用过氧化氢溶液和二氧化锰制氧气,回答下列问题:
(1)为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置)去),进行了两次实验,两次实验的部分设计如表所示:
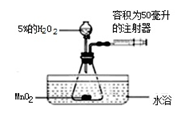
实验1
实验2
MnO2的质量
0.5克
0.5克
5%的H2O2溶液体积
40mL
待填
水浴温度
20℃
80℃
① 此反应的符号表达式是______________
② 实验2中“待填”的数据是 毫升;在两次实验中,可以通过一定时间内__________内的______________的多少来精确比较H2O2分解反应速率的大小。
③ 实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还可能的原因有 。
④ 实验结束后若要将不溶于水的MnO2从剩余物中分离出来,实验操作步骤(简单描述)是___________→用水冲洗MnO2 →烘干二氧化锰。
(2)探究使带火星木条复燃的氧气的最低浓度。用容积为300mL的集气瓶排水法收集氧气,当刚好把瓶中预先留有的100mL水排尽时,集气瓶中氧气的体积分数为(写出计算式即可):________________________。
实验研究结果显示:O2的体积分数大于49%时就可使带火星的木条复燃。因此,用带火星的木条验满O 2的方法 (填“可靠”或“不可靠”)。为此,收集O2时最好使用 集气法(不需要验满)。
九年级化学探究题困难题查看答案及解析
-
为探究浓度对过氧化氢分解反应速率的影响,同学们设计了如下三个实验:二氧化锰放在气球中,实验时将二氧化锰同时倒入试管中,在反应结束前的某一时间同时观察,现象如图所示。

(1)过氧化氢与二氧化锰混合时发生反应的化学方程式为______。
(2)②中所取过氧化氢溶液体积和二氧化锰质量分别为______。
(3)该实验得出的结论是______。
九年级化学简答题中等难度题查看答案及解析