课外探究时,某兴趣小组同学选择了“金属和酸反应快慢与什么因素有关”课题.
(1)其他条件相同,同种金属与不同质量分数的盐酸反应,反应的快慢不同.取质量相等的铝片,分别放入5%、20%的足量稀盐酸中,实验表明盐酸浓度越大,反应速率越快.如图1中Ⅰ、Ⅱ、Ⅲ是三位同学记录实验生成氢气的质量(m)与反应时间(t)的关系曲线,其中正确的是 .
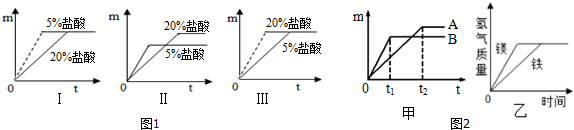
(2)其他条件相同,不同金属与相同质量分数的盐酸反应,反应的快慢不同.取质量相等的镁片、锌片、铁片中的两种金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图甲所示.则曲线A对应的金属与稀盐酸反应后生成的盐的名称是 .
(3)有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图乙所示.下列结果可能的是 (填序号).
①反应后镁有剩余 ②反应后铁有剩余
③反应后稀硫酸有剩余 ④反应后稀盐酸有剩余
⑤剩余铁的和镁的质量相等 ⑥消耗的稀硫酸和稀盐酸质量相等.
九年级化学探究题中等难度题