-
某同学为了检验家里购买的硫酸铵化肥是否合格,称取了27.5 g化肥样品与足量浓烧碱溶液一起加热,产生的氨气用足量的100.0 g废硫酸吸收,测得吸收氨气后的溶液总质量为106.8 g,已知合格硫酸铵化肥中含氮量不低于20%。所涉及的反应为:(NH4)2SO4+2NaOH Na2SO4+2NH3↑+2H2O,
Na2SO4+2NH3↑+2H2O,
2NH3+H2SO4=(NH4)2SO4。试计算:
(1)化肥样品完全反应后产生氨气_________g。
(2)该化肥的含氮量为____________(精确到0.1%),属于_____________(填“合格”或“不合格”)产品。
-
某同学为了检验家里购买的硫酸铵化肥是否合格,称取了27.5g化肥样品与足量浓烧碱溶液一起加热,产生的氨气用足量的100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如右图所示.已知合格硫酸铵化肥中含氮量不低.20%.所涉及的反应为(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑;2NH3+H2SO4=(NH4)2SO4.试计算:
(1)化肥样品完全反应后产生氨气______g.
(2)该化肥的含氮量为______ (精确到0.1%),属于______ (选填“合格”或“不合格”)产品.
(3)废硫酸充分吸收氨气后溶液中的硫酸铵质量分数是多少(写出计算过程,精确到0.1%).

-
某同学为了检验家里购买的硫酸铵化肥是否合格,称取了27.5g化肥样品与足量浓烧碱溶液一起加热,产生的氨气用足量的100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如右图所示.已知合格硫酸铵化肥中含氮量不低.20%.所涉及的反应为(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑;2NH3+H2SO4=(NH4)2SO4.试计算:
(1)化肥样品完全反应后产生氨气______g.
(2)该化肥的含氮量为______ (精确到0.1%),属于______ (选填“合格”或“不合格”)产品.
(3)废硫酸充分吸收氨气后溶液中的硫酸铵质量分数是多少(写出计算过程,精确到0.1%).

-
某同学为了检验家里购买的硫酸铵化肥是否合格,称取了27.5g化肥样品与足量浓烧碱溶液一起加热,产生的氨气用足量的100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如右图所示.已知合格硫酸铵化肥中含氮量不低于20%.所涉及的反应为(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑;2NH3+H2SO4=(NH4)2SO4.试计算:
(1)化肥样品完全反应后产生氨气______g.
(2)该化肥的含氮量为______(精确到0.1%),属于______(选填“合格”或“不合格”)产品.
(3)反应中所消耗的硫酸的质量是多少(写出计算过程).

-
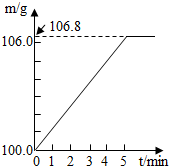
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸(足量)吸收.测得吸收氨气的溶液总质量m与反应时间的变化如图所示.(所涉及反应(NH4)SO4+2NaOH=Na2SO4+2H2O+NH3↑;
2NH3+H2SO4=(NH4)2SO4)
请计算:
(1)完全反应后产生氨气质量为______.
(2)该化肥的含氮量为多少?写出解题过程.通过计算判断这种化肥是否合格?
-
(2009•肇庆)某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如右下图所示.所涉及的反应为:
(NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑;2NH3+H2SO4═(NH4)2SO4.
请计算:
(1)完全反应后产生氨气______g.
(2)该化肥的含氮量为______(精确到0.1%),则这种化肥属于______(填:“合格”或“不合格”.合格硫酸铵含氮量为20%以上)产品.
(3)请计算废硫酸中硫酸的质量分数(写出计算过程).
(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是______.

-
(2009•肇庆)某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收.测得吸收氨气的溶液总质量m与反应时间t的变化如右下图所示.所涉及的反应为:
(NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑;2NH3+H2SO4═(NH4)2SO4.
请计算:
(1)完全反应后产生氨气______g.
(2)该化肥的含氮量为______(精确到0.1%),则这种化肥属于______(填:“合格”或“不合格”.合格硫酸铵含氮量为20%以上)产品.
(3)请计算废硫酸中硫酸的质量分数(写出计算过程).
(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是______.

-
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如图所示(假设两者恰好完全反应).所涉及的反应为:(NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4═(NH4)2SO4.请计算:
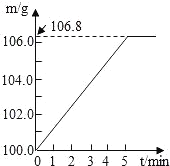
(1)完全反应后产生氨气_____g。
(2)该化肥的含氮量为_____(精确到0.1%),则这种化肥属于_____ (填:“合格”或“不合格”。合格硫酸铵含氮量为20%以上)产品。
(3)请计算废硫酸中硫酸的质量分数_____(写出计算过程)。
-
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如图所示(假设两者恰好完全反应).所涉及的反应为:(NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4═(NH4)2SO4.请计算:
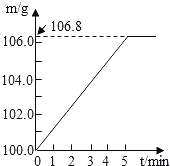
(1)完全反应后产生氨气_____g。
(2)该化肥的含氮量为_____(精确到0.1%),则这种化肥属于_____ (填:“合格”或“不合格”。合格硫酸铵含氮量为20%以上)产品。
(3)请计算废硫酸中硫酸的质量分数_____(写出计算过程)。
-
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5 g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如图所示。所涉及的反应为:
(NH4)2SO4+2NaOH Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 ==(NH4)2SO4。
Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 ==(NH4)2SO4。

请计算:
(1)完全反应后产生氨气________g。
(2)该化肥的含氮量为 ________(精确到0.1%),则这种化肥属于________ (填:“合格”或“不合格”。合格硫酸铵含氮量为20%以上)产品。
(3)请计算废硫酸中硫酸的质量分数(写出计算过程)。
(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是________。
Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4=(NH4)2SO4 。








