-
Ⅰ、Ⅱ两题只选做一题,如果两题全做,只按Ⅰ题计分.
Ⅰ.我们在实验室看到的浓硝酸往往呈黄色,这是由于硝酸的化学性质不稳定、见光或受热易分解的缘故.
(1)硝酸分解的化学方程式为:4HNO3═2H2O+4R↑+O2↑,则R的化学式为;为了防止硝酸的分解,你认为贮存硝酸的合理方法是.
(2)溶质质量分数为10%的硝酸的pH(填“>”、“<”或“﹦”)溶质质量分数为5%的硝酸的pH.
Ⅱ.下图所示为上海世博会吉祥物“海宝”的毛绒玩具,其外部材料为纯羊毛绒,内充物为无毒的聚酯纤维.
(1)以上两种材料中,属于合成纤维的是,请说出一点合成纤维与天然纤维相比的缺点是(填一点即可).
(2)聚酯纤维仅有C、H、O三种元素组成,则其在空气中完全燃烧的产物是.九年级化学填空题中等难度题查看答案及解析
-
我们在实验室看到的浓硝酸往往呈黄色,这是由于硝酸的化学性质不稳定、分解生成NO2的缘故.纯净的硝酸或浓硝酸在常温下见光或受热就会分解,有关反应为:见光或受热4HNO3═2H2O+4NO2↑+O2↑.为防止硝酸的分解,下列贮存硝酸的方法中你认为合理的是( )
A.无色试剂瓶
B.棕色试剂瓶
C.无色试剂瓶并置于阴凉处
D.棕色试剂瓶并置于阴凉处九年级化学选择题中等难度题查看答案及解析
-
学校化学兴趣小组的同学在实验中发现工业硝酸是呈黄色,他们查资料后找到这样解释;工业硝酸呈黄色是由于NO2溶于浓硝酸引起的.“这个解释对吗?”,他们决定进行探究[已知如下化学知识:3NO2(红棕色)+H2O=2HNO3+NO↑(无色) 2NO+O2=2NO2,4HNO3(浓)=4NO2↑+O2↑+2H2O.硫氰化铁为血红色物质(Fe(SCN)3)]
请填写空白.
(一)[猜想]:工业硝酸呈黄色是由于NO2溶于浓硝酸引起的
[设计与实验]:
甲、乙、丙三位同学各在一支洁净试管中倒入约2ml工业硝酸,进行如下实验:
(二)实验步骤 现象 结论 甲 加入5ml的蒸馏水,
振荡使之充分混合试管中的硝酸接近于无色 硝酸中没有其它杂质,猜想正确 乙 置于酒精灯上小火加热(在通风厨中进行) 有红棕色气体逸出,继续加热,直到不再有红棕色气体逸出为止.溶液的黄色变浅,但不能完全消失.
________.丙 通入氧气 通入足量氧气后,溶液的黄色变浅.
[提出问题]:上述实验后,溶液还是浅黄色,它还含有什么物质呢?乙、丙两同学提出如下猜想.
[猜想]:________.
[设计与实验]
[讨论与交流]:实验步骤 现象 结论 乙 在除去NO2的工业硝酸中,缓缓加入足量NaOH固体 ________ 猜想
正确丙 在除去NO2的工业硝酸中加入硫氰化钾 产生血红色物质
(1)在(一)中,丙同学实验的原理是:________(用方程式表示)
(2)甲同学实验得出错误结论的原因可能是________.九年级化学填空题中等难度题查看答案及解析
-
硝酸(HNO3)是实验室常见的一种酸。实验小组对硝酸的某些性质进行研究。
Ⅰ、挥发性
(实验1)取一瓶质量分数为68%的浓硝酸,打开瓶盖,遇潮湿的空气,瓶口可以看到_____,原因是_____。
Ⅱ、不稳定性
(查阅资料1)硝酸是无色液体,见光或受热分解生成红棕色的NO2气体、氧气及一种无色液体
(1)硝酸分解的化学方程式为:_____。
(实验2)取3份浓度和体积均相同的浓硝酸分别放入3支试管中,塞好塞子,放置在室外阳光充足的地方(气温为26℃)。记录溶液上方的气体颜色随时间的变化情况。
实验编号
①
②
③
实验条件
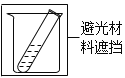
实验现象
6分钟出现浅红棕色
15分钟红棕色比较明显
30分钟红棕色非常明显
60分钟无明显变化
3分钟出现浅红棕色
6分钟红棕色比较明显
10分钟红棕色非常明显
(2)实验①、②对比是研究_____对浓硝酸稳定性的影响。
(3)实验①、③对比可得出的结论是_____。
Ⅲ、酸性
(查阅资料2)硝酸能够与金属氧化物反应生成盐和水。
(实验3)向氧化铜粉末中加入硝酸,能够看到的现象是_____。
IV、氧化性
(查阅资料3)浓硝酸在加热条件下能与木炭发生反应:
C+4HNO3(浓)
4NO2↑+CO2↑+2H2O。
(实验4)如图所示,将红热的木炭伸到浓硝酸上方,观察到有红棕色气体产生。请解释生成该红棕色气体的原因可能是_____。
九年级化学科学探究题困难题查看答案及解析
-
硝酸(HNO3)是实验室常见的一种酸,实验小组对硝酸的某些性质进行研究。
I.挥发性
(实验1)取一瓶质量分数68%的浓硝酸,打开瓶盖,遇潮湿的空气,瓶口可以看到__________。
II.不稳定性
(查阅资料1)硝酸是无色液体,见光或受热分解生成红棕色的NO2气体。
(1)硝酸分解的化学方程式为:4HNO3
4NO2↑+O2↑+___。
(实验2)取3份浓度和体积均相同的浓硝酸分别放入3支试管中,塞好塞子,放置在室外阳光充足的地方(气温为26 ℃)。记录溶液上方的气体颜色随时间的变化情况。
实验编号
①
②
③
实验条件
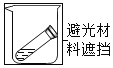
实验现象
6分钟出现浅红棕色
15分钟红棕色比较明显
30分钟红棕色非常明显
60分钟无明显变化
3分钟出现浅红棕色
6分钟红棕色比较明显
10分钟红棕色非常明显
(2)实验①、②对比是研究对浓硝酸稳定性的影响__________________________________。
(3)实验①、③对比可得出的结论是__________________________________________。
III.酸性
(查阅资料2)硝酸能够与金属氧化物反应生成盐和水。
(实验3)向氧化铜粉末中加入硝酸,能够观察到的现象是_________________________。
IV.氧化性
(查阅资料3)浓硝酸在加热条件下能与木炭发生反应。C+4HNO3(浓)
4NO2↑+ CO2↑+2H2O
(实验4)如图所示,将红热的木炭伸到浓硝酸上方,观察到有红棕色气体产生。请解释生成该红棕色气体的原因可能有:
①___________________________________________________。
②___________________________________________________。
九年级化学科学探究题困难题查看答案及解析
-
(2003•济南)在实验室里,硝酸银溶液通常保存在棕色瓶中,这是因为硝酸银很不稳定,在光照条件下易分解,生成银、二氧化氮和氧气.此反应的化学方程式是.
九年级化学填空题中等难度题查看答案及解析
-
在实验室里,硝酸银溶液通常保存在棕色瓶中,这是因为硝酸银很不稳定,在光照条件下易分解,生成银、二氧化氮和氧气.此反应的化学方程式是________.
九年级化学填空题中等难度题查看答案及解析
-
在实验室里,硝酸银溶液通常保存在棕色瓶中,这是因为硝酸银很不稳定,在光照条件下易分解,生成银、二氧化氮和氧气。写出此反应的化学方程式:________。
九年级化学信息分析题中等难度题查看答案及解析
-
硝酸(HNO3)是实验室常见的一种酸。实验小组对硝酸的某些性质进行研究。
Ⅰ.挥发性
(实验1)取一瓶质量分数为68%的浓硝酸,打开瓶盖,遇潮湿的空气,瓶口可以看到________,是由于挥发出来的硝酸蒸体遇到空气里的水蒸气形成硝酸小液滴的缘故。
Ⅱ.不稳定性
(查阅资料1)硝酸是无色液体,见光或受热分解生成红棕色的NO2气体。
(1)硝酸分解的化学方程式为:4HNO3
4NO₂↑+O₂↑+_____。
(实验2)取3份浓度和体积均相同的浓硝酸分别放入3支试管中,塞好塞子,放置在室外阳光充足的地方(气温为26℃)。记录溶液上方的气体颜色随时间的变化情况。
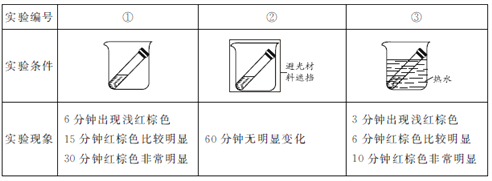
(2)实验①、②对比是研究______对浓硝酸稳定性的影响。
(3)实验①、③对比可得出的结论是_______。
Ⅲ.酸性
(查阅资料2)硝酸能够与金属氧化物反应生成盐和水。
(实验3)向氧化铜粉末中加入硝酸,能够看到的现象是_______。
IV .氧化性
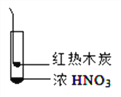
(查阅资料3) 浓硝酸在加热条件下能与木炭发生反应:C+4HNO₃(浓)
4NO₂↑+CO₂↑+2H2O。
(实验4)如图所示,将红热的木炭伸到浓硝酸上方,观察到有红棕色气体产生。请解释生成该红棕色气体的原因可能有________。
九年级化学科学探究题困难题查看答案及解析
-
(6分)请按照要求写出下列化学方程式。
(1)木炭还原氧化铜 ;
(2)实验室制取二氧化碳 ;
(3)在实验室里,硝酸银溶液通常保存在棕色瓶中,这是因为硝酸银很不稳定,在光照
的条件下易分解,生成银、二氧化氮和氧气。
此反应的化学方程式是 。
九年级化学填空题中等难度题查看答案及解析