-
化学小组同学对于“金属和硫酸反应的快慢与什么因素有关”的课题开展探究
[已有知识]
(1)根据金属的活动性顺序,只有排在氢(H)前面的金属才能与稀盐酸或稀硫酸反应制取氢气,且越靠________速率越快.
(2)实验室制取二氧化碳:当其他因素都相同时,稀盐酸与粉末状石灰石反应速度大于与块状石灰石速率,由此可知化学反应速率快慢与________有关.
[设计实验]下表是他们分别用相同质量的Fe丝和足量稀硫酸反应的三组实验数据:
(3)实验②和③表明:该反应快慢与________有关.实验编号 硫酸的质量分数/% 反应的温度 Fe丝消失的时间/S ① 3 20 500 ② 6 20 300 ③ 6 30 80
(4)如果实验②反应的温度改为25℃,请推出Fe丝消失的时间(用t表示)的取值范围________.
[归纳总结]影响金属和稀硫酸反应快慢的因素主要有:反应物的种类,金属颗粒大小,反应温度以及________等.
[拓展延伸]
(5)该实验除了用Fe丝消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量反应的快慢吗?方法:________
(6)金属除了能和酸反应外还能和其他金属的盐溶液反应,已知下列各组物质间均能发生置换反应.
A.Fe和CuSO4溶液 B.Mg和MnSO4溶液 C.Mn和FeSO4溶液
①写出Fe和CuSO4溶液反应的化学方程式________.
②Mn、Fe、Mg、Cu四种金属的活动性由弱到强的顺序________.九年级化学填空题中等难度题查看答案及解析
-
某课外小组的同学以“铁、铜、银的化学性质”为课题,进行科学探究活动,请根据已学知识完成下列探究问题。
【提出问题】铁、铜、银的金属活动性顺序是怎样的?
【猜想和假设】根据所学知识,猜想三种金属在金属活动顺序中的相对位置关系:
猜想一:Ag Fe Cu;
猜想二:Fe Cu Ag;
猜想三:__ _
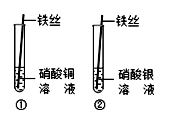
【制定计划】甲同学设计的实验如图所示。他们在实验中都进行了规范的操作和细致的观察。
【收集证据】你认为实验①中应观察到的现象是___________
【解释与结论】乙同学认为甲同学的实验设计有错误,其理由是______________
【反思】反思后甲同学对自己的实验进行了改正,其作法是__________________
由此证明了探究三者的金属活动性顺序活动中猜想_____________正确。
九年级化学探究题中等难度题查看答案及解析
-
某课外小组的同学以“铁、铜、银的化学性质”为课题,进行科学探究活动,请根据已学知识完成下列探究问题。
【提出问题】铁、铜、银的金属活动性顺序是怎样的?
【猜想和假设】根据所学知识,猜想三种金属在金属活动顺序中的相对位置关系:
猜想一:Ag Fe Cu;
猜想二:Fe Cu Ag;
猜想三:__ _
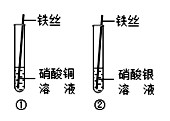
【制定计划】甲同学设计的实验如图所示。他们在实验中都进行了规范的操作和细致的观察。
【收集证据】你认为实验①中应观察到的现象是___________
【解释与结论】乙同学认为甲同学的实验设计有错误,其理由是______________
【反思】反思后甲同学对自己的实验进行了改正,其作法是__________________
由此证明了探究三者的金属活动性顺序活动中猜想_____________正确。
九年级化学探究题中等难度题查看答案及解析
-
某课外小组的同学以“铁、铜、银的化学性质”为课题,进行科学探究活动,请根据已学知识完成下列探究问题.
【提出问题】铁、铜、银的金属活动性顺序是怎样的?
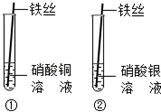
【制定计划】甲同学设计的实验如图所示.他们在实验中都进行了规范的操作和细致的观察.
【收集证据】你认为实验①中应观察到的现象是 ;
实验②中发生反应的化学方程式为 ;
【解释与结论】乙同学认为甲同学的实验设计有错误,其理由是 ;
【反思小结】反思后甲同学对自己的实验进行了改正只需将②中的 改为 就可证明了三者的金属活动性顺序是 .
九年级化学探究题中等难度题查看答案及解析
-
某课外小组的同学以“铁、铜、银的化学性质”为课题,进行科学探究活动,请根据已学知识完成下列探究问题.
【提出问题】铁、铜、银的金属活动性顺序是怎样的?
【制定计划】甲同学设计的实验如图所示.他们在实验中都进行了规范的操作和细致的观察.
【收集证据】你认为实验①中应观察到的现象是(1)________
【解释与结论】乙同学认为甲同学的实验设计有错误,其理由是(2)________
【反思揪】反思后甲同学对自己的实验进行了改正,其作法是(3)________
由此证明了三者的金属活动性顺序是(4)________.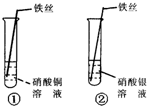
九年级化学填空题中等难度题查看答案及解析
-
金属锌与稀硫酸反应生成硫酸锌和氢气,化学课外小组的同学对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小组同学用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号
硫酸的质量分数
(均取20mL)
锌的形状
(均取1g)
氢气的体积(mL)
(均收集3分钟)
20%
锌粒
31.7
20%
锌片
50.9
30%
锌粒
61.7
30%
锌片
79.9
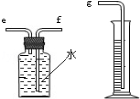
(1)小组同学用右图装置收集并测量氢气的体积,其中量筒的作用是 ,氢气应从 (填e或f或g)管通入。(已知:氢气难溶于水)
【收集证据】
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是 。
【得出结论】
(3)结论是 。
【评价与反思】
(4)下表是小组同学第①组实验的详细数据。
时段(均为1分钟)
第1分钟
第2分钟
第3分钟
第4分钟
第5分钟
第6分钟
H2的体积
3.1mL
16.7mL
11.9mL
9.6mL
7.6mL
6.0mL
请描述锌与硫酸反应快慢的变化 ,并解释第二分钟以后变化的原因 。
(5)锌与硫酸反应的快慢可能还受温度因素的影响,请设计实验验证 。
九年级化学实验题中等难度题查看答案及解析
-
金属锌与稀硫酸反应生成硫酸锌和氢气,化学课外小组的同学对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小组同学用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号
硫酸的质量分数
(均取20mL)
锌的形状
(均取1g)
氢气的体积(mL)
(均收集3分钟)
20%
锌粒
31.7
20%
锌片
50.9
30%
锌粒
61.7
30%
锌片
79.9
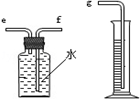
(1)小组同学用右图装置收集并测量氢气的体积,其中量筒的作用是________,氢气应从________(填e或f或g)管通入。(已知:氢气难溶于水)
【收集证据】
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是 ________。
【得出结论】
(3)结论是 ________。
【评价与反思】
(4)下表是小组同学第①组实验的详细数据。
时段(均为1分钟)
第1分钟
第2分钟
第3分钟
第4分钟
第5分钟
第6分钟
H2的体积
3.1mL
16.7mL
11.9mL
9.6mL
7.6mL
6.0mL
请描述锌与硫酸反应快慢的变化________,并解释第二分钟以后变化的原因________。
(5)锌与硫酸反应的快慢可能还受温度因素的影响,请设计实验验证________。
九年级化学探究题中等难度题查看答案及解析
-
金属锌与稀硫酸反应生成硫酸锌和氢气,化学课外小组的同学对“锌与硫酸反应快慢的影响因素”进行了探究。
(提出问题)锌与硫酸反应的快慢受哪些因素的影响呢?
(猜想与假设)a.可能与稀硫酸的浓度有关;b.可能与锌的形状有关。
(设计并实验)小组同学用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号
稀硫酸的浓度(均取20mL)
锌的形状(均取1g)
氢气的体积(mL)(均收集3分钟)
①
20%
锌粒
31.7
②
20%
锌片
50.9
③
30%
锌粒
61.7
④
30%
锌片
79.9
(1)锌与稀硫酸反应的化学方程式为_____。
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是_____。
(3)利用如图装置进行实验时,为了较准确的测量氢气的体积,在读取量气管中液面读数的过程中,应注意_____(填字母编号)。
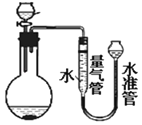
A.读数时视线与凹液面最低处相平。
B.保持水准管静止,待水准管中液面不再上升时再读数。
C.读数前应上下移动水准管,待两管液面相平再读数。
通过上述实验,你得出的结论是硫酸的质量分数越大,反应速率越快。锌与硫酸的接触面积越大,反应速率越快
(4)发生装置中留有氢气,是否会影响实验最终结果_____(填“是”或“否”)。
(5)下表是小组同学第①组实验的详细数据。
时段(均为1分钟)
第1分钟
第2分钟
第4分钟
第3分钟
第5分钟
第6分钟
H2的体积
3.1mL
16.7mL
9.6mL
11.9mL
7.6mL
6.0mL
解释第二分钟以后变化的原因_____。
九年级化学科学探究题困难题查看答案及解析
-
某同学选择“金属和酸反应的快慢与什么因素有关”的课题开展探究.下表是他们分别用接触面积、质量相同的金属丝和足量稀酸反应的三组实验数据:
实验编号
反应物
酸的质量分数%
反应的温度℃
金属丝消失的时间s
①
铝丝和稀盐酸
5
20
450
②
铝丝和稀盐酸
10
20
240
③
铝丝和稀盐酸
10
30
65
④
铁丝和稀盐酸
10
30
125
⑤
铝丝和稀硫酸
10
30
超过1000
(1)实验开始前都需要用砂纸充分打磨金属,目的是:
(2)对比试验 可知,金属和酸反应的快慢还与金属的种类有关.
(3)本通过测量 来反应金属和酸反应的快慢.
(4)通过比较实验①和②可得出实验结论: .
九年级化学填空题简单题查看答案及解析
-
某同学选择“金属和酸反应的快慢与什么因素有关”的课题开展探究.下表是他们分别用相同质量的金属丝和足量稀酸反应的三组实验数据:
(1)写出铝丝和稀盐酸反应的方程式______.实验编号 反应物 酸的质量分数% 反应的温度℃ 金属丝消失的时间s ① 铝丝和稀盐酸 5 20 450 ② 铝丝和稀盐酸 10 20 240 ③ 铝丝和稀盐酸 10 30 65 ④ 铁丝和稀盐酸 10 30 125 ⑤ 铝丝和稀硫酸 10 30 超过1000
(2)如果实验②中反应温度改为25℃,请推出铝丝消失的时间(用t表示)的取值范围是______.
(3)对比试验①和②可知,金属和酸反应的快慢与______有关,对比试验______和______可知,金属和酸反应的快慢还与金属的种类有关.
(4)通过对表中①至④的数据分析还有另外一种因素对金属和酸反应的快慢也有影响,其影响情况为______.
(5)对比实验③和⑤,某同学认为发现问题,为什么铝丝易与稀盐酸反应而难与稀硫酸反应.他大胆提出假设______.九年级化学解答题中等难度题查看答案及解析