-
材料是人类赖以生存和发展的重要物质,铜是目前使用最广泛的金属之一。
(一)铜材料的有关知识
(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是________。
(2)纯铜又称紫铜,常见铜合金有黄铜、青铜等种类。家用电缆常用紫铜,以聚氯乙烯塑料或TPU橡胶包裹。
① 以上叙述中不涉及到的材料是_______(选填序号)。
A.金属材料 B.无机非金属材料 C.有机合成材料
② 我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理_______。
③ 鉴别黄铜和黄金,以下方法不可行的是______(选填序号)。
A.观察颜色 B.加稀盐酸 C.在空气中灼烧
(二)铜及其化合物的实验
I.硫酸铜是制备其他含铜化合物的重要原料,以下是制取硫酸铜的常见方法。
(1)方案1:向稀硫酸中加入铜粉,再用导管通入空气并加热,铜粉逐渐减少,溶液由无色变为蓝色。
①反应中溶液的PH逐渐_________(填“增大”或“减小”)。
②该反应的化学方程式_________。
(2)方案2:将铜片加入浓硫酸中,加热,产生刺激性气味,溶液逐渐变成蓝色。将产生的气体通入酸性高锰酸钾溶液中,溶液褪色,说明该气体是________。
(3)从环保角度进行比较,你认为方案_______(填“1”或“2”)更合理。
Ⅱ.在一定量硫酸铜溶液中加入碳酸钠溶液,过滤、洗涤、低温干燥得到碱式碳酸铜固体,其组成为:xCuCO3·yCu(OH)2·zH2O。能证明固体已洗净的方法为__________。
(三)碱式碳酸铜的热分解实验
兴趣小组称取此固体12.0g,在科研人员的指导下用下图装置进行热分解实验。
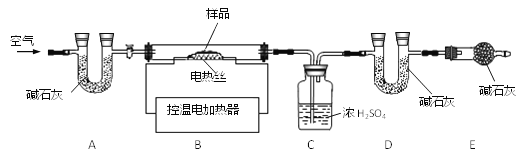
【查阅资料】Cu(OH)2的分解温度为66℃~68℃,CuCO3的分解温度为200℃~220℃,各生成对应的两种氧化物。该碱式碳酸铜失去结晶水的温度与Cu(OH)2的分解温度接近。
(1)装置A的作用是___________。
(2)加热前后及过程中均通入空气,加热后通空气的目的是________。
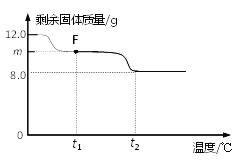
(3)控制温度在不同的范围对B中样品加热。测得装置C、D的质量在实验前后的变化情况如下表所示,测得B中剩余固体质量随温度的变化如下图所示。
| 装置 | 实验前/g | 实验后/g |
| C | 198.0 | 199.8 |
| D | 221.0 | 223.2 |
①图中F点对应的m=__________。
② 根据提供的数据, xCuCO3·yCu(OH)2·zH2O中x ﹕y ﹕z = _________。
③ 若缺少装置E,测得的________(选填“x”、“y”、“z”)的值会偏大。
-
材料是人类赖以生存和发展的重要物质,铜是目前使用最广泛的金属之一。
(一)铜材料的有关知识
(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是________。
(2)纯铜又称紫铜,常见铜合金有黄铜、青铜等种类。家用电缆常用紫铜,以聚氯乙烯塑料或TPU橡胶包裹。
① 以上叙述中不涉及到的材料是_______(选填序号)。
A.金属材料 B.无机非金属材料 C.有机合成材料
② 我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理_______。
③ 鉴别黄铜和黄金,以下方法不可行的是______(选填序号)。
A.观察颜色 B.加稀盐酸 C.在空气中灼烧
(二)铜及其化合物的实验
I.硫酸铜是制备其他含铜化合物的重要原料,以下是制取硫酸铜的常见方法。
(1)方案1:向稀硫酸中加入铜粉,再用导管通入空气并加热,铜粉逐渐减少,溶液由无色变为蓝色。
①反应中溶液的PH逐渐_________(填“增大”或“减小”)。
②该反应的化学方程式_________。
(2)方案2:将铜片加入浓硫酸中,加热,产生刺激性气味,溶液逐渐变成蓝色。将产生的气体通入酸性高锰酸钾溶液中,溶液褪色,说明该气体是________。
(3)从环保角度进行比较,你认为方案_______(填“1”或“2”)更合理。
Ⅱ.在一定量硫酸铜溶液中加入碳酸钠溶液,过滤、洗涤、低温干燥得到碱式碳酸铜固体,其组成为:xCuCO3·yCu(OH)2·zH2O。能证明固体已洗净的方法为__________。
(三)碱式碳酸铜的热分解实验
兴趣小组称取此固体12.0g,在科研人员的指导下用下图装置进行热分解实验。
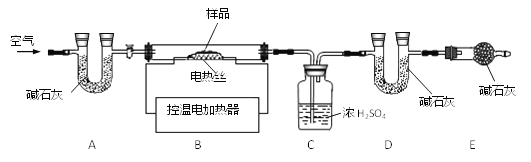
【查阅资料】Cu(OH)2的分解温度为66℃~68℃,CuCO3的分解温度为200℃~220℃,各生成对应的两种氧化物。该碱式碳酸铜失去结晶水的温度与Cu(OH)2的分解温度接近。
(1)装置A的作用是___________。
(2)加热前后及过程中均通入空气,加热后通空气的目的是________。
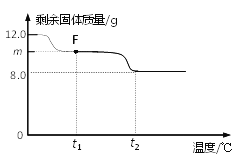
(3)控制温度在不同的范围对B中样品加热。测得装置C、D的质量在实验前后的变化情况如下表所示,测得B中剩余固体质量随温度的变化如下图所示。
| 装置 | 实验前/g | 实验后/g |
| C | 198.0 | 199.8 |
| D | 221.0 | 223.2 |
①图中F点对应的m=__________。
② 根据提供的数据, xCuCO3·yCu(OH)2·zH2O中x ﹕y ﹕z = _________。
③ 若缺少装置E,测得的________(选填“x”、“y”、“z”)的值会偏大。
-
材料是人类赖以生存和发展的重要物质,目前使用量最多的金属材料仍然是钢铁。
(一)铁材料的有关知识
(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料.
这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是____________________.
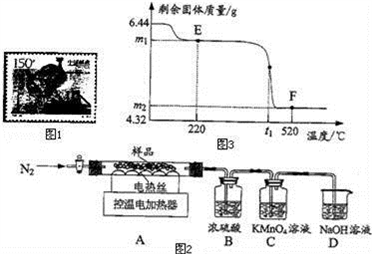
(2)钢铁材料通常分为生铁和钢.如图1是我国1997年发行的纪念钢产量首次突破1亿吨的邮票.邮票通常密封保存在聚乙烯塑料袋中
①以上叙述中不涉及到的材料是_________________(选填序号).
A.合金 B.无机非金属材料 C.有机合成材料
②以赤铁矿为原料冶炼铁反应的化学方程式 _________________________________________。
③钢铁露置在空气中易生锈,请提出防止其生锈的一种措施____________________.
(二)铁及其化合物的实验
(3)将Fe粉溶于稀H2SO4,此反应属于_____(填基本反应类型).用点燃法检验生成的H2前必须______.
(4)向上述反应后的溶液中滴加NaOH溶液,生成白色Fe(OH)2沉淀,随后沉淀变为灰绿色.
①生成Fe(OH)2反应的化学方程式_______________________________.
②白色沉淀变为灰绿色的原因之一是部分Fe(OH)2接触空气生成Fe(OH)3,反应的化学方程式_____________.生成的Fe(OH)3分解为Fe2O3.
③过滤、洗涤、低温干燥得到灰绿色固体,其组成为2FeSO4•2Fe(OH)2•Fe2O3〔相对分子质量为644].能证明固体已洗净的方法为__________________________________.
(三)灰绿色固体的热分解实验
兴趣小组称取此固体6.44g,在科研人员的指导下用如图2装置进行热分解实验.
[查阅资料]
①Fe(OH)2在150℃~200℃时完全分解为FeO;
②FeSO4在450℃~500℃时完全分解为Fe2O3,2FeSO4 Fe2O3+SO2↑+SO3↑.
Fe2O3+SO2↑+SO3↑.
(5)加热前后及过程中均通入N2,加热前通N2的目的是_____________________________.
(6)控制温度在不同的范围对A中样品加热,测得剩余固体质量随温度的变化如图3所示.B装置中浓硫酸只能吸收SO3和H2O,当加热到t1℃时,装置C中的现象为______________.
①图3中E点对应的m1= ______________.
②图3中F点对应物质中Fe2O3的质量为__g.
③科研人员将F点所得剩余固体隔绝空气,在密闭容器中加热到1400℃,得到纯净的磁性Fe3O4.已知加热过程中发生两个反应,且反应前后固体总质量不变.请写出其中一个反应的化学方程式______________________.
-
人类的生活和生产都离不开金属材料。
(一)铁材料的有关知识
(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是_________。
(2)下列说法不正确的是________________。(填字母序号)
A.铁丝在氧气中剧烈燃烧,火星四射,生成氧化铁;
B.回收废旧金属有利于节约金属资源;
C.在铁桶中加入硫酸铜溶液和石灰乳来配制农药波尔多液。
D.铁锅常用于炒饭炒菜,是利用了铁的导热性
铁制品锈蚀的过程,实际上是铁与空气中的_____________________等发生化学反应的过程。请写出一种防锈措施 __________________________________。
(二)请你参与探究几种常见金属饰品所含金属的相关活动,并回答下列问题。
现用一定量的AgNO3和Cu(NO3)2混合溶液,进行了如右图所示的实验,并对溶液A和固体B的成分进行了分析和研究。
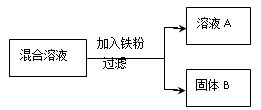
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】
①只有Fe(NO3)2 ②有Fe(NO3)2 、AgNO3
③有Fe(NO3)2 、Cu(NO3)2 ④有___________________________。
【交流讨论】不合理的猜想是_______________(填标号)。
【实验探究】根据下表中的实验步骤及现象,完成表中的实验结论
| 实 验步骤 验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加稀盐酸 | 有气泡产生 | 溶液A中的溶质成分符合猜想____________, 固体B中的金属成分为____________(写化学式)。 |
【数据处理】称取10克固体B于烧杯中,向烧杯中加入100克稀硫酸,恰好完全反应后称得烧杯内混合物的总质量为109.8克。请计算
(1)所用稀硫酸的溶质质量分数为多少?(请写出计算过程)
______
(2)若配制上述浓度的稀硫酸100克,则需质量分数98%的浓硫酸______克。
-
铁及其化合物在生活生产中应用非常广泛。
(一)铁材料的有关知识

(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、 Al三种金属的活动性由强到弱的顺序是_______________。
(2)磁铁矿是早期司南(如图)的材料,磁铁矿中所含铁的氧化物主要是________________。
(3)我国C919大型客机去年惊艳亮相,客机上大规模使用碳纤维复合材料、铝锂合金、铁钛合金、纳米陶瓷等先进材料,其中不涉及到的材料是_________(选填序号)。
A 合金
B 无机非金属材料
C 合成材料
D 复合材料
(4)铁矿石有赤铁矿、磁铁矿、黄铁矿(FeS2)等。工业上用黄铁矿制取硫酸而不用于炼铁,不用于炼铁原因是:①冶炼中产生SO2污染环境;②______________。
(二)制取碱式硫酸铁
碱式硫酸铁是-种废水处理剂,用硫酸厂的废渣(主要成分为铁的氧化物、少量FeS及SiO2)制备碱式硫酸铁晶体[Fe4(OH)2(SO4)5·6H2O]主要流程如下:
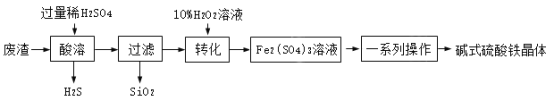
(1)废渣应研磨成粉末,目的是_____。
(2)“酸溶”过程中生成H2S气体的化学方程式为________
(3)过滤后洗涤,证明固体已洗净的方法是_______。
(4)“转化”发生反应的化学方程式为_______,该反应温度不宜过高的原因是________。
(三)碱式硫酸铁晶体的热分解实验
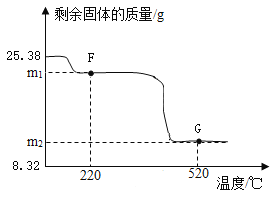
兴趣小组称取此晶体样品25.38g,在科研人员的指导下用下图装置进行热分解实验。
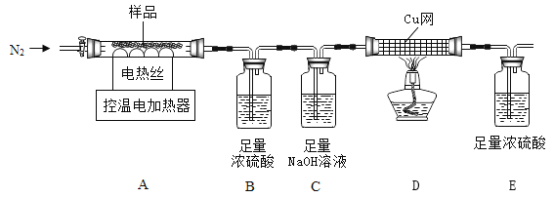
[查阅资料]①碱式硫酸铁晶体(相对分子质量为846)200°C完全分解生成Fe2O3、H2O和Fe2(SO4)3;
②Fe2(SO4)3在500°C完全分解为Fe2O3、SO2、SO3和O2;
③B装置中浓硫酸只能吸收SO3和H2O。.
(1)装配好实验装置后,先要_________。
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是防止倒吸和______。
(3)控制不同的温度对A中固体加热,测得装置B、C和D中的质量变化如下表,测得剩余固体质量随温度的变化如图所示。
| 温度/C | 室温 | 220 | 520 |
| B装置/g | 200.00 | 203.78 | 207.78 |
| C装置/g | 200.00 | 200.00 | x |
| D装置/g | 100.00 | 100.00 | 101.60 |
①如图中m1=____________。
②表格中x=_____________。
③将最终的剩余固体继续加热到更高的温度,发现固体减少0.32g后质量不再改变,写出此过程中发生反应的化学方程式____________。
-
(一)铁材料的有关知识
(1)人类使用金属先后经历了“青铜”、“铁器”时代,到近代才开始大量使用铝材料.这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是_____.
(2)在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理_____.
(3)钢铁露置在空气中易生锈,写出一种防止钢铁生锈的方法_____.
以下是同学对铁锈的成分、铁锈制草酸亚铁晶体及草酸亚铁晶体热分解的研究.
(二)用上述铁锈制草酸亚铁晶体(FeC2O4·nH2O)
资料:①FeSO4遇到氧气氧化,会转化为Fe2(SO4)3.
②FeSO4的溶解度如下表:
| 温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
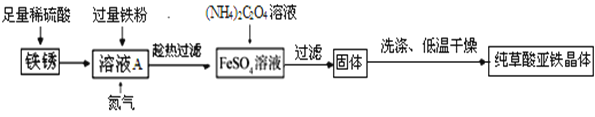
(制备流程)
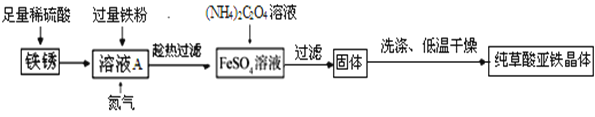
(1)溶液加入过量铁粉,发生的反应有:Fe+Fe2(SO4)3=3FeSO4、_____.充分反应后要趁热过滤的目的是_____.
(2)流程中产生草酸亚铁晶体反应的化学方程式为_____.
(3)制备过程中,溶液中通入氮气的作用是_____.
(三)探究FeC2O4·nH2O热分解的产物及n的值
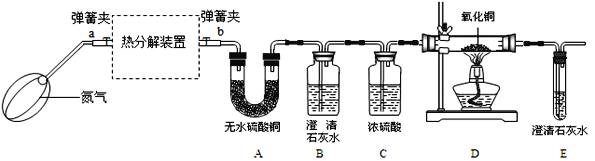
(实验装置)
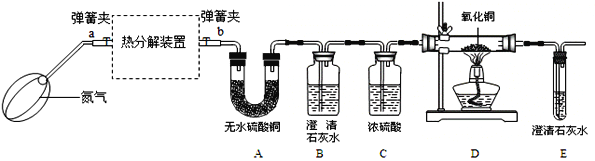
资料:①FeC2O4·nH2O为淡黄色粉末;FeO和Fe3O4都是黑色固体,其中FeO易被氧气氧化.
②FeC2O4·nH2O加热至300℃完全失去结晶水;继续加热至400℃,剩余固体受热分解产生黑色固体、CO2和CO.
(实验分析)
(1)若通过E装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解产生CO,则需在B和C装置之间增加盛有_____(填试剂名称)的洗气瓶.
(2)先鼓入氮气,再加热分解装置的原因是_____.
(3)指出上述实验装置不足之处_____.
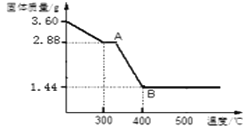
(4)取3.60gFeC2O4·nH2O,按上述实验步骤进行实验,测得热分解装置中固体质量随温度变化曲线如下图所示:
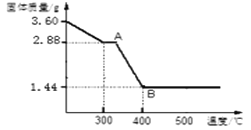
①FeC2O4·nH2O中n的值为_____.
②反应后,热分解装置中残留的黑色物质为_____(填化学式).
③草酸亚铁晶体受热分解的方程式为_____.
④若将图中1.44g固体在空气中充分加热,固体增加0.16g,此固体(铁的氧化物)为_____。
-
(一)铁材料的有关知识
(1)人类使用金属先后经历了“青铜”、“铁器”时代,到近代才开始大量使用铝材料.这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是_____.
(2)在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理_____.
(3)钢铁露置在空气中易生锈,写出一种防止钢铁生锈的方法_____.
以下是同学对铁锈的成分、铁锈制草酸亚铁晶体及草酸亚铁晶体热分解的研究.
(二)用上述铁锈制草酸亚铁晶体(FeC2O4·nH2O)
资料:①FeSO4遇到氧气氧化,会转化为Fe2(SO4)3.
②FeSO4的溶解度如下表:
| 温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
(制备流程)
(1)溶液加入过量铁粉,发生的反应有:Fe+Fe2(SO4)3=3FeSO4、_____.充分反应后要趁热过滤的目的是_____.
(2)流程中产生草酸亚铁晶体反应的化学方程式为_____.
(3)制备过程中,溶液中通入氮气的作用是_____.
(三)探究FeC2O4·nH2O热分解的产物及n的值
(实验装置)
资料:①FeC2O4·nH2O为淡黄色粉末;FeO和Fe3O4都是黑色固体,其中FeO易被氧气氧化.
②FeC2O4·nH2O加热至300℃完全失去结晶水;继续加热至400℃,剩余固体受热分解产生黑色固体、CO2和CO.
(实验分析)
(1)若通过E装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解产生CO,则需在B和C装置之间增加盛有_____(填试剂名称)的洗气瓶.
(2)先鼓入氮气,再加热分解装置的原因是_____.
(3)指出上述实验装置不足之处_____.
(4)取3.60gFeC2O4·nH2O,按上述实验步骤进行实验,测得热分解装置中固体质量随温度变化曲线如下图所示:
①FeC2O4·nH2O中n的值为_____.
②反应后,热分解装置中残留的黑色物质为_____(填化学式).
③草酸亚铁晶体受热分解的方程式为_____.
④若将图中1.44g固体在空气中充分加热,固体增加0.16g,此固体(铁的氧化物)为_____。
-
(2006•泰州)人类利用金属的历史经历了从青铜器时代到铁器时代,再到铝合金大量使用的过程.这一事实与下列因素有关的是( )
| A.地壳中金属元素的含量 | B.金属的导电性、延展性 |
| C.金属的活动性 | D.金属冶炼的水平 |
-
人类利用金属的历史经历了从青铜器时代到铁器时代,再到铝合金大量使用的过程.这一事实与下列因素有关的是( )
A.地壳中金属元素的含量 B.金属的导电性、延展性
C.金属的活动性 D.金属冶炼的水平
-
人类利用金属的历史经历了从青铜器时代到铁器时代,再到铝合金大量使用的过程.这一事实与下列因素有关的是( )
A.地壳中金属元素的含量
B.金属的导电性、延展性
C.金属的活动性
D.金属冶炼的水平















