-
钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2.4H2O],煅烧可获得钛酸钡粉体。

(1)BaTiO3中Ti元素的化合价是_____。
(2)“酸浸”过程中发生反应的化学方程式为_____。
(3)“操作A”的名称是_____。
(4)“绿色化学”理念提倡循环利用,流程中能循环使用的物质是_____。
(5)现有394kg BaCO3,理论上可以制备BaTiO3的质量为_____kg.( BaTiO3的相对分子质量为233,BaCO3的相对分子质量为197)
-
钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2.4H2O],煅烧可获得钛酸钡粉体。
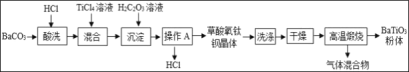
(1)BaTiO3中Ti元素的化合价是_____。
(2)“酸浸”过程中发生反应的化学方程式为_____。
(3)“操作A”的名称是_____。
(4)“绿色化学”理念提倡循环利用,流程中能循环使用的物质是_____。
(5)现有394kg BaCO3,理论上可以制备BaTiO3的质量为_____kg.( BaTiO3的相对分子质量为233,BaCO3的相对分子质量为197)
-
钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2.4H2O],煅烧可获得钛酸钡粉体。
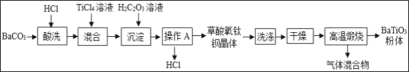
(1)BaTiO3中Ti元素的化合价是_____。
(2)“酸浸”过程中发生反应的化学方程式为_____。
(3)“操作A”的名称是_____。
(4)“绿色化学”理念提倡循环利用,流程中能循环使用的物质是_____。
(5)现有394kg BaCO3,理论上可以制备BaTiO3的质量为_____kg.( BaTiO3的相对分子质量为233,BaCO3的相对分子质量为197)
-
钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2.4H2O],煅烧可获得钛酸钡粉体。
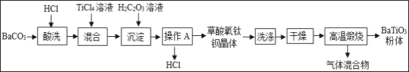
(1)BaTiO3中Ti元素的化合价是_____。
(2)“酸浸”过程中发生反应的化学方程式为_____。
(3)“操作A”的名称是_____。
(4)“绿色化学”理念提倡循环利用,流程中能循环使用的物质是_____。
(5)现有394kg BaCO3,理论上可以制备BaTiO3的质量为_____kg.( BaTiO3的相对分子质量为233,BaCO3的相对分子质量为197)
-
草酸钙(Ca C2O4)是不能被人体吸收的沉淀物,豆腐中含有较多的钙盐【硫酸钙(CaSO4)等】,波菜、洋葱、竹笋中含有丰富的草酸(H2C2O4),草酸钠(Na2 C2O4)。豆腐和上述几种蔬菜混合食用,可能诱发“结石症”。
(1)由草酸的化学式可知,其中碳元素的化合价是____。
(2)草酸与硫酸钙反应的化学方程式为:H2C2O4+ CaSO4= Ca C2O4↓+ H2 SO4,
请写出草酸钠与硫酸钙反应生成草酸钙和硫酸钠(Na2 SO4)的化学方程式: _________________。
-
草酸亚铁晶体是一种淡黄色晶体粉末,常用于照相显影剂及制药工业,是电池材料的制备原料.

草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO4足量):
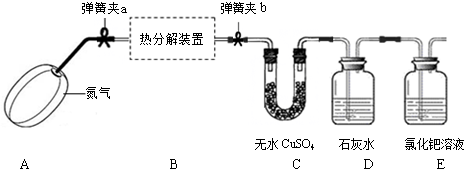
【实验步骤】:
①连接好装置,______;
②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④______,用酒精灯加热热分解装置,直至晶体完全变成黑色,停止加热;
⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
| 装置B的质量(/g) | 装置C的质量(/g) |
| 实验前 | 145.8 | 168.2 |
| 实验后 | 140.4 | 170.0 |
| 热分解装置质量为136.8g |
【实验分析及数据处理】:
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了______,FeC2O4•xH2O中x的值为______;
(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了______;
(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了______;
(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(提示:相对分子质量分别为FeC2O4:144; H2O:18)
______;
(5)实验过程中,鼓入氮气的目的是______;
(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式______;
【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁.你认为这种说法是否正确?请说出可能的理由______;
(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么?______;
(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式______.
-
(14分)草酸亚铁晶体(化学组成为FeC2O4·xH2O)是一种淡黄色晶体粉末,常用于照相显影剂及制药工业,是电池材料的制备原料.

5、铁的氧化物被CO还原所需的温度:

草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO4足量):
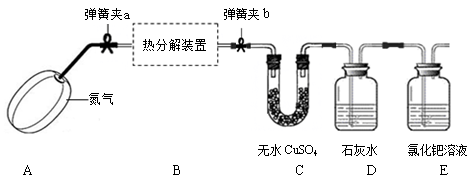
【实验步骤】:
①连接好装置,▲ ;
②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④▲ ,用酒精灯加热热分解装置,直至晶体完全变成黑色,停止加热;
⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
| 装置B的质量(/g) | 装置C的质量(/g) |
| 实验前 | 145.8 | 168.2 |
| 实验后 | 140.4 | 170.0 |
| 热分解装置质量为136.8g |
【实验分析及数据处理】:
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了▲ ,FeC2O4·xH2O中x的值为▲ ;
(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了▲ ;
(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了▲ ;
(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(3分)
(提示:相对分子质量分别为FeC2O4:144; H2O:18)▲ ;
(5)实验过程中,鼓入氮气的目的是▲ ;
(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式▲ ;
【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁。你认为这种说法是否正确?请说出可能的理由▲ ;
(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么?▲ ;
(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式▲ .
-
草酸晶体是重要的有机试剂,其化学式为H2C2O4•2H2O.某研究性学习小组进行以下的猜想:
若加热完全分【解析】
A、只生成CO2、H2O;B、只生成CO、H2O;C、可生成CO、CO2、H2O.请应用所学的化学原理分析以上三种猜想的正确性:
(1)______(填“A”或“B”或“C”)是合理猜想,根据是______.
(2)写出草酸晶体加热完全分解的合理化学方程式(要配平)______ CO2↑+CO↑+3H2O
-
工业铁红主要成分是Fe2O3,还含有少量的FeO、Fe3O4
(查阅资料)(1)草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O4•3H2O  CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
(2)碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
(3)铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
(问题讨论)为了测定铁红中铁的质量分数,小组间进行如下实验。(装置气密性良好)

(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是________(填字母序号)
a.浓硫酸 b.澄清的石灰水 c氢氧化钠溶液
(2)C装置的作用是 __________________________。
(3)写出E装置中所发生反应的一个化学方程式: _____________________。
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①若E中充分反应后得到铁粉的质量为mg,则 ____ < m < ______。
②若实验前后称得F装置増重7.7g,则此铁红中铁的质量分数是 _________。
(实验反思) (1)如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会 ________(选填“偏小”“不变”“偏大”)。
(2)该实验装置的一个明显缺陷是 ___________________。
-
工业铁红主要成分是Fe2O3,还含有少量的FeO、Fe3O4
【查阅资料】(1)草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O4•3H2O  CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
(2)碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
(3)铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
【问题讨论】为了测定铁红中铁的质量分数,小组间进行如下实验。(装置气密性良好)
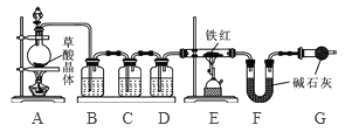
(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是________(填字母序号)
a.浓硫酸 b.澄清的石灰水 c氢氧化钠溶液
(2)C装置的作用是 __________________________。
(3)写出E装置中所发生反应的一个化学方程式: _____________________。
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①若E中充分反应后得到铁粉的质量为mg,则 ____ < m < ______。
②若实验前后称得F装置増重7.7g,则此铁红中铁的质量分数是 _________。
【实验反思】 (1)如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会 ________(选填“偏小”“不变”“偏大”)。
(2)该实验装置的一个明显缺陷是 ___________________。









