-
锰是治炼工业中常用的添加剂。以碳酸锰矿(主要成分为MnCO3,还含有 FeCO3、NiCO3等杂质)为原料生产金属锰的工艺流程如下图,请回答以下问题:
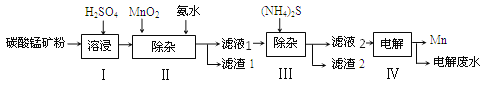
(1)步骤Ⅰ中,将碳酸锰矿研磨成粉末的主要目的是_______,其中碳酸锰与硫酸反应的化学方程式为_________________。
(2)步骤Ⅱ中,先加入二氧化锰发生以下反应:MnO2+2FeSO4+2H2SO4=MnSO4+2H2O+x,x的化学式为______;已知滤液1中的主要溶质为MnSO4同时还含有少量NiSO4,则步骤Ⅱ中加入氨水的主要目的是________。
(3)步骤Ⅲ中,所得滤液2中含有的溶质为MnSO4、(NH4)2SO4,则滤渣2中主要成分为______(填化学式)
(4)步骤Ⅳ中,电解后的废液中还含有Mn2+,常用石灰乳进行一级沉降得到沉淀Mn(OH)2和氨气,过滤后,再向滤液中加入Na2S进行二级沉降得到沉淀MnS。写出二级沉降过程中发生的化学反应方程式:___________________;沉降过程的产物中,______________________可循环利用于上述流程。
-
工业上用菱锰矿[主要成分为MnCO3,含FeCO3、Cu2(OH)2CO3、SiO2等杂质]为原料来制取二氧化锰,其生产流程示意图如下:

回答下列问题:
(1)加盐酸之前,需要将菱锰矿粉碎,目的是________
(2)操作②是______,此操作过程中用的玻璃仪器有玻璃棒、______、 _______,其中玻璃棒的作用是________。
(3)向菱锰矿中加入盐酸,MnCO3、FeCO3、Cu2(OH)2CO3都溶解并转化为MnCl2、FeCl2、CuCl2。盐酸与MnCO3反应的化学方程式为_______________。滤渣1主要成分是二氧化硅,需要洗涤,洗涤的目的是________________,可以通过在最后一次洗涤液中滴加________(填化学式)溶液,若无明显现象,则已洗涤干净。
(4)加入双氧水将铁元素转化为Fe(OH)3沉淀,其反应为:2FeCl2 + H2O2 + 4H2O = 2Fe(OH)3↓ + 4HCl,该反应化合价发生变化的元素是氧和________(填元素名称)。
(5)加入Na2S、MnS等硫化物,均可将MnCl2中混有的CuCl2转化为CuS沉淀除去,但实际生产中选用MnS,其原因是________。
-
工业上用菱锰矿[主要成分为MnCO3,含FeCO3、Cu2(OH)2CO3、SiO2等杂质]为原料来制取二氧化锰,其生产流程示意图如下:
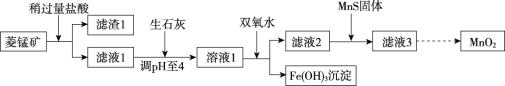
回答下列问题:
(1)将滤液与滤渣分离的操作是______。
(2)向菱锰矿中加入盐酸,MnCO3、FeCO3、Cu2(OH)2CO3都溶解并转化为MnCl2、FeCl2、CuCl2。盐酸与MnCO3反应的化学方程式为________。
(3)加入生石灰将溶液pH调至4,此时溶液呈________(填“酸性”或“碱性”)。
(4)加入双氧水将铁元素转化为Fe(OH)3沉淀,其反应为: 2FeCl2 + H2O2 + 4H2O = 2Fe(OH)3↓ + 4HCl,该反应化合价发生变化的元素是氧和_______。
(5)加入Na2S、MnS等硫化物,均可将MnCl2中混有的CuCl2转化为CuS沉淀除去,但实际生产中选用MnS,其原因是________。
-
碳酸锂作为锂的基础锂盐,广泛用于玻璃制造和陶瓷生产过程中的添加剂,也是制备锂电池的重要原料。碳酸锂在热水中的溶解度很小,工业上以锂辉石精矿(主要成分是Li2O、含有Al2O3、SiO2等杂质)为原料制取碳酸锂的硫酸法生产工艺流程如下

(1)锂辉石热酸浸提前要进行“研磨”,其目的是_____
(2)“水浸”中加入CaCO3的作用之一是为了调节pH=5,让溶液中的Al3+变成Al(OH)3沉淀出来,要确定溶液的pH值为5,可以用pH试纸来测定,其操作方法是_____
(3)“沉锂”中加入的Na2CO3溶液是饱和溶液,其作用是_____,反应的化学方程式为_____
(4)“洗涤”中使用热水,原因是_____,证明洗涤干净的方法是_____
(5)为了探究热酸浸提的最佳条件,将矿石在一定条件下酸浸4小时,锂元素浸出率的数据如下表
| 编号 | 矿酸比 | 硫酸浓度(%) | MgSO4用量(g) | 温度(℃) | 锂元素浸出率(%) |
| 1 | 1:1 | 90 | 0.00 | 100 | 70.34 |
| 2 | 1:1 | 98 | 0.00 | 100 | 73.89 |
| 3 | 1:1 | 98 | 0.00 | 150 | 78.24 |
| 4 | 1:3 | 98 | 0.00 | 200 | 85.53 |
| 5 | 1:3 | 98 | 1.25 | 250 | 90.26 |
| 6 | 1:3 | 98 | 2.50 | 250 | 95.88 |
①本实验中,编号为_____两组实验能说明温度对锂元素浸出率的影响
②根据上表数据,MgSO4用量对锂元素浸出率的影响是_____
③在工业生产过程中,相当数量的硫酸和纯碱变成了价值较低的Na2SO4等物质,从而造成了生产成本的提高,为了降低生产成本,除了尽可能减少硫酸的配量外,降低能源消耗也是一个方面,因此,可以继续设计实验,以探究出最佳锂元素浸提工艺条件,下列设计合理的是_____(填字母)
A 矿酸比1:2,硫酸浓度98,MgSO4用量0.00,温度150℃
B 矿酸比1:2,硫酸浓度98,MgSO4用量1.25,温度200℃
C 矿酸比1:2,硫酸浓度98,MgSO4用量2.50,温度200℃
D 矿酸比1:2,硫酸浓度98,MgSO4用量2.50,温度250℃
-
碳酸锰(MnCO3)是一种高性能磁性材料。以软锰矿粉(主要含MnO2,还含有少量的Fe2O3、Al2O3等杂质)为原料制取MnCO3的流程如下:
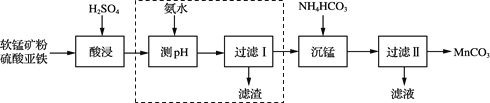
已知“沉锰”反应为MnSO4+2NH4HCO3===(NH4)2SO4+MnCO3↓+H2O+CO2↑
(1)“酸浸”时发生的主要反应为2FeSO4+MnO2+2H2SO4===X+MnSO4 +2H2O,X的化学式为______;“酸浸”时还发生的反应有______(任写一个化学方程式)。
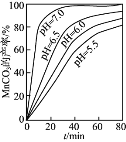
(2)流程中虚线内工序的主要目的是______。“沉锰”工序中,如图为MnCO3的产率与溶液pH、反应时间t的关系,由图可知应控制溶液的pH 为______。
(3)“过滤Ⅱ”后续的操作为洗涤、干燥,证明MnCO3固体已经洗涤干净的操作是______。
-
碳酸锂作为锂的基础锂盐,广泛用于玻璃制造和陶瓷生成过程中的添加剂,也是制备锂电池的重要原料。碳酸锂在热水中的溶解度很小,工业上以锂辉石精矿(主要成分是Li2O,含有Al2O3、SiO2 等杂质)为原料制取碳酸锂,其“硫酸法”生产工艺流程如下图所示。请回答问题:

(1)锂辉石热酸浸提前要进行“研磨”,其目的是_____。
(2)“水浸”中加入CaCO3的作用之一是为了调节pH=5,让溶液中的Ai3+变成Al(OH)3沉淀出来,要确定溶液的pH为5,可以使用pH试纸来测定。其操作方法是_____。
(3)“沉锂 ”中要加入的Na2CO3溶液是饱和溶液,其作用是_____,反应化学方程式为_____。
(4)“洗涤”中使用热水,原因是_____。证明Li2CO3洗涤干净的方法是_____。(写操作,现象和结论)
-
碳元素是组成许多物质的基本元素。
(1)化石燃料主要包括煤、 和天然气,它们都含有碳元素。
(2)很多天然矿石中含有碳元素,菱锰矿的主要成分是碳酸锰( MnCO3),其中锰元素的化合价 。
(3)在 440℃和高压条件下,金属钠与二氧化碳反应能生成金刚石(C)和碳酸钠,该反应的化学方程式为 。

(4)炭雕是活性炭成型技术与传统雕刻工艺的完美结合,因为活性炭有疏松多孔的结构,具有 能力,所以,炭雕即可以净化室内空气,又可以美化居住环境。
-
碳元素是组成许多物质的基本元素。
(1)化石燃料主要包括煤、________和天然气,它们都含有碳元素。
(2)很多天然矿石中含有碳元素,菱锰矿的主要成分是碳酸锰( MnCO3),其中锰元素的化合价___。
(3)在 440℃和高压条件下,金属钠与二氧化碳反应能生成金刚石(C)和碳酸钠,该反应的化学方程式为______________ 。
(4)炭雕是活性炭成型技术与传统雕刻工艺的完美结合,因为活性炭有疏松多孔的结构,具有_____能力,所以,炭雕即可以净化室内空气,又可以美化居住环境。

-
我国某科研团队以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料,制取高纯碳酸锰,工艺流程如下图:
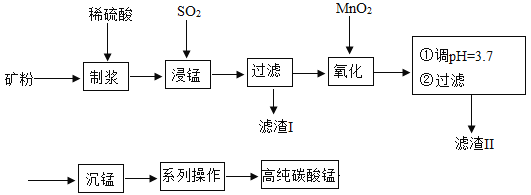
已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为_____、_____(写化学式) ;
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:_____, 该反应中共有_____种元素的化合价发生了改变。
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:_____。
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为_____%(保留一位小数)
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
| 矿酸比 | 温度/(℃) | 浸出率/(%) |
| 1 | 1:0.5 | 60 | 80.2 |
| 2 | 1:0.5 | 80 | 83.8 |
| 3 | 1:0.6 | 60 | X |
| 4 | 1:0.6 | 80 | 91.8 |
表中 X 最有可能的数值为_____。
a.79.7 b.80.8 c.87.6 d.92.8
-
我国某科研团队以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料,制取高纯碳酸锰,工艺流程如下图:
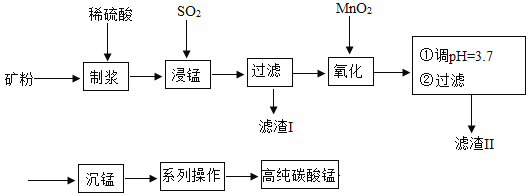
已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为_____、_____(写化学式) ;
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:_____, 该反应中共有_____种元素的化合价发生了改变。
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:_____。
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为_____%(保留一位小数)
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
| 矿酸比 | 温度/(℃) | 浸出率/(%) |
| 1 | 1:0.5 | 60 | 80.2 |
| 2 | 1:0.5 | 80 | 83.8 |
| 3 | 1:0.6 | 60 | X |
| 4 | 1:0.6 | 80 | 91.8 |
表中 X 最有可能的数值为_____。
a.79.7 b.80.8 c.87.6 d.92.8










