-
氢化镁(MgH2)常被作为储氢介质,它与几种物质的转化关系如下。已知B、E之间发生中和反应,且F是一种盐酸盐。(所有的反应物和生成物均已标出)

(1)写出E的化学式: ;
(2)在实验室发生A→C+D的反应条件是: ;
(3)C作为一种新能源具有很多优点,试写出其中的一个优点: ;
(4)写出MgH2 + A→B+C的化学方程式: 。
九年级化学计算题极难题查看答案及解析
-
(9分)实验室有一瓶硫酸溶液,老师请小红同学设计方案测定该废液中硫酸的质量分数。小红同学先取一洁净小烧杯,称其质量为18.2g,然后往其中倒入少量硫酸废液后称量,总质量为33.2g,之后,将一枚质量为10.8g的铁钉(已用砂纸打磨去年铁锈)放入该小烧杯中反应,待铁钉表面不再有气泡产生后,再次称量,总质量为43.9 g。
请回答下列问题:
(1)反应中产生的气体的质量是 。
(2)计算该废液中硫酸的质量分数(写出计算过程,计算结果保留一位小数)。(6分)
(3)如果铁钉的铁锈未除净,对计算结果的影响是 (选填“偏大”、“偏小”、“无影响”),原因是 。
九年级化学计算题极难题查看答案及解析
-
侯氏制碱法为纯碱工业的发展做出了杰出的贡献。用此方法制得的工业纯碱产品中会含有一定量的氯化钠。为测定一种用侯氏制碱法生产的工业纯碱产品中碳酸钠的纯度,现取26.5g该工业纯碱样品。加入100g某溶质质量分数的稀盐酸,恰好完全反应,得到117.7g不饱和溶液,计算:
(1)生成CO2气体的质量
(2)样品中碳酸钠的纯度
(3)若向反应后的溶液中加入54.5g水,求所得溶液中溶质和溶剂的质量最简比
九年级化学计算题极难题查看答案及解析
-
(7分)学过金属活动性后,秦思同学通过实验探究锌粉与硝酸亚铁和硝酸银两种盐溶液的反应。实验现象和数据如下:

第一次
第二次
第三次
第四次
硝酸亚铁与硝酸银的混合溶液
100g
100g
100g
100g
锌粉
2g
3.25g
m
9.75g
向滤液中加入稀盐酸后的实验现象
产生白色沉淀
无明显现象
无明显现象
无明显现象
向滤渣中加入100 g稀盐酸后的实验现象
无明显现象
无明显现象
产生气泡,溶液变为浅绿色
现象与第三次相同
(1)第四次向滤渣中加入稀盐酸后产生气泡的化学方程式为 ;
(2)根据第一次的实验现象,你认为此次滤液中的溶质是 ;
(3)根据已知条件列出求解第二次实验中置换出金属银的质量(x)的比例式 ;
(4)若第三次实验锌与两种盐溶液恰好完全反应,则m的质量为__________________;
(5)若向第三次反应后的滤液中加入一定质量的水,所得不饱和溶液中溶质的质量分数为10%,则加入水的质量为__________________;
(6)若用溶质质量分数为36.5%的浓盐酸配制第四次实验中与滤渣恰好完全反应所需的稀盐酸,则需要浓盐酸与水的质量比为_______________。
九年级化学计算题极难题查看答案及解析
-
(一)实验室有一瓶标签如图所示的浓盐酸,要配制200g7.3%的盐酸,需要用该盐酸多少毫升?

(二)某校化学兴趣小组用所配制的稀盐酸,测定该某矿山上的石灰石样品中碳酸钙的质量分数,假设矿石中只含杂质二氧化硅(二氧化硅是一种极难溶于水也不与盐酸反应且耐高温的固体),他们取一块,将其粉碎后,称出11g放入烧杯内(烧杯的质量为20g), 然后加入100g所配制的稀盐酸,用玻璃棒搅拌至不再产生气泡为止,二者恰好完全反应,得到下列数据,请分析表格中的数据,回答下列问题。
反应前
反应后
实验
数据
烧杯和石灰石质量
加入盐酸质量
反应后混合物质量
31g
100g
126.6g
(1)生成二氧化碳的质量为多少?
(2)此石灰石样品碳酸钙的质量分数为多少;
(3)将反应后混合物过滤,将滤液蒸发掉多少克水后可得到某温度下氯化钙的饱和溶液(某温度下,氯化钙的溶解度为25克)(计算结果保留一位小数)
(4)若某石灰厂在矿山上开采出这样的矿石550吨,最后可得含杂质的生石灰多少吨?
九年级化学计算题极难题查看答案及解析
-
某工厂废液中含有氯化钠、氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如下图所示。
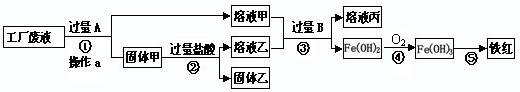
回答下列问题:
(1)加入过量A溶解后,再进行操作a时玻璃棒的作用是。
(2)工厂废液中加入过量A反应的化学方程式为________。
(3)固体乙的主要成分是________。
(4)铁红是炼铁的主要原料,用CO和铁红炼铁的化学方程式为。
(5)某研究性学习小组的同学为了测定某钢铁厂生铁样品中铁的质量分数,在实验室中
称取生铁样品5.8g放入烧杯中,然后再加入足量的稀硫酸,使之充分反应后,共收
集到0.2g氢气(杂质不参加反应)。则该生铁样品中铁的质量分数为________。(列出计算过程,保留一位小数。)
九年级化学计算题极难题查看答案及解析
-
Na2CO3中往往会含有少量的NaCl,现在一烧杯中盛有20.4g的固体混合物,向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:

①当滴加稀盐酸至图中B点时,烧杯中溶液的pH 7(填>、=、<)。 (1分)
②当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。(计算结果保留一位小数)(4分)
九年级化学计算题极难题查看答案及解析
-
(7分)在一烧杯中盛有60.2gBaCO3 和BaCl2的粉末状混合物,向其中加入188.8g水使混合物中可溶物完全溶解,然后向其中逐滴加入溶质质量分数为10%的稀盐酸至146g时恰好反应完全,请根据题意回答问题:
(1)在滴加盐酸过程中观察到的明显实验现象是 。
(2)当盐酸滴加至140g时,烧杯中溶液里含有溶质的是 。(写化学式)
(3)计算恰好反应完全时烧杯中所得不饱和溶液的质量。(结果精确到0.1g)
九年级化学计算题极难题查看答案及解析
-
28g石灰石样品与210.8g稀盐酸恰好完全反应后(样品中的杂质既难溶于水,又不与稀盐酸反应),生成了8.8g二氧化碳。(溶解在水中的二氧化碳忽略不计)计算:
(1)该石灰石样品中碳酸钙的质量分数。
(2)所得溶液的溶质质量分数。
九年级化学计算题极难题查看答案及解析
-
(2015秋•辛集市期末)烧碱是一种重要的化工原料,用碳酸钠溶液与熟石灰发生反应,之后将生成物进行一系列处理得到固体烧碱,同学们在实验室制取少量烧碱固体.实验过程中向200g碳酸钠溶液中不断加入澄清石灰水,所加澄清石灰水的质量与生成沉淀的质量关系如图所示.请回答下列问题.

(1)a点时反应混合液中的阳离子主要是 (填化学式);
(2)通过计算回答,此碳酸钠溶液中溶质的质量分数是多少?
九年级化学计算题极难题查看答案及解析