-
(8分)现有Fe和Fe2O3的固体混合物,东东同学为了分析混合物中Fe和Fe2O3的含量,设计了如下实验方案:(注意:100g是Fe与Fe2O3两种物质的总质量)
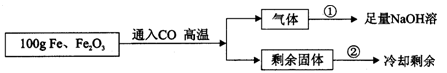
【实验数据】实验共记录了两组实验数据:
第①组,完全吸收气体后,NaOH溶液质量增加了66g;
第②组,完全反应,冷却后称量剩余固体的质量为Wg。
根据实验设计及有关数据进行分析与计算。
(1)根据第①组数据,CO与Fe2O3,反应产生CO2 g。
(2)混合物中Fe2O3的质量为多少?
(3)第②组数据W是 g。
九年级化学计算题极难题查看答案及解析
-
(8分)现有Fe和Fe2O3的固体混合物,东东同学为了分析混合物中Fe和Fe2O3的含量,设计了如下实验方案:(注意:100g是Fe与Fe2O3两种物质的总质量)
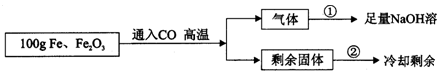
【实验数据】实验共记录了两组实验数据:
第①组,完全吸收气体后,NaOH溶液质量增加了66g;
第②组,完全反应,冷却后称量剩余固体的质量为Wg。
根据实验设计及有关数据进行分析与计算。
(1)根据第①组数据,CO与Fe2O3,反应产生CO2 g。
(2)混合物中Fe2O3的质量为多少?
(3)第②组数据W是 g。
九年级化学计算题极难题查看答案及解析
-
某厂生产的纯碱包装袋上标有Na2CO3 90%字样(杂质为NaCl)。为判断该纯碱是否合格,取12g样品放入烧杯中,加入100g稀盐酸,恰好完全反应。反应后所得溶液质量为107.6 g(产生的气体全部逸出,且知:Na2CO3 +2HCl=2NaCl+CO2↑+H2O)。
试计算:(写出计算过程)
(1)反应生成二氧化碳的质量;
(2)所用稀盐酸中溶质的质量分数;
(3)判断该纯碱产品是否合格。
九年级化学计算题极难题查看答案及解析
-
(10分)某兴趣小组分别向80.00 g 10%的NaOH溶液中加入体积不同、质量分数相同的盐酸,充分反应后,将所得溶液加热蒸发,直到固体完全析出且没有任何变化后,再研细、烘干、称量;重复将固体烘干、称量,直至称得的固体质量不再发生变化。实验测得,向80.00 g10%的NaOH溶液中加入80.00 mL盐酸时,溶液恰好呈中性,其它测得的部分数据则如下表所示:

(1)加热蒸发所得溶液时需要用玻璃棒不断搅拌,其目的是: ;
(2)向80.00 g 10%NaOH溶液中加入盐酸的体积为100.00 mL时,最后所得固体的质量仍为11.70 g,其原因是: ,
(3)列式求出向80.00 g 10%NaOH溶液中加入40.00 mL盐酸时,最后所得固体中NaCl的质量分数(小数点后保留两位)。
九年级化学计算题极难题查看答案及解析
-
我市锰矿资源丰富,MnO2是一种无机功能材料,主要用于制造干电池。当地某工厂加工得到了粗MnO2(主要含有杂质MnCO3,其它杂质忽略不计),为了测定其中MnO2的含量,称取57.5g粗MnO2样品,加入足量的稀硫酸溶液,产生CO2气体4.4g。
(已知:MnCO3+ H2SO4
MnSO4+H2O+CO2↑)
试完成下列问题:(1)计算57.5g粗MnO2中含有MnCO3的质量,
(2)计算粗MnO2中的MnO2的质量分数。
九年级化学计算题极难题查看答案及解析
-
我市庐江县小包庄去年发现一大型铁矿,主体为磁铁矿.冶炼磁铁矿的反应:4CO+Fe3O4
3Fe+4CO2.用100t含Fe3O480%的磁铁矿石,理论上冶炼含杂质4%的生铁多少?(答案保留一位小数)
九年级化学计算题极难题查看答案及解析
-
实验室常用过氧化氢溶液与二氧化锰混合制取氧气.现将2.5g二氧化锰放入盛有100g过氧化氢溶液的锥形瓶中,反应完全结束后,共收集到1.6g气体.请完成下列问题:
(1)反应结束后,过滤,洗涤并烘干滤渣,称得滤渣的质量为 g.
(2)计算原过氧化氢溶液中溶质的质量分数.
九年级化学计算题极难题查看答案及解析
-
实验室有一瓶存放时间过长的氢氧化钠固体,其中一部分已转化成了碳酸钠。现需用该药品配制氢氧化钠溶液。取6克该药品,溶于13.7mL水中(水的密度为1g/cm3),然后慢慢地滴加溶质质量分数为7.4%的澄清石灰水,当用去10克澄清石灰水时,碳酸钠恰好反应完全。计算:(1)6克该药品中碳酸钠的质量;(2)滤出沉淀后所得溶液的溶质质量分数。
九年级化学计算题极难题查看答案及解析
-
某校课外兴趣小组对一批粗锌样品(含有杂质,杂质不溶于水,也不与酸反应)进行分析,甲、乙、丙三组同学分别进行实验,实验数据记录如下:
组别
药品
甲
乙
丙
烧杯 + 稀硫酸/g
152.5
152.5
252.5
粗锌样品/g
20
15
15
烧杯及剩余物/g
172.1
167.1
267.1
请你认真分析数据,帮助他们回答下列问题(每组反应均充分):
(1) 组同学所取用的稀硫酸与粗锌样品恰好完全反应;
(2)计算粗锌样品中锌的质量分数;
(3)计算原硫酸溶液中溶质的质量分数;
(4)计算恰好完全反应的那组实验所得溶液中溶质的质量分数(烧杯质量为52.5g,计算结果精确到0.1%)
九年级化学计算题极难题查看答案及解析
-
(6分)把6.5g 锌放入到50g 硫酸溶液恰好完全反应。计算:
可制得氢气多少克?
这种硫酸溶液中溶质的质量分数是多少?
九年级化学计算题极难题查看答案及解析