-
工业废气H2S经资源化利用后可回收能量并得到单质硫。反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l) ΔH=-632 kJ·mol-1。H2S燃料电池的工作原理如图所示。下列有关说法不正确的是
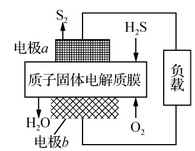
A.电极a为电池的负极
B.电极b上的电极反应式为:O2+4H++4e-=2H2O
C.若电路中通过2 mol电子,则电池内部释放632 kJ热能
D.若有17 g H2S参与反应,则会有1 mol H+经质子膜进入正极区
高二化学选择题极难题查看答案及解析
-
图甲和图乙表示的是元素的某种性质随原子序数的变化。下列说法正确的是

A.图甲可能表示的是元素原子的第一电离能随原子序数的变化关系
B.图甲可能表示的是元素单质的熔点随原子序数的变化关系
C.图乙可能表示的是元素原子的半径随原子序数的变化关系
D.图乙不可能表示同族元素的电负性随原子序数的变化关系
高二化学选择题极难题查看答案及解析
-
分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些酸和醇重新组合可形成的酯共有
A.15种 B.28种 C.32种 D.40种
高二化学选择题极难题查看答案及解析
-
下列说法正确的是:
A.把NaHCO3和Na2CO3混和物6.85 g溶于水制成100 mL溶液,其中c(Na+)=1 mol·L-1,该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量无法计算
B.将54.4 g铁粉和氧化铁的混合物中加入4.0mol/L200 mL的稀硫酸,恰好完全反应,放出氢气4.48 L(标准状况),反应后的溶液中滴加KSCN不显红色,且无固体剩余物,反应后得到FeSO4的物质的量是0.8mol
C.现向一密闭容器中充入1mol N2和3mol H2,在一定条件下使该反应发生,达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
D.某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42+ 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是H+、NH4+、Mg2+、Al3+

高二化学选择题极难题查看答案及解析
-
已知 H2A 为二元弱酸。室温时,配制一组c(H2A)+c(HA-) +c(A2-)=0. 10mol·L-1的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如下图所示。下列指定溶液中微粒的物质的量浓度关系不正确的是
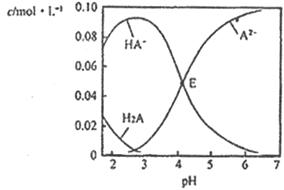
A. pH=7 的溶液中:c(Na+)>2c(A2-)
B. E点溶液中:c(Na+)- c(HA-) <0.10mol·L-1
C. c(Na+)=0.10mol·L-1的溶液中:c(H+)+c(H2A)=c(OH-)+c(A2-)
D. pH=2 的溶液中 c(H2A)+c(A2-)>c(HA-)
高二化学选择题极难题查看答案及解析
-
在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)
M(g)+N(g),所得实验数据如下表:
实验
编号
温度/℃
起始时物质的量/mol
平衡时物质的量/mol
n(X)
n(Y)
n(M)
①
700
0.40
0.10
0.090
②
800
0.10
0.40
0.080
③
800
0.20
0.30
a
④
900
0.10
0.15
b
下列说法正确的是
A.实验①中,若5 min时测得n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol·L-1·min-1
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡时,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
高二化学选择题极难题查看答案及解析
-
某气态不饱和链烃CnHm在一定条件下与H2加成为CnHm+x,取CnHm和H2混合气体共60mL进行实验,发现随混合气中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温同压下测定).由此可知x的数值为

A.4 B.3 C.2 D.1
高二化学选择题极难题查看答案及解析
-
用NA表示阿伏加德罗常数的值.下列叙述正确的
是( )
A.9g甲基(﹣CH3)所含有的电子数是10 NA个
B.22.4L乙烷中含有的共价键数为7NA个
C.常温下,14g乙烯和丙烯的混合物中总原子数为3NA
D.4.2g C3H6中含有的碳碳双键数一定为0.1NA
高二化学选择题极难题查看答案及解析
-
2.48 g铁铜合金完全溶解于80 mL 4.0 mol·L-1稀硝酸中,得到标准状况下672 mL NO气体(假设此时无其他气体产生),下列说法正确的是
A. 取反应后溶液,滴入几滴KSCN溶液,无血红色出现
B. 该合金中铁与铜的物质的量之比是1∶2
C. 反应后溶液(忽略溶液体积变化)中c(H+)=2.5 mol·L-1
D. 向反应后的溶液中加入2.0 mol·L-1NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是120 mL
高二化学选择题极难题查看答案及解析
-
把3mol P和2.5mol Q置于2L密闭容器中,发生如下反应:3P(g)+Q(g)
xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L·min),下列叙述错误的是
A. 5min内P的平均反应速率为0.15mol/(L·min)
B. Q的平衡浓度为1mol/L
C. Q的转化率为25%
D. x是2
高二化学选择题极难题查看答案及解析