-
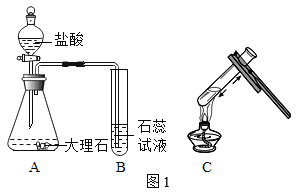
化学小组用图1装置验证二氧化碳与水的反应。
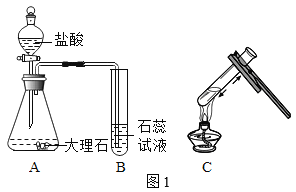
| 盐酸浓度 | 观察到的现象 |
| 甲组 | 浓盐酸(36.5%) | B中石蕊溶液由紫色变成红色 C中石蕊溶液没有变为紫色 |
| 乙组 | 稀盐酸(13.5%) | B中石蕊溶液由紫色变为红色 C中石蕊溶液变为紫色 |
(1)A中反应的化学方程式为_____。
(2)乙组C中反应的化学方程式为_____。
(讨论与交流)同学们认为甲组C中石蕊溶液没有变为紫色,是因为浓盐酸挥发出过多的HCl溶于石蕊溶液。
(提出猜想)盐酸的挥发性与浓度有关。
(进行实验)用图2装置研究不同浓度盐酸的挥发性。用离子传感器测定烧杯中所得溶液的氯离子浓度(氯离子浓度可以近似表示挥发出的HCl的量),实验数据见下表。
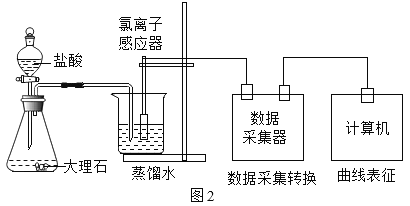
盐酸浓度与氯离子浓度的对应关系(相同时间内测得)
| 盐酸浓度(%) | 13.5 | 20 | 26.2 | 29.2 | 32.2 | 36.5 |
| 氯离子浓度(mg/L) | 1.1 | 1.4 | 3.7 | 19.0 | 59.8 | 209.2 |
分析表中数据,能够得出盐酸的挥发性与浓度的关系是_____。
(得出结论)猜想正确
(实验反思)甲组石蕊溶液变红不能证明二氧化碳与水反应。
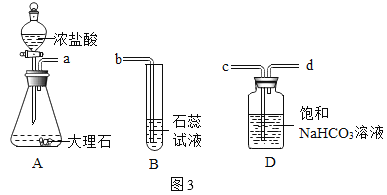
(实验改进)甲组同学在装置A与装置B之间连接装置D。三个装置之间导管口的连接顺序是:a→_____ →_____→b。选择饱和NaHCO3溶液除杂的原因是_____。

-
化学小组用图1装置验证二氧化碳与水的反应。

| 盐酸浓度 | 观察到的现象 |
| 甲组 | 浓盐酸(36.5%) | B中石蕊溶液由紫色变成红色 C中石蕊溶液没有变为紫色 |
| 乙组 | 稀盐酸(13.5%) | B中石蕊溶液由紫色变为红色 C中石蕊溶液变为紫色 |
(1)A中反应的化学方程式为_____。
(2)乙组C中反应的化学方程式为_____。
(讨论与交流)同学们认为甲组C中石蕊溶液没有变为紫色,是因为浓盐酸挥发出过多的HCl溶于石蕊溶液。
(提出猜想)盐酸的挥发性与浓度有关。
(进行实验)用图2装置研究不同浓度盐酸的挥发性。用离子传感器测定烧杯中所得溶液的氯离子浓度(氯离子浓度可以近似表示挥发出的HCl的量),实验数据见下表。
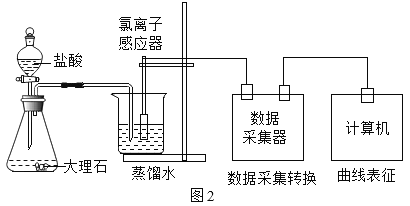
盐酸浓度与氯离子浓度的对应关系(相同时间内测得)
| 盐酸浓度(%) | 13.5 | 20 | 26.2 | 29.2 | 32.2 | 36.5 |
| 氯离子浓度(mg/L) | 1.1 | 1.4 | 3.7 | 19.0 | 59.8 | 209.2 |
分析表中数据,能够得出盐酸的挥发性与浓度的关系是_____。
(得出结论)猜想正确
(实验反思)甲组石蕊溶液变红不能证明二氧化碳与水反应。
(实验改进)甲组同学在装置A与装置B之间连接装置D。三个装置之间导管口的连接顺序是:a→_____ →_____→b。选择饱和NaHCO3溶液除杂的原因是_____。
-
化学小组用图1装置验证二氧化碳与水的反应。
| 盐酸浓度 | 观察到的现象 |
| 甲组 | 浓盐酸(36.5%) | B中石蕊溶液由紫色变成红色 C中石蕊溶液没有变为紫色 |
| 乙组 | 稀盐酸(13.5%) | B中石蕊溶液由紫色变为红色 C中石蕊溶液变为紫色 |
(1)A中反应的化学方程式为_____。
(2)乙组C中反应的化学方程式为_____。
(讨论与交流)同学们认为甲组C中石蕊溶液没有变为紫色,是因为浓盐酸挥发出过多的HCl溶于石蕊溶液。
(提出猜想)盐酸的挥发性与浓度有关。
(进行实验)用图2装置研究不同浓度盐酸的挥发性。用离子传感器测定烧杯中所得溶液的氯离子浓度(氯离子浓度可以近似表示挥发出的HCl的量),实验数据见下表。

盐酸浓度与氯离子浓度的对应关系(相同时间内测得)
| 盐酸浓度(%) | 13.5 | 20 | 26.2 | 29.2 | 32.2 | 36.5 |
| 氯离子浓度(mg/L) | 1.1 | 1.4 | 3.7 | 19.0 | 59.8 | 209.2 |
分析表中数据,能够得出盐酸的挥发性与浓度的关系是_____。
(得出结论)猜想正确
(实验反思)甲组石蕊溶液变红不能证明二氧化碳与水反应。
(实验改进)甲组同学在装置A与装置B之间连接装置D。三个装置之间导管口的连接顺序是:a→_____ →_____→b。选择饱和NaHCO3溶液除杂的原因是_____。

-
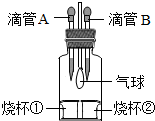
某学习小组利用右图装置完成如下实验,以验证所学物质的性质.
(1)若A中盛有浓盐酸,B中盛有紫色的石蕊试液,将A、B中液体分别滴入烧杯①、②中,一段时间后观察到的现象是______.
(2)化学反应通常伴随能量的变化,可借助反应前后的温度变化来判断是否发生了反应.在不使用温度计的情况下,若A中盛有稀盐酸,烧杯①中盛有固体氢氧化钠,将A中的稀盐酸滴入烧杯①,观察到气球变瘪,则证明反应发生了.有的同学提出:该现象不足以证明NaOH与稀盐酸发生了化学反应.他的理由是:______.(填一种即可)
(3)若将集气瓶中充满CO2,先将B中盛放的NaOH溶液滴入烧杯②中少量,会看到气球微微变鼓;再将A中的液体滴入烧杯①.请根据下列实验现象将下表中的试剂补充完整.
现象
装置 | ①
气球变瘪又恢复原状 | ②
气球变瘪 | ③
气球先变瘪后又变得更鼓 |
| 滴管A | ______ | ______ | H2O |
| 烧杯① | H2O | 固体Na2CO3 | ______ |
-
某学习小组利用右图装置完成如下实验,以验证所学物质的性质。
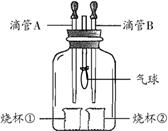
(1)若A中盛有浓盐酸,B中盛有紫色的石蕊试液,将A、B中液体分别滴入烧杯①、②中,一段时间后观察到的现象是________。
(2)化学反应通常伴随能量的变化,可借助反应前后的温度变化来判断是否发生了反应。在不使用温度计的情况下,若A中盛有稀盐酸,烧杯①中盛有固体氢氧化钠,将A中的稀盐酸滴入烧杯①,观察到气球变瘪,则证明反应发生了。有的同学提出:该现象不足以证明NaOH与稀盐酸发生了化学反应。他的理由是:________。(填一种即可)
(3)若将集气瓶中充满CO2,先将B中盛放的NaOH溶液滴入烧杯②中少量,会看到气球微微变鼓;再将A中的液体滴入烧杯①。请根据下列实验现象将下表中的试剂补充完整。
|  现象 现象
装置 | ① 气球变瘪又恢复原状 | ② 气球变瘪 | ③ 气球先变瘪后又变得更鼓 |
| 滴管A | | | H2O |
| 烧杯① | H2O | 固体Na2CO3 | |
-
某化学兴趣小组利用如图所示装置制取二氧化碳并对其性质进行验证:
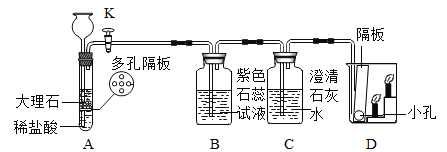
(1)A装置的优点是______________________。
(2)当打开K,反应一段时间后,B处紫色石蕊溶液变成红色,写出B处发生反应的化学方程式:________________________;C处澄清石灰水变浑浊,写出C处发生变化的化学方程式:______________________;D烧杯中______(填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的性质是_________、____________________(写两点),二氧化碳灭火的原理是______________。
-
某化学兴趣小组进行如下组合实验,对二氧化碳的性质进行验证。
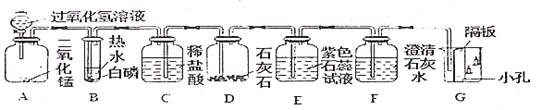
当打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进人D中。E处紫色石蕊溶液变成红色,F处澄清石灰水变浑浊。
(1)A中发生反应的化学方程式为________。
(2)B中白磷能够燃烧的原因是____________;_______________。
(3)G烧杯中___________(填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的物理性质是___________,具有的化学性质是_____________。
(4)E处使紫色石蕊变成红色的物质是________________;
(5)写出D处发生变化的化学方程式_____________________。
-
某小组设计如下实验制取二氧化碳并验证其性质(不考虑盐酸的挥发性)。
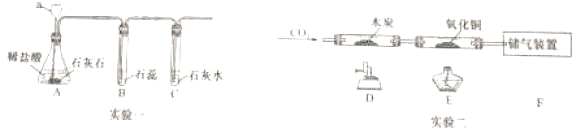
①写出仪器a的名称__。
②A中发生反应的化学方程式是___;B中使石蕊变红的物质是__;C装置的作用是__,观察到的现象是__。
③实验二中,先通入二氧化碳一段时间后再加热,目的是__;D处玻璃管中发生反应的化学方程式是__;装置F的作用是___。
④设计实验证明储气装置中的一种气体成分__。
| 步骤 | 现象及结论 |
| ___________ | ____________ |
-
观察和实验是学习科学的重要方式,下列实验中观察到的现象正确的是( )
A.盐酸能使紫色石蕊试液变蓝色
B.硫酸铜溶液中滴加氢氧化钾溶液出现红褐色絮状沉淀
C.铁锈放入稀硫酸中充分反应,溶液变成棕黄色
D.在澄清石灰水中加入稀硝酸,溶液颜色无明显变化
-
利用右图装置分别进行两组实验。

(1)验证二氧化碳是否与水反应。A中盛放干燥的紫色石蕊纸花,B中盛放 ,关闭K1、打开K2,从a处通入二氧化碳气体,若观察到 现象,则可以证明二氧化碳与水发生了化学反应。
(2) 除去氧气中混有的少量二氧化碳气体。实验小组的同学在讨论实验方案时出现了分歧。小刚方案:A中盛放澄清的石灰水,打开K1、关闭K2,从a处通入混合气体,在b处放带火星的木条,若带火星的木条复燃,则二氧化碳已除去。A中反应的化学方程式为 。小丽认为该方案不够严谨,对此进行了改进。她的方案是 。














