-
下列说法不正确的是( )
A.镁铝合金mg和足量的盐酸反应生成H20.1g,则m可能是0.8
B.常温下,将5.6g生石灰放入94.4g水中,所得溶液中溶质质量分数小于1%
C.将镁粉和铝粉的混合物7.2g与足量的氧气充分反应,得到的氧化物质量可能为13.6g
D.将铁合金置于氧气中燃烧得到0.44g二氧化碳和29g四氧化三铁,则铁合金是钢
九年级化学多选题困难题查看答案及解析
-
下列说法正确的是( )
A. 镁铝合金mg和足量的盐酸反应生成0.1g H2,则m可能是1
B. 要使SO2、SO3中含有相同质量的氧元素,则SO2与SO3的分子个数比2:3
C. 将质量分数为20%的KNO3溶液90g配制成40%的溶液,需加入45gKNO3固体
D. 氧化钙和碳酸钙的固体混合物质量为120g,将其高温煅烧至碳酸钙完全分解,称得剩余固体的质量为84g。则原固体混合物中钙元素的质量分数为50%
九年级化学多选题困难题查看答案及解析
-
下列说法正确的是
A. 镁铝合金mg和足量的盐酸反应生成0.1g H2,则m可能是1
B. 要使SO2、SO3中含有相同质量的氧元素,则SO2与SO3的分子个数比2:3
C. 将质量分数为20%的KNO3溶液90g配制成40%的溶液,需加入45gKNO3固体
D. 氧化钙和碳酸钙的固体混合物质量为120g,将其高温煅烧至碳酸钙完全分解,称得剩余固体的质量为84g。则原固体混合物中钙元素的质量分数为50%
九年级化学多选题困难题查看答案及解析
-
镁铝合金x g和足量的盐酸反应后可生成0.1 g H2,则x可能为
A. 0.8 B. 1 C. 1.5 D. 无法确定
九年级化学单选题中等难度题查看答案及解析
-
镁铝合金xg与足量的稀盐酸反应后,经测定生成0.2g氢气,则x 可能为( )
A. 2.2 B. 1.6 C. 2.8 D. 无法确定
九年级化学单选题中等难度题查看答案及解析
-
在托盘天平的两盘分别放入质量相等的烧杯,烧杯中各盛放100g溶质质量分数为7.3%的稀盐酸,向两个烧杯中同时放入下列物质,反应停止后天平不平衡的是
A.5.6g铁 5.6g镁铝合金
B.2.4g镁 2.4g铝
C.10g碳酸钙 5.6g氧化钙
D.16.8gNaHCO3 16.8gMgCO3
九年级化学单选题中等难度题查看答案及解析
-
某氢氧化钠固体样品,可能含有固体氢氧化钾和不溶于酸的杂质 A,取 5.6g 该样品与 100g 一定质量分数 的稀盐酸反应,两者恰好完全反应,生成 mg 水,下列说法正确的是( )
A. 若样品不含任何杂质,则 m<1.8
B. 若 m=1.8,则样品中一定含有杂质 A,可能含有固体氢氧化钾
C. 若 m=1.8,则样品中至少含有杂质 A 或固体氢氧化钾中的一种
D. 若样品中既含有 A,也含有固体氢氧化钾,则一定 m>1.8
九年级化学单选题困难题查看答案及解析
-
某氢氧化钠固体样品,可能含有固体氢氧化钾和不溶于酸的杂质A,取5.6g该样品与100g一定质量分数的稀盐酸反应,两者恰好完全反应,生成mg水。下列说法正确的是
A. 若样品不含任何杂质,则m < 1.8
B. 若m =1.8,则样品中一定含有杂质A,可能含有固体氢氧化钾
C. 若m =1.8,则样品中至少含有杂质A或固体氢氧化钾中的一种
D. 若样品中既含有A,也含有固体氢氧化钾,则一定m > 1.8
九年级化学单选题困难题查看答案及解析
-
某NaOH固体样品,可能含有固体KOH和不溶于酸的杂质A,取5.6g该样品与100g一定质量分数的稀盐酸反应,两者恰好完全反应,生成mg水。下列说法正确的是
A.若样品不含任何杂质,则m<1.8
B.若m=1.8,则样品中一定含有杂质A,可能含有固体KOH
C.若m>1.8, 则样品中一定含有固体KOH, 可能含有杂质A
D.若样品中不含A,则盐酸的溶质质量分数可能为4%
九年级化学多选题困难题查看答案及解析
-
镁铝合金强度大、密度小,合金表面易上色,常用作笔记本电脑的外壳。
Ⅰ.(1)形状大小相同的铝和镁,分别放入同样的盐酸溶液中,下列说法不正确的是 (填序号)。
A.两者都发生反应 B.镁比铝反应剧烈 C.铝不与盐酸溶液反应
(2)镁与氢氧化钠溶液不反应,而金属铝能与氢氧化钠、水共同作用生成易溶于水的钠盐(用化学式NaAlO2表示)和H2,写出该反应的化学方程式: 。
Ⅱ.三位同学通过进行如下途径探究,来推算某铝镁合金(假设不含其它杂质)中铝的质量分数。
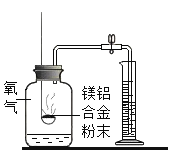
方案一:镁铝合金与氧气反应,测定参与反应的氧气体积。如右图所示,称量一定量镁铝合金粉末,在足量的氧气中充分燃烧,冷却至室温,打开止水夹。参与反应的氧气体积与
相等。
方案二:铝镁合金与盐酸反应,测定生成气体的体积。装置如右图所示。
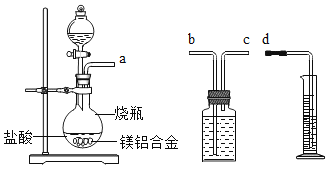
(1)通过排水法测定所收集到的氢气体积,装
置导管口a、b、c、d的连接顺序是:
a→
(2)反应结束,冷却至室温。烧瓶内还留有气体,对实验结果 (填“有”或“没有”)影响。
方案三:铝镁合金与氢氧化钠溶液反应,测定剩余固体质量。称取8g镁铝合金样品,把60g氢氧化钠溶液平均分成三份依次加入样品中,反应过程如下图:

(1)实验中所加的氢氧化钠溶液应过量,其目的是 。
(2)从上图数据可知,该合金中镁元素与铝元素的质量比为 。
(反思与拓展)利用铝镁合金中铝与氢氧化钠溶液反应反应和方案二装置,通过测定
体积,也可得出合金中铝的质量。
九年级化学综合题困难题查看答案及解析