-
已知 Na2CO3与 HCl 反应分两步进行:
第一步 Na2CO3与 HCl 反应生成 NaHCO3: ;
;
第二步 NaHCO3 与 HCl 反应生成 CO2: 。
。
现有这样一个实验:在两支试管中分别加入 3mL 稀盐酸,将两个各装有 0.3g NaHCO3 或 Na2CO3 粉末的小气球分别套在两支试管口,将气球内的NaHCO3或 Na2CO3 同时倒入试管中(反应中盐酸足量)。观察到现象如下:
(1)盛________的试管中产生气体的速率要快得多。
(2)盛_________的试管中气球变得更大,大小气球中生成气体的质量之比为(填最简单整数比)_____。
(3)甲同学用手触摸试管,发现盛 NaHCO3 粉末的试管变冷,而盛 Na2CO3的试管温度有升高。为研究是吸热还是放热反应,继续进行了下列实验(每次实验各做 3 次平行实验,取平均值):
| 序号 | 试剂 1 | 试剂 2 | 混合前温度 | 混合后温度 |
| ① | 35mL 水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
| ② | 35mL 水 | 3.2 Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 35mL 稀盐酸 | 含2.5g NaHCO3的饱和溶液 32.5mL | 20℃ | 19℃ |
| ④ | 35mL 稀盐酸 | 含 3.2g Na2CO3的饱和溶液 23.1mL+10ml 水 | 20℃ | 24.2℃ |
| ⑤ | 35mL 稀盐酸 | 2.5gNaHCO3固体 | 20℃ | 16.2℃ |
| ⑥ | 35mL 稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 25.1℃ |
通过上述实验可得出五条结论:
①NaHCO3 的溶解是__(吸热或放热)过程;
②Na2CO3 的溶解是____(吸热或放热)过程;
③NaHCO3 的饱和溶液和盐酸的反应是___(吸热或放热)反应;
④Na2CO3 的饱和溶液和盐酸的反应是____(吸热或放热)反应;
⑤NaHCO3 固体与稀盐酸反应的反应热是由_____(填①~⑤序号)的热效应之和。
-
(6分)
Na2CO3与盐酸反应分两步进行:
第一步反应为:Na2CO3+HCl===NaCl+NaHCO3;
第二步反应为:NaHCO3+HCl===NaCl+H2O+CO2↑
取Na2CO3溶液100g,逐滴加入稀盐酸直到过量。反应过程中产生的气体质量与加入
的盐酸质量的关系如图所示:

(1)反应中最多可以产生CO2___________g。
(2)求Na2CO3溶液中溶质质量分数(要求书写计算过程)。
(相对原子质量:C—12、Na—23、H—1、O—16)
-
碳酸钠与盐酸的反应是分两步进行的,第一步反应的化学方程式为:Na2CO3+HCl═NaCl+NaHCO3.为验证该反应分两步进行.如图所示进行实验(装置气密性良好).

步骤Ⅰ:用注射器1向小药瓶中緩慢注入一定量的稀盐酸,边注入边振蕩,细玻璃管中液柱略微升高;換注射器2从瓶中缓慢抽取气体,澄清石灰水不浑浊.
步骤Ⅱ:…
(1)补充步骤Ⅱ的实验操作和预期现象.
(2)说明细玻璃管在实验中的作用.
(3)实验后,将小药瓶、注时器1、注射器2中的所有物质依次倒入一个洁净的烧杯中,只得到无色溶液,向其中滴加酚酞溶液不变色.写出溶液中溶质成分存在的几种情况(酚酞省略不写).
-
向碳酸钠溶液中滴加盐酸,利用 pH 传感器测得溶液 pH 与消耗盐酸体积的变化关系如图所示。已知该反应过程分为两个阶段:
①Na2CO3 +HCl = NaHCO3+ NaCl;
②NaHCO3 +HCl = NaCl + H2O + CO2↑,AB 段主要进行①反应,CD 段主要进行②反应。下列说法不合理的是
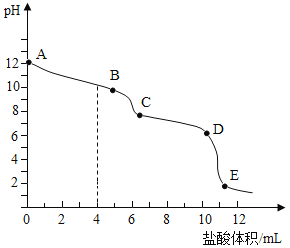
A.加入盐酸体积为 4mL 时有大量气泡产生
B.Na2CO3 溶液比 NaHCO3 溶液的碱性更强
C.D 点处反应基本结束
D.E 点溶液的溶质有氯化钠和氯化氢
-
已知NaHCO3受热分解生成Na2CO3, 。把12克NaHCO3和Na2CO3的混合物样品加热至完全反应,剩余固体的质量为8.9克。下列说法正确的是( )
。把12克NaHCO3和Na2CO3的混合物样品加热至完全反应,剩余固体的质量为8.9克。下列说法正确的是( )
A.反应生成的CO2质量为4.4克 B.样品中Na2CO3的质量分数为30%
C.样品中NaHCO3的质量为8.6克 D.样品中钠元素的质量分数为43.3%
-
仅仅根据化学方程式 Na2CO3+2HCl═2NaCl+CO2↑+H2O,不能获得的信息是( )
A.反应进行得非常快
B.生成的CO2是气态的
C.反应在常温下可以进行
D.反应物是Na2CO3和HCl
-
仅仅根据化学方程式Na2CO3+2HCl=2NaCl+CO2↑+H2O不能获得的信息是
A. 反应进行得非常快 B. 生成的CO2是气态的
C. 反应在常温下可以进行 D. 反应物是Na2CO3和HCl
-
仅仅根据化学方程式Na2CO3 + 2HCl == 2NaCl + CO2↑+ H2O,不能获得的信息是
A. 反应进行得非常快 B. 生成的CO2是气态的
C. 反应在常温下可以进行 D. 反应物是Na2CO3和HCl
-
能用来鉴别Na2CO3和NaHCO3两种白色固体的方法是( )
A.分别放入水中,观察溶解速率
B.分别取少量加入到石灰水中,观察有无沉淀生成
C.分别取少量溶于水后,滴入HCl溶液观察有无气体生成
D.分别取少量溶于水后,滴入CaCl2溶液观察有无沉淀生成
-
现有一种Na2CO3和NaHCO3的混合物,某同学为测定其含量,取一定量的该样品溶于水,逐滴加入稀盐酸并不断振荡,首先发生反应:Na2CO3 + HCl = NaHCO3 + NaCl,然后才发生反应:NaHCO3+ HCl = NaCl + CO2↑+ H2O。
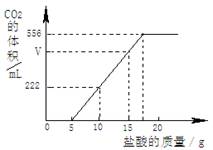
已知:该温度下CO2密度为1.98g/L,实验测得产生的CO2的与加入稀盐酸的数据如右图。
(1)当加入________g盐酸时,才开始产生CO2;图中V=________mL。
(2)请计算:①所加入盐酸中HCl的质量分数为多少?
②原样品中Na2CO3和NaHCO3的质量各是多少?(百分数精确到0.1%,质量精确到0.01g)
;
。


