-
为了比较铝与相同pH的稀盐酸和稀硫酸反应的快慢.某化学兴趣小组做了如下实验探究:

(1)写出铝与稀硫酸反应的化学方程式________________________。
(2)X=________________________。
(3)实验过程中,发现铝与稀盐酸反应更加剧烈,同学们提出了以下猜想:
[做出猜想]猜想1:水分子( H2O)起催化作用;
猜想2:氯离子(Cl-)起催化作用;
猜想3:硫酸根离子(SO42-)起阻碍作用;
...............
你认为上述猜想_____________不合理,说出你的理由______________________。
[进行猜想]为了验证上述猜想是否正确,向试管1中加入少量____________(填序号)。试管Ⅱ中加入少量____________做对比实验。
A 硫酸铜
B 氯化钠
C 硫酸钠
D 浓硫酸
[得出结论]猜想2正确。
[拓展延伸]同一个化学反应可以具有不同的催化剂,对反应速率的影响结果也不相同。由此,小明提出了一个新的探究话题?________________________ (说出一种即可)。
-
为了比较铝与相同pH的稀盐酸和稀硫酸反应的快慢,某化学兴趣小组做了如下探究实验.

(1)铝与稀硫酸反应的化学方程式为_____.
(2)x=_____,选择此数值的理由_____.实验过程中,可以通过观察_____来比较铝与稀盐酸和稀硫酸反应的剧烈程度.
(3)实验过程中,发现铝与稀盐酸反应更加剧烈,同学们提出了以下猜想:
猜想一:试管Ⅰ中氯离子对反应起了促进作用;
猜想二:试管Ⅱ中硫酸根离子对反应起了阻碍作用;
猜想三:以上两种猜想同时成立.
为了验证上述猜想是否正确,向试管Ⅰ中加入少量_____(填序号),向试管Ⅱ中加入少量_____(填序号),作对比实验.
A 硫酸铜 B 氯化钠 C 硫酸钠 D 浓盐酸
(4)通过(3)中的对比实验,观察到试管Ⅰ中反应快慢无明显变化,试管Ⅱ中反应明显加剧,则_____猜想成立.
-
为了比较铝与相同pH的稀盐酸和稀硫酸反应的快慢,某化学兴趣小组做了如下探究实验.

(1)铝与稀硫酸反应的化学方程式为_____.
(2)x=_____,选择此数值的理由_____.实验过程中,可以通过观察_____来比较铝与稀盐酸和稀硫酸反应的剧烈程度.
(3)实验过程中,发现铝与稀盐酸反应更加剧烈,同学们提出了以下猜想:
猜想一:试管Ⅰ中氯离子对反应起了促进作用;
猜想二:试管Ⅱ中硫酸根离子对反应起了阻碍作用;
猜想三:以上两种猜想同时成立.
为了验证上述猜想是否正确,向试管Ⅰ中加入少量_____(填序号),向试管Ⅱ中加入少量_____(填序号),作对比实验.
A 硫酸铜 B 氯化钠 C 硫酸钠 D 浓盐酸
(4)通过(3)中的对比实验,观察到试管Ⅰ中反应快慢无明显变化,试管Ⅱ中反应明显加剧,则_____猜想成立.
-
为了比较铝与相同pH的稀盐酸和稀硫酸反应的快慢,某化学兴趣小组做了如下的探究实验:
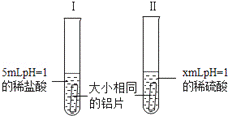
(1)x=_____;
(2)实验过程中,发现铝与稀盐酸反应更加剧烈,同学们提出了以下猜想:
猜想一:试管Ⅰ中氯离子对反应起了促进作用;
猜想二:试管Ⅱ中_______对反应起了阻碍作用;
猜想三:以上两种猜想同时成立.
为了验证上述猜想是否正确,向试管Ⅰ中加入少量硫酸钠,向试管Ⅱ中加入少量____(填序号),作对比试验.
A、硫酸铜 B、氯化钠 C、浓盐酸
(3)通过(2)中的对比试验,观察到试管Ⅰ中反应快慢无明显变化,试管Ⅱ中反应明显加剧,则猜想_____成立.
-
为了比较铝与相同pH的稀盐酸和稀硫酸反应的快慢,某化学兴趣小组做了如下的探究实验:

(1)铝与稀硫酸反应的化学方程式为________________________________________________________________________________________________。
(2)X=________________________________________,实验过程中,可以通过观察________________________________________来比较铝与稀盐酸和稀硫酸反应的剧烈程度。
(3)实验过程中,发现铝与稀盐酸反应更加剧烈,同学们提出了以下猜想:
猜想一:试管Ⅰ中氯离子对反应起了促进作用;
猜想二:试管Ⅱ中硫酸根离子对反应起了阻碍作用;
猜想三:以上两种猜想同时成立。
为了验证上述猜想是否正确,向试管Ⅰ中加入少量________________________________________________________(填序号),向试管Ⅱ中加入少量________________________________________________________(填序号),做对比实验。
A.硫酸铜 B.氯化钠 C.硫酸钠 D.浓盐酸
(4)通过(3)中的对比实验,观察到试管Ⅱ中反应快慢无明显变化,试管Ⅰ中反应明显加剧,则猜想________________________成立。
-
为了比较铝与相同pH的稀盐酸和稀硫酸反应的快慢,某化学兴趣小组做了如下的探究实验:

(1)铝与稀硫酸反应的化学方程式为________________________________________________________________________________________________。
(2)X=________________________________________,实验过程中,可以通过观察________________________________________来比较铝与稀盐酸和稀硫酸反应的剧烈程度。
(3)实验过程中,发现铝与稀盐酸反应更加剧烈,同学们提出了以下猜想:
猜想一:试管Ⅰ中氯离子对反应起了促进作用;
猜想二:试管Ⅱ中硫酸根离子对反应起了阻碍作用;
猜想三:以上两种猜想同时成立。
为了验证上述猜想是否正确,向试管Ⅰ中加入少量________________________________________________________(填序号),向试管Ⅱ中加入少量________________________________________________________(填序号),做对比实验。
A.硫酸铜 B.氯化钠 C.硫酸钠 D.浓盐酸
(4)通过(3)中的对比实验,观察到试管Ⅱ中反应快慢无明显变化,试管Ⅰ中反应明显加剧,则猜想________________________成立。
-
为了比较铝与相同pH的稀盐酸和稀硫酸反应的快慢,某化学兴趣小组做了如下的探究实验:

(1)铝与稀硫酸反应的化学方程式为________________________________________________________________________________________________。
(2)X=________________________________________,实验过程中,可以通过观察________________________________________来比较铝与稀盐酸和稀硫酸反应的剧烈程度。
(3)实验过程中,发现铝与稀盐酸反应更加剧烈,同学们提出了以下猜想:
猜想一:试管Ⅰ中氯离子对反应起了促进作用;
猜想二:试管Ⅱ中硫酸根离子对反应起了阻碍作用;
猜想三:以上两种猜想同时成立。
为了验证上述猜想是否正确,向试管Ⅰ中加入少量________________________________________________________(填序号),向试管Ⅱ中加入少量________________________________________________________(填序号),做对比实验。
A.硫酸铜 B.氯化钠 C.硫酸钠 D.浓盐酸
(4)通过(3)中的对比实验,观察到试管Ⅱ中反应快慢无明显变化,试管Ⅰ中反应明显加剧,则猜想________________________成立。
-
某校化学兴趣小组对“大理石与稀盐酸反应快慢与温度的关系”进行了探究。
[实验探究]在不同温度下测量收集等体积CO2所需的时间及溶液温度变化(盐酸浓度18%、大理石颗粒大小均匀、质量相同),如下表:
| 温度/°C | 需要的时间/s | 温度变化/°C |
| 15 | 145 | +1 |
| 20 | 105 | +1 |
| 25 | 73 | +3 |
| 30 | 51 | +3 |
| 35 | 30 | +4 |
(1)写出大理石和稀盐酸反应的化学方程式_____________________。
(2)根据上表分析,大理石和稀盐酸反应过程中伴随着________________________(填“吸热”或“放热”现象)。
(3)在实验中控制的变量有_____________________________(填写一种即可)。
[实验结论]
(4)实验结果_______________________(填“可靠”或“不可靠”),理由是______________________。
[评价与反思]
(5)根据上表数据分析,你认为实验中温度计的灵敏度__________(填“高”或“不高”),其原因是______。
(6)除了温度,大理石和稀盐酸反应的快慢还可能受哪些因素的影响?请设计方案验证:
[影响因素]______________________。
[实验方案]______________________。
-
为研究锌和铝的金属活动性 ,某研究小组进行了如下探究。
(1)小明设计方案:向表面积相同的铝片和锌粒中分别加入盐酸,根据反应的快慢判断两者的活动性强弱。写出铝与盐酸反应的化学方程式:________。
(2)小芳将一砂纸打磨过的铝片放入一定量的盐酸中,发现有气泡产生 ,还观察到有“灰黑色沉淀”这一异常现象出现。
(提出问题)铝与盐酸反应出现的灰黑色沉淀的组成是什么?
(查阅文献)①铝在颗粒较小时为灰黑色,AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇。②一种金属加入到两种活动性均比它弱的金属化合物溶液的混合液中,会先置出最弱的金属。再置换出第二种金属。该金属会先和最弱的金属盐溶液反应。
(提出合理假设)假设a:该灰黑色沉淀可能含有_________;假设b:该灰黑色沉淀可能含有AlCl3;假设c:该灰黑色沉淀可能含有难溶于酸的物质。
(设计并完成实验)取灰黑色沉淀分别进行如下实验。
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量稀盐酸 | 有微量气泡,固体全部溶解,得到澄清溶液 |
| ② | 加入适量蒸馏水 | 固体部分溶解 |
| ③ | 加入适量无水乙醇 | 固体部分溶解 |
(得出结论)由实验①可判断假设c_____________(填“成立”或“不成立”,)再集合②和③可得出该灰黑色沉淀的成分是__________。
(3)你认为①中小明的实验能否比较锌和铝的金属活动性强弱?______(填“能”或“不能”),分别从设计方法或操作可行性的角度,具体说明理由(一点即可)_____。
(拓展延伸)附加分:若正确回答下列小题,将获得4分的奖励 ,但化学试卷总分不超过60分。为继续研究另一种金属锌的化学性质,小敏向一定质量的硝酸银和硝酸铜的混合溶液中加入锌粉,溶液质量与加入锌的质量关系如图所示。那么,在a点时,溶液里含的金属化合物有_________种;bc段发生的化学反应方程式为_________;d点得到的固体的成分为_____

-
某兴趣小组为探究金属活动性强弱,分别做了镁、铝、铜与稀盐酸反应的实验。
(1)比较金属活动性强弱:铝比铜______(填“强”或“弱”)。写出镁与稀盐酸反应的化学方程式: ___
(2)小芳同学做镁与稀盐酸反应的实验时,发现试管中出现灰白色沉淀,该小组同学对灰白色沉淀的成分进行如下探究:
[提出假设]假设一:含有氯化镁
假设二:含有镁粉
假设三:含有氢氧化镁
……
[查阅资料]①氯化镁易溶于水:
②在一定条件下镁可与冷水缓慢反应。
[设计并进行实验]各取少量灰白色沉淀加入2支试管中进行如下实验:
| 编号 | 实验操作 | 实验现象 |
| 实验1 | 加入适量蒸馏水、搅拌 | 沉淀未见减少 |
| 实验2 | 加入适量稀盐酸 | 沉淀全部溶解,没有气泡产生 |
[得出结论]由实验1可知,假设___不成立;由实验2可知,沉淀中不含___。
假设三__________(填“成立”或“可能成立”或“不成立”)。
[实验反思]实验后同学们请教老师得知,灰白色沉淀的主要成分是碱式氯化镁,碱式氯化镁受热易分解产生氯化氢气体。于是小芳再取少量灰白色沉淀于试管中加热,并将蘸有紫色石蕊溶液的滤纸条悬于试管口,预期的实验现象是__________________________
注意:若答对第(3)小题奖励4分.化学试卷总分不超过60分。
(3)为探究镁与稀盐酸反应生成碱式氯化镁的条件.该小组同学进行了如下实验:在小烧杯中加入一定量的盐酸和去除氧化膜的镁带,观察实验现象,并测量溶液pH的变化。结果见下表:
| 时间/min | 0 | 2 | 4 | 8 | 12 | 16 | 20 | 24 |
| 溶液pH | 2.0 | 5.3 | 7.0 | 8.6 | 9.3 | 9.8 | 10.0 | 10.0 |
| 实验现象 | - | 镁带溶解较快,产生大量气泡,无沉淀生成 | 镁带缓慢溶解,产生气泡速率减慢,溶液变浑浊,烧杯底部有灰白色沉淀 |
根据表中信息回答下列问题:
①请描述溶液pH变化的规律并解释原因:____________________
②请对生成碱式氯化镁的条件提出猜想,并设计实验证明猜想:____________________







