-
碳酸亚铁(FeCO3)可用于制作补铁药物,以下是用硫铁矿烧渣(主要成分为Fe2O3、SiO2 等)为原料制备碳酸亚铁的生产流程示意图: 已知 40℃以上,(NH4)2CO3易分解。
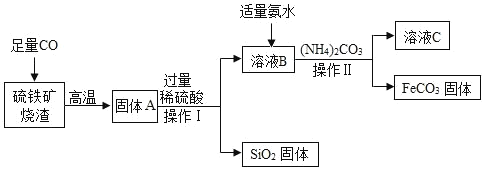
(1)操作Ⅰ的名称为_____该操作所用到的玻璃仪器有烧杯、玻璃棒和_____。
(2)写出向硫铁矿中通入 CO 的化学方程式_____。
(3)加入(NH4)2CO3后,该反应必须控制的条件是温度_____。
(4)写出溶液 B 中主要成分的阴离子符号_____。
(5)从溶液C中可回收一种化工产品(NH4)2SO4,请写出它的一种用途用作_____。
-
碳酸亚铁(FeCO3)可用于制作补铁药物,以下是用硫铁矿烧渣(主要成分为Fe2O3、SiO2等)为原料制备碳酸亚铁的生产流程示意图:
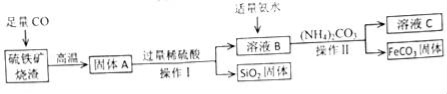
【资料】40℃以上时,(NH4)2CO3易分解.
(1)操作Ⅰ的名称为 .
(2)写出向固体A中加入稀硫酸后发生的化学方程式: .
(3)加入(NH4)2CO3后,该反应必须控制的条件是 .
(4)从溶液C中可回收一种化工产品,请写出它的一种用途 .
-
碳酸亚铁(FeCO3)可用于制作补铁药物,以下是用硫铁矿烧渣(主要成分为Fe2O3、SiO2等)为原料制备碳酸亚铁的生产流程示意图:
(资料)40 以上时,(NH4)2CO3易分解。
以上时,(NH4)2CO3易分解。
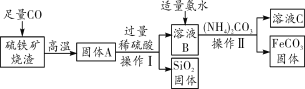
(1)操作 的名称为________。
的名称为________。
(2)写出生成FeCO3的化学方程式:______________。
(3)加入(NH4)2CO3后,该反应必须控制的条件是:_________________。
-
碳酸亚铁(FeCO3)可用于制作补铁药物,以下是用赤铁矿烧渣(主要成分为Fe2O3、SiO2等)为原料制备碳酸亚铁的生产流程示意图:
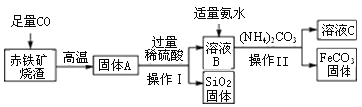
(资料)40℃以上时,(NH4)2CO3易分解。
(1)操作Ⅰ的名称为_____,该操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是_____(填字母序号)。
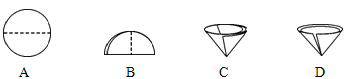
(2)向硫铁矿烧渣中通入CO发生反应的化学方程式为__________。
(3)加入(NH4)2CO3后,该反应必须控制的条件是__________。
(4)溶液C中一定含有的元素有__________。
-
碳酸亚铁(FeCO3)是生产补血剂的原料.以下是某同学设计的利用铁矿烧渣(主要成分是Fe2O3、FeO和泥沙等)制取碳酸亚铁的实验流程图:
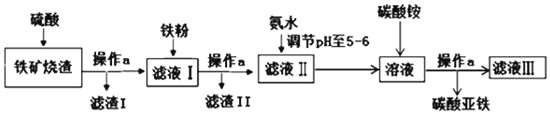
请回答下列问题:
(1)操作a中需要用到的玻璃仪器主要有烧杯、玻璃棒和__.
(2)滤液Ⅰ中含有的金属阳离子:Fe2+、__ (填离子符号).
(3)滤液Ⅰ中加入铁粉后可能发生的化学反应方程式:①__;②Fe+H2SO4=FeSO4+H2↑.
(4)“调节滤液Ⅱ的pH”的操作用__测定加入氨水后溶液的pH.
(5)加入碳酸铵得到碳酸亚铁的反应化学方程式:__.
-
碳酸亚铁(FeCO3)是生产补血剂的原料。以下是某同学设计的利用铁矿烧渣(主要成分为Fe2O3、FeO和泥沙等)制取碳酸亚铁的实验流程图:
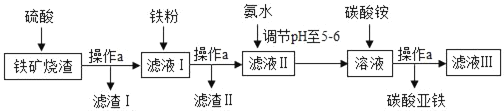
请回答下列问题:
(1)操作a中需要用到的玻璃仪器主要有烧杯、玻璃棒和_____。
(2)加入过量稀硫酸前要将铁矿烧渣粉碎的目的是_____滤液I中含有的溶质是:FeSO4、_____(填化学式)。
(3)滤液Ⅰ中加入铁粉后可能发生的化学方程式:
①Fe+Fe2(SO4)3=3FeSO4
②_____。
(4)加入碳酸铵得到碳酸亚铁的反应化学方程式:_____。
-
高纯氧化铁(Fe2O3)又称“引火铁”,可作催化剂,在现代工业上有广泛应用前景。以下是用赤铁矿(含少量不溶于水的SiO2等)为原料,制备高纯氧化铁的生产流程图。(资料:FeCO3难溶于水)
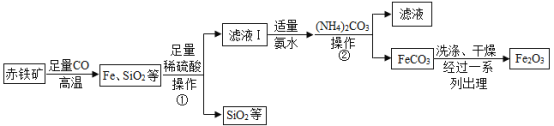
(1)写出高温时赤铁矿中的Fe2O3与CO发生反应的化学方程式___________________________。
(2)上述流程图中第2步实验加入足量稀硫酸后观察到的现象为:固体部分溶解,________________。
(3)操作②用到的玻璃仪器有________________。
(4)上述流程中加入碳酸铵时发生反应的基本反应类型是________________。
-
黄铁矿(主要成分为二硫化亚铁,FeS2)可用于工业制备硫酸(H2SO4),其所得矿渣中氧化铁(Fe2O3)含量较高,可用于高炉炼铁。其工业流程图如图所示:
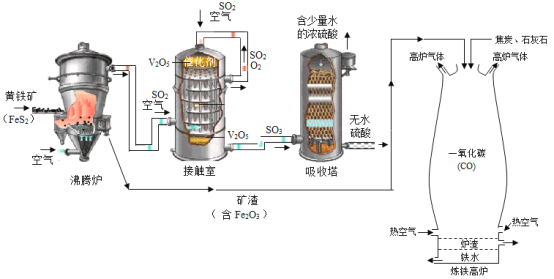
其中高炉炼铁的另两种原料分别为焦炭和石灰石(主要成分为CaCO3),其基本原理为:焦炭在高温下先转化为一氧化碳(CO),一氧化碳再与氧化铁(Fe2O3)在高温下反应制得铁。石灰石的作用是将杂质转化成炉渣除去。请回答下列问题:
(1)请将沸腾炉里的反应填写完整:4FeS2+11O2 2Fe2O3+______。
2Fe2O3+______。
(2)黄铁矿粉碎的目的是______。
(3)将从接触室中排出来的SO2和空气重新送回接触室的目的是______。
(4)试写出炼铁高炉中一氧化碳炼铁的化学方程式______。
-
黄铁矿(主要成分为二硫化亚铁,FeS2)可用于工业制备硫酸(H2SO4),其所得矿渣中氧化铁(Fe2O3)含量较高,可用于高炉炼铁。其工业流程图如图所示:
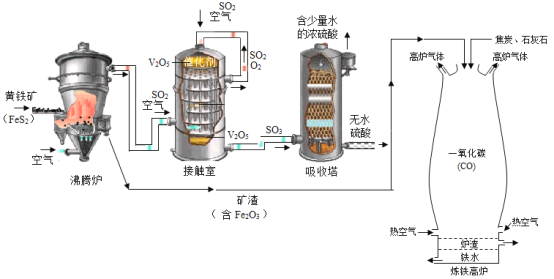
其中高炉炼铁的另两种原料分别为焦炭和石灰石(主要成分为CaCO3),其基本原理为:焦炭在高温下先转化为一氧化碳(CO),一氧化碳再与氧化铁(Fe2O3)在高温下反应制得铁。石灰石的作用是将杂质转化成炉渣除去。请回答下列问题:
(1)请将沸腾炉里的反应填写完整:4FeS2+11O2 2Fe2O3+______。
2Fe2O3+______。
(2)黄铁矿粉碎的目的是______。
(3)将从接触室中排出来的SO2和空气重新送回接触室的目的是______。
(4)试写出炼铁高炉中一氧化碳炼铁的化学方程式______。
-
高纯度的氧化铁可作现代电子工业的材料,以下是用硫铁矿烧渣(主要成分为FeO、SiO2)为原料制备Fe2O3的生产流程示意图。
(已知:1.(NH4)2CO3 溶液呈碱性,40℃以上时分解。2.(NH4)2CO3溶液和FeSO4 溶液能发生复分解反应。)

(1)实验室中,操作I、操作II需到的玻璃仪器有玻璃棒、烧杯、_____等 。
(2)根据题中信息,加入适量氨水的目的是_____。加入(NH4)2CO3后,该反应必须控制的条件是_____。
(3)滤液II经处理后可用作肥料,过量施用该肥料会造成_____。
(4)写出在空气中煅烧FeCO3 的化学反应方程式_____。










