-
工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图:

加热碳酸化吸氨纯碱饱和氨盐水碳酸钠饱和食盐水.其生产过程中有下列反应:① ;②
;② ;
;
碳酸氢钠和氯化铵的溶解度曲线如图所示.

请回答下列问题:
(1)30℃时,碳酸氢钠的溶解度是_____。
(2)30℃时,氯化铵饱和溶液中溶质质量分数_____碳酸氢钠饱和溶液中溶质质量分数(填“大于”“小于”“等于”之一)
(3)反应①中生成物碳酸氢钠和氯化铵的质量比为____:_____。
(4)氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,哪种物质首先结晶析出?____根据溶解度曲线和两者的质量关系分析原因_______。
-
工业上采用氨碱法生产纯碱(NaCO3),主要流程如图1:
(1)试剂A是 ,写出通入A步骤反应的化学方程式: .
(2)为什么要先吸氨,后碳酸化? .
(2)我国化学家侯德榜在氨碱法的基础上创立的“侯氏制碱法”,保留了氨碱法的优点,克服其缺点,即向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl,NaCl溶液则可循环使用.NH4Cl和NaCl的溶解度曲线如图2所示.

①二者中 的溶解度随温度的变化较大.
②将一定量t2℃时NH4Cl饱和溶液的温度降到t1℃,该过程没有发生改变的是 (从下列选项中选择)
A、溶液的质量 B、溶质的质量 C、溶剂的质量 D、溶质质量分数
③要使NH4Cl结晶析出而NaCl留在溶液中,通常将温度控制在较低范围(<t1℃),请说明理由 .
④NH4Cl可用作氮肥,在使用时应注意不能与熟石灰混合施用的原因是(用化学方程式表示) .
-
工业上采用氨碱法生产纯碱,是先向________中通入氨气,制成饱和氨盐水;在加压的条件下不断通入________,而使________结晶析出;将________加热分解即得纯碱.发生反应的化学原理是(填化学方程式):(1)________;(2)________.
-
我国化工专家侯德榜发明了“联合制碱法”,其生产过程中发生的反应主要是:其工业生产纯碱的工艺流程示意图如下所示,其中向粗盐水中加入的沉淀剂A、B分别为氧化钙和碳酸钠.
① NH3 + CO2 + H2O = NH4HCO3 ② NH4HCO3 + NaCl = NaHCO3↓ + NH4Cl ③ 2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
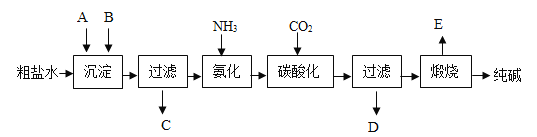
请回答下列问题:
(1)实验室提纯粗盐的实验操作依次为:取样、溶解、沉淀、过滤、蒸发结晶.若过滤时发现滤液中有少量浑浊,从实验操作的角度给出一种可能的原因:______.
(2)实验室中,用提纯得到的氯化钠配制100g 0.9%的生理盐水,使用的仪器除药匙、玻璃棒、托盘天平、胶头滴管、烧杯外,还需要适当的仪器是_________.
(3)生产纯碱的工艺流程中,碳酸化时析出NaHCO3晶体,没有析出Na2CO3晶体的原因是____。
(4)本工艺流程中氨(氨气)是循环使用的,为此,向滤液D中加入石灰水产生氨(氨气).写出该反应的化学方程式_________。
-
如图是工业生产纯碱的工艺流程示意图.

已知:①粗盐水中含有MgCl2、CaCl2;②常温下,NH3极易溶于水,CO2能溶于水,③NaHCO3加热易分解,Na2CO3加热不易分解.
完成下列填空:
(1)粗盐水加入沉淀剂NaOH、Na2CO3分别除去MgCl2、CaCl2,固体C为________,书写其中一个反应的化学方程式________;
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是________,“碳酸化”时,NaCl、NH3、CO2 和H2O相互作用析出NaHCO3,写出该反应的化学方程式________.
(3)“碳酸化”后过滤获得的NH4Cl可用作________肥,也可先________(填“加热”或“冷却”)NH4Cl溶液,再加入石灰水以循环使用的物质是________;
(4)“煅烧”时,NaHCO3分解生成的气体D是________,若将气体D直接排入空气不合理的理由是________.
(5)鉴别产品纯碱中是否含有碳酸氢钠的方法是________.
-
工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图1:

(1)在①〜③三个过程中,发生分解反应的是____________(填序号)
(2)侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图2所示,试回答下列问题:

①在t1℃时,Na2CO3的溶解度是____g
②t2℃时,NaCl的溶解度_______Na2CO3的溶解度(填“大于”“等于”“小于”之一)
③要从海水中提取NaCl,应采用的方法是_________________(填“蒸发结晶”或“降温结晶”)
④若把10g的Na2CO3加入50g水中,充分溶解后,得到t1℃的Na2CO3溶液的质量是___g
-
工业上采用氨碱法生产纯碱,纯碱是工业制取烧碱的一种原料,主要流程如图所示:
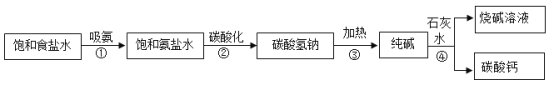
(1)在①﹣④四个过程中,发生了分解反应的是_____(填序号);
(2)上述物质中,在焙制糕点时常用作发酵粉的是_____(填化学式);
(3)实验小组的同学把质量分数为10%的Na2CO3溶液,逐滴加入到石灰水中,生成沉淀的质量与加入Na2CO3溶液的质量关系如图所示。请根据题意回答下列问题:
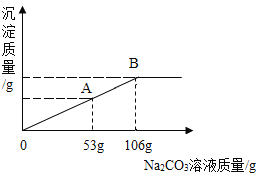
①当滴入Na2CO3溶液53g时(即图中A点),溶液里含有的溶质有_____(写化学式);
②当滴入10%的Na2CO3溶液106g时(即图中B点),恰好完全反应。试通过计算,求此时所得不饱和溶液中溶质的质量___。
-
下图是工业生产纯碱的工艺流程示意图。

已知:①粗盐水中含有MgCl2、CaCl2;②常温下,NH3极易溶于水,CO2能溶于水,③NaHCO3加热易分解,Na2CO3加热不易分解。
完成下列填空:
(1)粗盐水加入沉淀剂NaOH、Na2CO3分别除去MgCl2、CaCl2,固体C为________________,书写其中一个反应的化学方程式________________;
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是________,“碳酸化”时,NaCl、NH3、CO2 和H2O相互作用析出NaHCO3,写出该反应的化学方程式________。
(3)“碳酸化”后过滤获得的NH4Cl可用作________________肥,也可先________(填“加热”或“冷却”)NH4Cl溶液,再加入石灰水以循环使用的物质是________;
(4)“煅烧”时,NaHCO3分解生成的气体D是________,若将气体D直接排入空气不合理的理由是________。
(5)鉴别产品纯碱中是否含有碳酸氢钠的方法是 ________。
【解析】(1)NaOH和MgCl2生成Mg(OH)2沉淀,Na2CO3和CaCl2生成沉淀CaCO3,
(2)先“氨化”后“碳酸化”的目的是有利于溶液吸收溶液CO2气体
(3)NH4Cl中含有氮元素可用作氮肥,NH4Cl和氢氧化钙生成氯化钙和氨气和水
(4) NaHCO3分解生成碳酸钠,水,二氧化碳
(5) NaHCO3加热易分解,Na2CO3加热不易分解进行解答
-
工业上采用氨碱法生产纯碱,主要流程如下图,请据图回答相关问题。













(1)氨碱法生产所得产品为纯碱,向纯碱水溶液中滴入无色酚酞试液显________色。
(2)从步骤①提取粗盐常用____________(填“蒸发结晶”或“降温结晶”)的方法。
(3)从酸碱反应的角度分析,步骤④中通入氨气的作用是________________________________________。
(4)步骤⑤所得的碳酸氢钠在生产和生活中有许多重要用途,请写出它的一种用途________________。
(5)步骤⑥中发生反应的化学方程式为_________________________,该反应类型属于__________反应。
-
工业上采用氨碱法生产纯碱,主要流程如下图,请据图回答相关问题。

⑴氨碱法生产所得产品为纯碱,向纯碱水溶液中滴入无色酚酞试液显________色。
⑵从步骤①提取粗盐常用___________(填“蒸发结晶”或“降温结晶”)方法。
⑶从酸碱反应的角度分析,步骤④中通入氨气的作用是____________________。
⑷步骤⑤所得的碳酸氢钠在生产和生活中有许多重要用途,请写出它的一种用途______。
⑸步骤⑥中发生反应的化学方程式为______________,该反应类型属于________反应。
⑹工业产品中往往含有一些杂质,用“氨碱法”制得的纯碱含有少量氯化钠。为了测定该产品中碳酸钠的纯度,进行以下实验:取16.5g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150g稀盐酸(足量)加入样品中,观察读数变化如下表所示:
| 时间/s | 0 | 5 | 10 | 15 |
| 读数/g | 215.2 | 211.4 | 208.6 | 208.6 |
请你据此分析计算:
①实验中产生二氧化碳的质量为____________;
②该产品中碳酸钠的质量分数_______(写出计算过程,结果精确到0.1%)

;②
;












