1926 年,我国著名化学家侯德榜改进了国外的纯碱生产工艺,发明了“联合制碱法”,其主要流程如图所示。
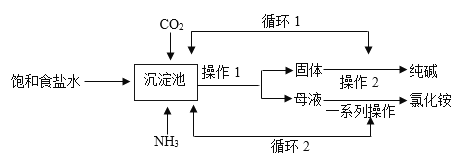
已知在沉淀池中发生的反应为:。
回答下列问题:
(1)操作1是_____(填操作名称)。
(2)操作2将固体充分加热,写出反应的化学方程式_____。
(3)“联合制碱法 ”使原料氯化钠的利用率从70%提高到96%,主要是因为设计了循环_____ (填数字序号)。
(4)纯碱样品中可能会含有少量氯化钠杂质。为了检验纯碱样品中是否含有氯化钠应选用的试剂是_____。
九年级化学流程题困难题
1926 年,我国著名化学家侯德榜改进了国外的纯碱生产工艺,发明了“联合制碱法”,其主要流程如图所示。

已知在沉淀池中发生的反应为:。
回答下列问题:
(1)操作1是_____(填操作名称)。
(2)操作2将固体充分加热,写出反应的化学方程式_____。
(3)“联合制碱法 ”使原料氯化钠的利用率从70%提高到96%,主要是因为设计了循环_____ (填数字序号)。
(4)纯碱样品中可能会含有少量氯化钠杂质。为了检验纯碱样品中是否含有氯化钠应选用的试剂是_____。
九年级化学流程题困难题
1926 年,我国著名化学家侯德榜改进了国外的纯碱生产工艺,发明了“联合制碱法”,其主要流程如图所示。

已知在沉淀池中发生的反应为:。
回答下列问题:
(1)操作1是_____(填操作名称)。
(2)操作2将固体充分加热,写出反应的化学方程式_____。
(3)“联合制碱法 ”使原料氯化钠的利用率从70%提高到96%,主要是因为设计了循环_____ (填数字序号)。
(4)纯碱样品中可能会含有少量氯化钠杂质。为了检验纯碱样品中是否含有氯化钠应选用的试剂是_____。
九年级化学流程题困难题查看答案及解析
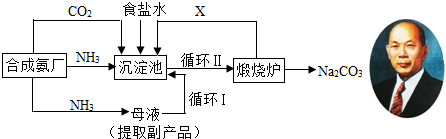
1926年的“联合制碱法”改进了国外的纯碱生产工艺,主要流程如图所示:
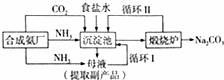
(1)它是由我国著名化学家 创立的。
(2)如何取出从沉淀池中不断结晶析出的碳酸氢钠: (填操作名称);碳酸氢钠在生产生活中的用途: (写出一种即可)。
(3)它使原料氯化钠的利用率从70%提高到96%,主要是因为设计了 (填流程图中的编号)的循环。
九年级化学填空题中等难度题查看答案及解析
1926年的“联合制碱法”改进了国外的纯碱生产工艺,主要流程如图所示:
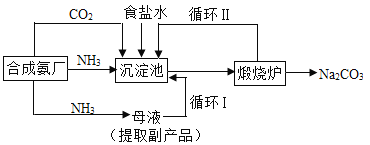
(1)它是由我国著名化学家________创立的。
(2)如何取出从沉淀池中不断结晶析出的碳酸氢钠:___(填操作名称);碳酸氢钠在生产生活中的用途:____(写出一种即可)。
(3)它使原料氯化钠的利用率从70%提高到96%,主要是因为设计了____(填流程图中的编号)的循环。
(4)沉淀池中制氨盐水的过程中要先通入氨气,再通入二氧化碳。如果反过来,二氧化碳的吸收率会降低。这是因为___。
九年级化学流程题中等难度题查看答案及解析
我国化学家侯德榜改革了国外的纯碱生产工艺,发明了联合制碱法,其生产流程可简要表示如下:
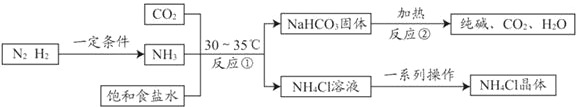
已知NH4Cl受热易分解,请回答下列问题。
(1)上述流程中可循环利用的物质是_____(写一种);
(2)反应②的化学方程式是_____;
(3)下表是几种物质在不同温度下的溶解度
| 温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | ﹣ | ﹣ | ﹣ | ﹣ | |
| NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | ﹣ | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.5 | 77.3 |
分析表中数据可知,反应①中NaHCO3作为固体析出的原因是_____;
上述流程中得到的NH4Cl溶液中一定有_____杂质,从NH4Cl溶液中获得NH4Cl晶体的一系列操作主要包括蒸发浓缩、_____、_____。
九年级化学流程题中等难度题查看答案及解析
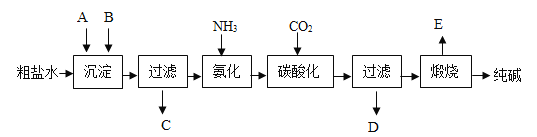
我国化工专家侯德榜发明了“联合制碱法”,其生产过程中发生的反应主要是:其工业生产纯碱的工艺流程示意图如下所示,其中向粗盐水中加入的沉淀剂A、B分别为氧化钙和碳酸钠.
① NH3 + CO2 + H2O = NH4HCO3 ② NH4HCO3 + NaCl = NaHCO3↓ + NH4Cl ③ 2NaHCO3Na2CO3+H2O+CO2↑
请回答下列问题:
(1)实验室提纯粗盐的实验操作依次为:取样、溶解、沉淀、过滤、蒸发结晶.若过滤时发现滤液中有少量浑浊,从实验操作的角度给出一种可能的原因:______.
(2)实验室中,用提纯得到的氯化钠配制100g 0.9%的生理盐水,使用的仪器除药匙、玻璃棒、托盘天平、胶头滴管、烧杯外,还需要适当的仪器是_________.
(3)生产纯碱的工艺流程中,碳酸化时析出NaHCO3晶体,没有析出Na2CO3晶体的原因是____。
(4)本工艺流程中氨(氨气)是循环使用的,为此,向滤液D中加入石灰水产生氨(氨气).写出该反应的化学方程式_________。
九年级化学流程题困难题查看答案及解析
九年级化学解答题中等难度题查看答案及解析
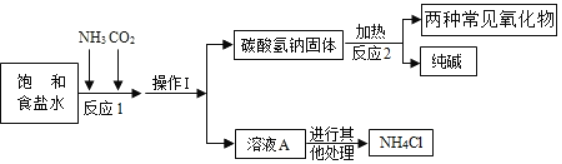
“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱与氯化铵的联合制碱工艺。
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示:
下列叙述不正确的是( )
A. 该过程操作1的名称是过滤
B. 该工艺流程可看出:该温度下碳酸氢钠的溶解度大于氯化铵的溶解度
C. 该过程涉及的物质中元素的化合价不发生改变
D. 图中反应2的化学方程式是2NaHCO3Na2CO3+CO2↑+H2O
九年级化学单选题困难题查看答案及解析
我国科学家侯德榜,在氨碱法的基础上,创立了更为先进的联合制碱法生产纯碱碳酸钠。某海边工厂利用贝壳、海盐等生产纯碱的主要工艺流程如图:
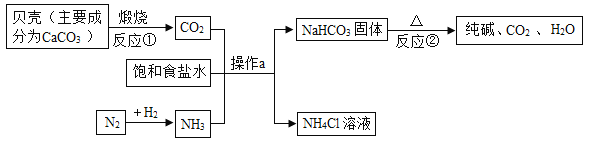
(1)反应①的化学方程式为____________,反应②属于_________反应(填基本反应类型)。
(2)工业上常用___________的方法制取氮气,该过程属于_________变化。
(3)操作a的名称是____________,实验室在进行该操作时,用到的玻璃仪器有烧杯、漏斗和____________。
(4)在工农业生产过程中,会排放CO2加剧温室效应。下列做法能减少二氧化碳排放的是______(填序号)。
a焚烧秸秆肥田
b提高火力发电量
c大力使用清洁能源
九年级化学流程题简单题查看答案及解析
我国科学家侯德榜,在氨碱法的基础上,创立了更为先进的联合制碱法生产纯碱碳 酸钠。某海边工厂利用贝壳、海盐等生产纯碱的主要工艺流程如下:

(1)反应①的化学方程式为_____。反应②属于_____反应(填基本反应类型)。
(2)工业上常用_____的方法制取氮气,该过程属于_____变化。
(3)操作 a 的名称是_____,实验室在进行该操作时,用到的玻璃仪器有烧杯、漏斗和_____。
(4)在工农业生产过程中,会排放 CO2 加剧温室效应。下列做法能减少二氧化碳排放的是_____(填序号)。
a 焚烧秸秆肥田 b 提高火力发电量 c 大力使用清洁能源
(5)有一种处理 CO2 的方法,是将 CO2 与氢气在一定条件下反应生成甲烷和水,该反应的化学方程式 为:_____。
九年级化学流程题困难题查看答案及解析
我国科学家侯德榜,在氨碱法的基础上,创立了更为先进的联合制碱法生产纯碱碳 酸钠。某海边工厂利用贝壳、海盐等生产纯碱的主要工艺流程如下:

(1)反应①的化学方程式为_____。反应②属于_____反应(填基本反应类型)。
(2)工业上常用_____的方法制取氮气,该过程属于_____变化。
(3)操作 a 的名称是_____,实验室在进行该操作时,用到的玻璃仪器有烧杯、漏斗和_____。
(4)在工农业生产过程中,会排放 CO2 加剧温室效应。下列做法能减少二氧化碳排放的是_____(填序号)。
a 焚烧秸秆肥田 b 提高火力发电量 c 大力使用清洁能源
(5)有一种处理 CO2 的方法,是将 CO2 与氢气在一定条件下反应生成甲烷和水,该反应的化学方程式 为:_____。
九年级化学流程题困难题查看答案及解析