-
小组同学通过学习发现甲烷的性质与氢气、一氧化碳有很多相似之处。
(提出问题)氢气、一氧化碳具有还原性,那么甲烷有没有还原性呢?
(查阅资料)1.无水硫酸铜是白色固体,吸收水分后变为蓝色。2.铁的氧化物与稀硫酸反应时无气体生成
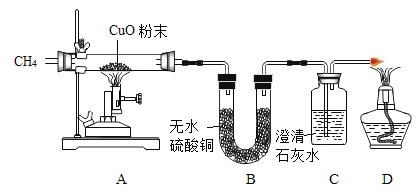
(实验探究)为探究上述问题,设计如下装置并进行实验。
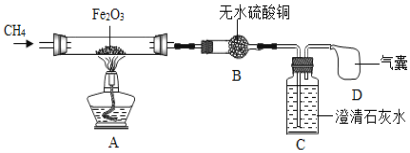
(1)实验开始时先通一段时间甲烷的目的是_____。
(2)加热一段时间后,观察到A中硬质玻璃管中的固体粉末由红色全部变成黑色,取少量黑色粉末于试管中,加入适量稀盐酸,观察到_____(填实验现象),说明有铁生成;B中白色固体变蓝,说明有_____生成;C中澄清石灰水变浑浊,说明有二氧化碳生成。
(结论)甲烷有还原性。若生成的黑色粉末全部是铁,甲烷还原氧化铁的化学方程式为_____。
-
甲,乙两位同学在学习甲烷性质时,发现甲烷与氢气和一氧化碳性质上有很多相似之处,如密度比空气小,难溶于水,具有可燃性等。H2和CO具有还原性,那么甲烷有没有还原性呢?为了验证甲烷是否具有还原性,乙同学设计如图所示装置并进行实验:
[实验装置]
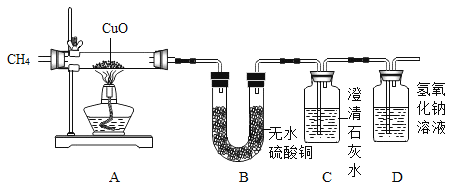
[实验步骤](假设药品都是足量的)
①分别称量装置A,B,C的质量;
②再次分别称量装置A,B,C的质量;
③向玻璃管中装入CuO,通入一段时间的CH4;
④停止加热,继续通入CH4至冷却到室温;
⑤缓缓通入足量的CH4,加热装置A,使其充分反应。
其合理的操作顺序是_____(填序号)。甲同学认为还缺少一个步骤,缺少的步骤是_____。
[进行实验]乙同学按照正确的步骤进行实验,并记录了实验现象和数据:
装置A中的黑色粉末变红;装置B中白色粉末变蓝;装置C中石灰水变浑浊;称量数据如表所示。
| A中玻璃管(含药品)质量 | 装置B的质量 | 装置C的质量 |
| 反应前 | 150 g | 156.6 g | 256.8 g |
| 反应后 | 147.2 g | 158.4 g | 257.9 g |
[现象分析与数据处理]
根据装置A,B,C中的现象可推知,CH4与CuO充分反应后的产物依次是_____。
[实验结论]
(1)CH4 _____(填“有”或“没有”)还原性;
(2)根据实验数据,甲同学提出甲烷与氧化铜反应的产物中还含有_____;
(3)装置A中发生的反应化学方程式为_____。
-
甲、乙两位同学在学习甲烷的性质时,发现甲烷与氢气和一氧化碳在性质上有很多相似之处,如密度比空气小,难溶于水,具有可燃性等。但H2和CO都具有还原性,那么甲烷有没有还原性呢?为了验证甲烷是否具有还原性,乙同学设计以下实验装置并进行实验探究:
[实验装置]
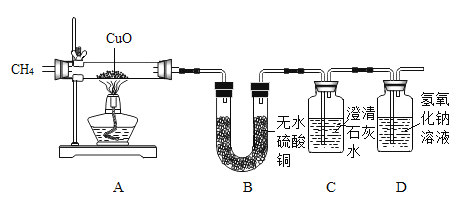
[查阅资料]白色无水CuSO4遇水变蓝,有吸水性。
[实验步骤](假设药品都是足量的,氢氧化钠溶液的作用是防止空气中的CO2进入装置C)
①分别称量装置A、B、C的质量;②向玻璃管中装入CuO;③先通一段时间的CH4,再加热装置A,使其充分反应;④停止加热,继续通入CH4至玻璃管冷却到室温;⑤再次分别称量装置A、B、C的质量。
先通一段时间的CH4,再加热装置A的目的是_____。甲同学认为还缺少一个步骤,缺少的步骤是_____。
[进行实验]乙同学按照正确的步骤进行实验,并记录了实验现象和数据
装置A中的黑色粉末变红;装置B中白色粉末变蓝;装置C中石灰水变浑浊;称量数据如下表所示
| 装置A中玻璃管(含药品)的质量 | 装置B的质量 | 装置C的质量 |
| 反应前 | 150g | 156.6g | 256.8g |
| 反应后 | 147.2g | 158.4g | 257.9g |
[现象分析与数据处理]
根据装置ABC中的现象可推知,CH4与CuO充分反应后的产物依次是_____、_____、_____。
[实验结论]
(1)CH4_____ (填“有”或“没有”)还原性。
(2)根据实验数据,甲同学提出甲烷与氧化铜反应的产物中还有一氧化碳,生成一氧化碳的质量为_____克。
(3)装置A中发生反应的化学方程式为_____。
-
课题式学习是研究性学习的一种方式,其基本学习模式为:提出问题→确定研究方案→解决问题→总结和评价
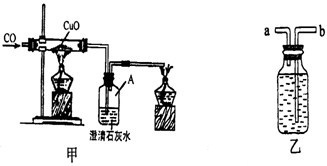
某校研究性学习小组的同学在“一氧化碳的化学性质”的学习中,设计了证明CO具有还原性的实验装置(如图甲),根据其研究过程请你回答下列问题:
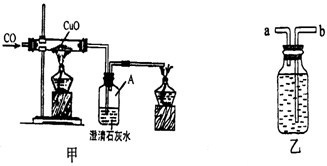
(1)实验过程中,洗气瓶A中的实验现象________.
(2)小余同学认为此装置有待优化,如尾气可先储存在瓶内,然后再处理.如图乙是他设计的贮气瓶,尾气应从________(选a、b填空)口通入.
(3)小徐同学质疑:CO能否使澄清石灰水变浑浊?因此进行设计:在CO通入CuO之前先通过澄清石灰水(即在盛CuO的硬质玻璃管的左端再接入一个盛澄清石灰水的洗气 瓶),来确定CO能否使澄清石灰水变浑浊.请判断小徐的设计是否有必要,并说明理由________.
-
课题式学习是研究性学习的一种方式,其基本学习模式为:提出问题→确定研究方案→解决问题→总结和评价
某校研究性学习小组的同学在“一氧化碳的化学性质”的学习中,设计了证明CO具有还原性的实验装置(如图甲),根据其研究过程请你回答下列问题:
(1)实验过程中,洗气瓶A中的实验现象________.
(2)小余同学认为此装置有待优化,如尾气可先储存在瓶内,然后再处理.如图乙是他设计的贮气瓶,尾气应从________(选a、b填空)口通入.
(3)小徐同学质疑:CO能否使澄清石灰水变浑浊?因此进行设计:在CO通入CuO之前先通过澄清石灰水(即在盛CuO的硬质玻璃管的左端再接入一个盛澄清石灰水的洗气 瓶),来确定CO能否使澄清石灰水变浑浊.请判断小徐的设计是否有必要,并说明理由________.
-
(2003•天津)通过化学学习,你是否已经体会到化学就在我们的身边?例如我们初步了解了氢气、一氧化碳、二氧化碳和甲烷等气体的一些重要性质.其中具有还原性,可用于冶炼金属的化合物是;可供家庭用的气体化石燃料的主要成分是;加压降温后的固体可用作致冷剂的是,燃烧物无污染,可作高能燃料的是.
-
通过化学学习,你是否已经体会到化学就在我们的身边?例如我们初步了解了氢气、一氧化碳、二氧化碳和甲烷等气体的一些重要性质.其中具有还原性,可用于冶炼金属的化合物是______;可供家庭用的气体化石燃料的主要成分是______;加压降温后的固体可用作致冷剂的是______;燃烧产物无污染,可作高能燃料的是______.
-
分类是研究物质的一种重要方法,同类物质具有相似的化学性质。学习完二氧
化碳的性质后,某化学兴趣小组的同学发现氢氧化钾与氢氧化钙的组成相似,设计
实验探究二氧化碳能否与氢氧化钾发生反应。
(1)实验准备
查阅资料:通常状况下,1体积的水约能溶解1体积二氧化碳。
(2)实验过程
【方案一】同学们取少量氢氧化钾溶液于试管中,向该溶液中通入二氧化碳气体,无明显现象。得出结论:二氧化碳不能与氢氧化钾发生反应。有的同学提出该结论不正确,理由是_______________________。
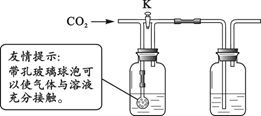
【方案二】在老师的帮助下,同学们利用下面的装置,通过实验证明二氧化碳与氢氧化钾确实发生了化学反应。
A B
分别取氢氧化钾和氢氧化钙溶液放入A、B中,
① 关闭K,通入二氧化碳 ,A、B中均无明显变化。B中盛放的溶液是_____。
② 打开K,继续通入二氧化碳。B中溶液变浑浊。B中反应的化学方程式为_____。
同学们依据上述实验现象,得出二氧化碳与氢氧化钾确实发生了化学反应。有同学
认为上述实验不足以证明二氧化碳和氢氧化钾发生了反应,其理由是_____。
③ 同学们用洗涤干净的上述装置重新实验,分别量取50 mL上述溶液放入A、B中,
关闭K,通入约500 mL二氧化碳,A、B中均无明显变化。此实验可以说明二氧化碳和氢氧化钾发生了反应,其理由是_____。
(3)实验反思
通过上述实验说明,对于没有明显现象的化学反应,可以从________的角度证明反应的发生。
-
善于提出问题、探究问题和解决问题是学好化学的重要法。某研究性学习小组的同学在学习铁及其化合物知识时进行了系列研究。
Ⅰ.提出问题:
问题1:铁有多种氧化物,它们的性质有哪些差异?
问题3:用一氧化碳还原氧化铁得到的黑色固体一定是单质铁吗?
Ⅱ.解决问题
【问题1】查询资料:
a.铁常见的氧化物有氧化铁(Fe2O3)、四氧化三铁(Fe3O4)和氧化亚铁(FeO)。
b.四氧化三铁是具有磁性的黑色晶体,可以被磁铁吸引。它不溶于水,可以近似地看作是氧化亚铁和氧化铁的化合物,能与酸反应生成两种盐。
C.氧化亚铁是不溶于水的黑色粉末,能与酸反应,无磁性,不能被磁铁吸引。
(1)请写出四氧化三铁与盐酸反应的化学方程式______________
(2)有一包黑色粉末,可能是铁粉、Fe3O4粉末、FeO粉末中的一种。请你设计一种实验方案进行鉴别。
| 实验步骤 | 实验现象及结论 |
| 步骤一:取少量样品用磁铁吸引 | 现象:_________________ |
| 步骤二:_________________ | _________________ |
【问题2】同学们查阅资料得知CO与氧化铁反应,在不同的温度下,氧化铁因失氧程度不同而生成其他铁的氧化物(或铁单质)和CO2.小组同学设计了如图1所示的实验装置测定一氧化碳与氧化铁反应后的固体产物。
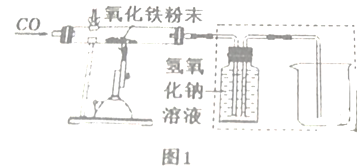
(3)实验开始应通入一氧化碳,再点燃酒精灯,目的是_________________________。
【注意】若答对以下问题奖励4分,化学试卷总分不超过60分。
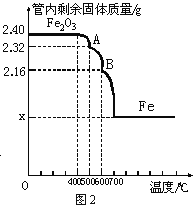
(4)同学们采集了用某种热分析仪记录的CO与氧化铁反应的有关数据,并得到固体质量与反应温度的关系曲线,如图2所示。根据相关信息,回答如下问题:
①图1虚线中装置的具体作用是____________________。
②在0~400℃温度范围内,管内固体质量不变,其原因是____________
③图中X=___________g,B点剩余固体的化学式是______________。
-
甲烷(CH4) 与CO、H2的性质有诸多相似处:难溶于水、具有可燃性等。而CO、H2都能还原金属氧化物,那么甲烷(CH4)能否还原氧化铜?若能反应,产物有哪些?校兴趣小组针对于此,称取4. 0g氧化铜粉末,展开探究:
[查阅资料]①无水CuSO4为一种白色固体,其遇水变蓝;
②Cu和Cu2O均为红色固体,且 。
。
[进行实验]甲同学组装装置并检查其气密性良好。通入纯净、干燥的CH4后,乙同学提醒CH4有可燃性,在点燃A处酒精喷灯前,需从C装置后尖嘴导管处收集气体并______________。D处燃着酒精灯的作用主要是处理多余的CH4,请写出发生反应的化学方程式___________。
[实验现象] A中黑色粉末逐渐变红; B中白色固体变蓝; C中澄清石灰水变浑浊。
[产物分析]结合实验现象,可以判断:甲烷能够还原氧化铜。
甲同学认为:实验后,装置A中所得红色固体全部为单质铜,并结合装置B、C实验现象,书写出甲烷与氧化铜反应完全转化为单质铜的化学方程式_______________________。
乙同学认为:实验后,装置A中所得红色固体并不一定全部为单质铜,理由是_______________________。
[定量测定]
小组同学待装置冷却后,停止通CH4,测得A中红色粉末的质量为3.4g.若CH4将4.0g,氧化铜完全还原为铜单质,则理论上所得铜单质的质量应该为_______________________;故所得红色粉末中一定含有氧化亚铜。
另一小组为进一步确定该红色粉末中氧化亚铜的质量,该小组同学将上述3.4g红色粉末置于试管中加入足量稀硫酸,加热并充分振荡,静置。观察到:红色固体逐渐减少,但未完全溶解,溶液由无色变蓝色。再将实验所得物质进行过滤、洗涤、干燥,称量,最终所得红色固体的质量为2.4g。通过计算确定原3.4g红色固体中氧化亚铜的质量(请写出计算过程)_____________________。








