-
过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,可以由鸡蛋壳(含CaCO3高达90%)为原料制得,其制备流程如下:
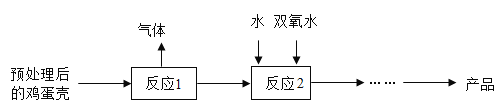
(1)反应1为高温煅烧碳酸钙,其化学方程式为_____。
(2)反应2的化学方程式为:CaO + H2O2 + 7H2O CaO2·8H2O,该反应属于化合反应。CaO2·8H2O属于_____(填字母序号)。
CaO2·8H2O,该反应属于化合反应。CaO2·8H2O属于_____(填字母序号)。
A 混合物 B 纯净物 C 化合物
(3)反应2制得的CaO2·8H2O中,可能含有的固体杂质是_____(填化学式)。
-
过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,通常有两种制备方法。已知:温度过高过氧化物会分解生成氧化物和氧气。
方法 1:由Ca(OH)2为原料最终反应制得,其制备流程如图:
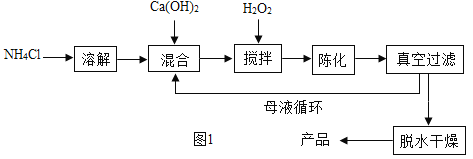
方法 2:由鸡蛋壳(含CaCO3高达 90%)为原料最终反应制得,其制备流程如图:
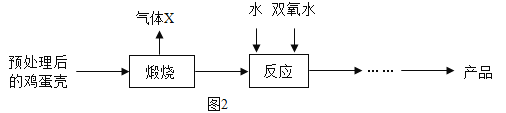
(1)方法 1 中搅拌的目的是_____。请将搅拌过程中发生反应的化学方程式补充完整 _____
_____ .制备过程中除水外可循环使用的物质是_____(填化学式)。
.制备过程中除水外可循环使用的物质是_____(填化学式)。
(2)方法 2 中气体 X 是_____,实验室常用_溶液来吸收。煅烧后的反应是化合反应,也能生成CaO2•8H2O,反应的化学方程式为_____。该反应需控制温度在 0~2℃,可将反应器放置在_,获得的CaO2产品中主要含有的固体杂质是_(填化学式)。
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高会造成氨水挥发外,还能_____。
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO2•8H2O的反应符合“绿色化学”的是________(填“方法 1”或“方法 2”)。
-
(10分)过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,通常有两种制备方法。已知:温度过高过氧化钙会分解生成氧化物和氧气。
方法1:由Ca(OH)2为原料最终制得,其制备流程如下:
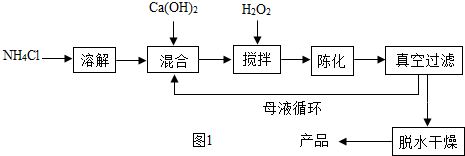
方法2:由鸡蛋壳(含CaCO3高达90%)为原料最终反应制得,其制备流程如下:
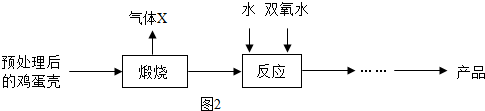
(1)方法1中搅拌的目的是 。请将搅拌过程中发生反应的化学方程式补充完整:
CaCl2 + H2O2 + 2NH3·H2O + 6 = CaO2·8H2O↓+ 2NH4Cl。制备过程中除水外可循环使用的物质是 (填化学式);
(2)方法2中气体X是 ,实验室常用 溶液来吸收。煅烧后的反应时化合反应,也能生成CaO2·8H2O,反应的化学方程式为 。该反应需控制温度在0 ~ 2℃,可将反应器放置在 中,获得CaO2产品中主要含有的固体杂质是 (填化学式);
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高除了防止氨水挥发外,还能 ;
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO2·8H2O的反应符合“绿色化学”的是 (填“方法1”或“方法2”)。
-
过氧化钙( CaO2)微溶于水,溶于酸,是一种对环境友好的多功能化合物。以下是制备过氧化钙的工艺流程图:
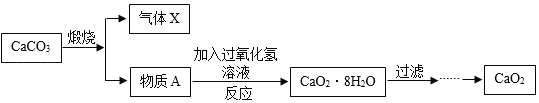
请回答下列问题:
(1)气体X是___________(填化学式),实验室常用澄清石灰水来检验X,该反应的化学方程式为____________。
(2)玻璃棒在过滤操作中所起到的作用是__________。下列是某同学进行过滤操作时的一些做法,其中正确的是___________(填字母序号)。
A直接向漏斗中倾倒待过滤的液体 B滤纸边缘高于漏斗边缘
C漏斗下端管尖紧靠烧杯内壁 D用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(3)写出由物质A反应生成CaO2·8H2O的化学方程式____________。
-
工业产品过氧化钙晶体(CaO2·8H2O)较稳定,呈白色,微溶于水,广泛用于环境杀菌、消毒。以贝壳(主要成分是 CaCO3,杂质不参加反应也不溶于水)为原料制备 CaO2的流程如下:
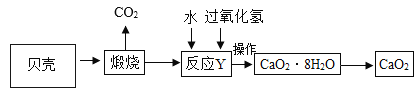
(1)CaO2中氧元素的化合价为___________;
(2)上述流程中将过氧化钙晶体从溶液中分离的步骤是过滤,该操作中用到的玻璃仪器有玻璃棒、 烧杯和_______________,其中玻璃棒的作用是_______________;
(3)反应 Y 需要在低温条件下进行,其原因是_________________;
(4)获取的 CaO2 中常含有 Ca(OH)2 杂质,原因是_______________(用化学方程式表示)。
-
过氧化钙(CaO2)是一种多功能无机化合物,通常由Ca(OH)2为原料制得,制备流程如下:

(1)原料中NH4Cl中氮元素的化合价是 ,NH4Cl中氮元素的质量分数为 %(精确到 0.1%)。
(2)请将搅拌过程中发生反应的化学方程式补充完整:
CaCl2 + H2O2 + 2NH3·H2O + 6 = CaO2·8H2O↓+ 2NH4Cl。制备过程中除水外可循环使用的物质是 (填化学式)。
-
过氧化钙(CaO2)是一种多功能无机化合物,通常由Ca(OH)2为原料制得,制备流程如下:
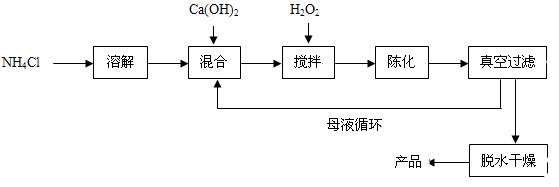
(1)原料中NH4Cl中氯元素的化合价是 ,NH4Cl是属于 肥(填化肥的种类)。
(2)搅拌过程中发生反应的化学方程式:CaCl2 + H2O2 + 2NH3·H2O + 6H2O = CaO2·8H2O↓+ 2 NH4Cl。
制备过程中除水外可循环使用的物质是 (填化学式)。
(3) 工业上也可用熟石灰和水、双氧水发生化合反应,也能生成CaO2•8H2O,反应的化学方程式 为 ,但这种方法获得产品中含有其他固体杂质。
-
过氧化钙( CaO2)是用途广泛的优良供氧剂。以电石渣[主要成分为Ca(OH)2,含少量CaCO3]为原料制备CaO2的一种工艺流程如下:
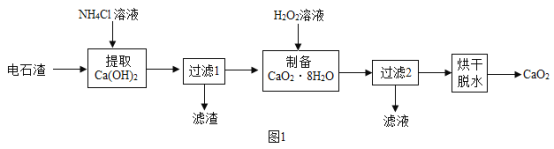
(查阅资料)I. Ca(OH)2+2NH4Cl=CaCl2+2NH3·H2O
Ⅱ.CaCl2+2NH3·H2O+H2O2 +6H2O= CaO2·8H2O↓+ 2NH4Cl
Ⅲ. CaO2·8H2O在水中不太稳定,会缓慢分解。
(1)“提取Ca(OH)2”时反应的基本类型是_______;Ca(OH)2的俗名为_______;“过滤1”所得滤渣的主要成分是_______。
(2)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“二低”指的是:滤纸边缘略低于漏斗口、_______。生产过程中为了精确测定溶液的pH,常使用_______ (填仪器名称)。
(3)在其他条件不变的情况下,制备CaO2·8H2O的反应时间(t)对其产率(w)的影响如图所示。
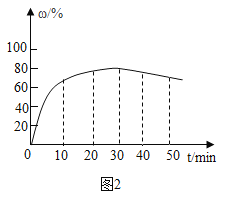
①平均反应速率最快的时间段为:_______ (填字母)。
a. 0~10min b. 10~20min c. 20~30min d.30~40min
②30min后,w开始下降的主要原因是_______。
(4)为了测定加入的NH4Cl溶液中溶质的质量分数,取30.00g NH4Cl溶液于烧杯中,加入稍过量的AgNO3溶液,完全反应后过滤、洗涤、干燥、称量,得到14.35g 白色固体。通过计算确定该溶液中NH4Cl的质量分数(精确到0.1%)____。
-
过氧化钙( CaO2)是用途广泛的优良供氧剂。以电石渣[主要成分为Ca(OH)2,含少量CaCO3]为原料制备CaO2的一种工艺流程如下:
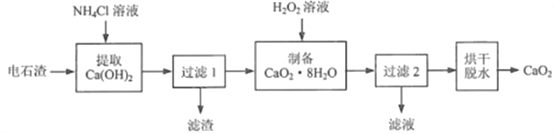
(查阅资料)I. Ca(OH)2+2NH4Cl=CaCl2+2NH3·H2O
Ⅱ.CaCl2+2NH3·H2O+H2O2 +6H2O= CaO2·8H2O↓+ 2NH4Cl
Ⅲ. CaO2·8H2O在水中不太稳定,会缓慢分解。
(1)“提取Ca(OH)2”时反应的基本类型是_______;Ca(OH)2的俗名为_______;“过滤1”所得滤渣的主要成分是_______。
(2)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“二低”指的是:滤纸边缘略低于漏斗口、_______。生产过程中为了精确测定溶液的pH,常使用_______ (填仪器名称)。
(3)在其他条件不变的情况下,制备CaO2·8H2O的反应时间(t)对其产率(w)的影响如图所示。
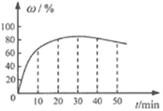
①平均反应速率最快的时间段为:_______ (填字母)。
a. 0~10min b. 10~20min c. 20~30min d.30~40min
②30min后,w开始下降的主要原因是_______。
(4)为了测定加入的NH4Cl溶液中溶质的质量分数,取30.00g NH4Cl溶液于烧杯中,加入稍过量的AgNO3溶液,完全反应后过滤、洗涤、干燥、称量,得到14.35g 白色固体。通过计算确定该溶液中NH4Cl的质量分数(精确到0.1%)____。
-
过氧化钙品体(CaO2·8H2O)较稳定,呈白色,微溶于水,广泛应用于环境杀菌消毒。以贝壳为原料制备CaO2的流程如下:
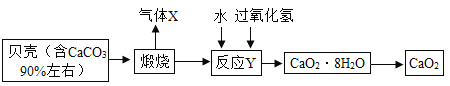
(1)过氧化钙晶体(CaO2·8H2O)较稳定,呈白色,微溶于水,厂泛应用于环境杀菌、消毒。这句话中描叙了过氧化钙的哪些物理性质____(任意答两点),CaO2中O元素的化合价为___价。
(2)气体X的化学式是____;将过氧化钙晶体与溶液分离的方法是____。
(3)贝壳煅烧的产物之一是生石灰(CaO),反应Y发生的是化合反应,反应产物是CaO2·8H2O,请写出该反应的化学方程式____。


_____
.制备过程中除水外可循环使用的物质是_____(填化学式)。











