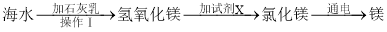-
海水中蕴藏着丰富的资源,含有的盐类物质总量有5×1016吨(如氯化钠、氯化镁、氯化钙、氯化钾等)。某工厂对海水综合利用的主要流程如下。
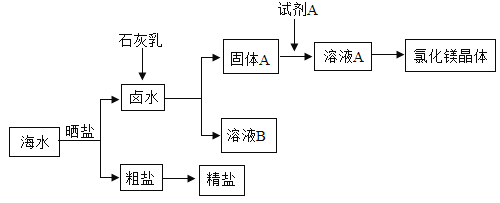
(1)海水晒盐的过程实际上是_______(填结晶的一种类型)的过程。卤水一定是______(填名称)的饱和溶液。
(2)试剂A与固体A发生反应的化学方程式为________。
(3)石灰乳的主要成分是_______(填化学式)。请写出该物质的一种重要用途________。
(4)由粗盐经过初步提纯(除去难溶性杂质)可得到精盐。实验的主要步骤有:①溶解;② _____;③蒸发。在溶解过程中用到的玻璃仪器有_______、玻璃棒。溶解时用玻璃棒搅拌的目的是_____,如果该操作不够准确,会导致得到的精盐质量_____(填“偏大”、“偏小”、“无影响”)。最终得到的精盐属于_______(填“混合物”、“纯净物”)。
(5)溶液A中的金属阳离子符号是________。
-
阅读下面的科普材料。
浩瀚的海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还蕴藏着丰饶的矿产;而海水本身含有大量的化学物质,又是宝贵的化学资源。海水中含有多种盐类,如氯化钠、氯化镁、硫酸钙等。
利用海水制盐的方法在我国仍以蒸发法为主,它的原理很简单,即在太阳照射后,海水受热使水分蒸发,当各种盐分别达到其饱和浓度时,依次以固态形式析出。随着科学和技术的进步,人们还利用其他方法从海水中制盐,如电渗析法、冷冻法等,用这两种方法不但可以制盐,同时也可以得到淡水。
食盐不仅是人类生活所不可缺少的物质,还是一种重要的化工原料。例如,作为基本化学工业之一的氯碱工业,就是通过电解饱和食盐水的方法得到氢氧化钠、氯气和氢气,并进而生产盐酸、漂白粉、塑料、肥皂和农药等,其他如造纸、纺织、印染、有机合成和金属冶炼等,也都离不开由食盐制得的化工产品。
海水可以提取食盐,还是个巨大的资源宝库。可以得到溴、镁等物质。目前,从海水中提取的溴约占世界溴年产量的三分之一。常用的技术叫做吹出法,即用氯气与溴化钠在酸性条件下反应,使其转变为溴后,用空气将其吹出。也可以用水蒸气,使溴和水蒸气一起蒸出。
而海水中的镁,则更是一种重要的资源。工业规模海水提镁的方法,是将海水抽入反应槽中,加入石灰乳,将海水中的镁转变为沉淀;再加入稀盐酸转化为氯化镁溶液,过滤、烘干,然后电解熔融状态的氯化镁就得到镁和氯气;氯气可以用来制取盐酸,再循环使用。
从海水得到的粗盐中含有泥沙、氯化钙、氯化镁、硫酸钠等杂质,用于电解法制碱必须经过精制。精制食盐水常加入一些试剂,使杂质沉淀过滤出来,再加入稀盐酸调节盐水的pH。
回答下列问题:
(1)根据材料可知,从海水中提取溴常用的技术叫做_______。
(2)铝和镁一样,属于活泼金属,铝在常温下具有较强抗腐蚀性的原因是_______。
(3)如果加入稀盐酸后盐水的pH=7,则溶液显_______性。
(4)根据材料可知,电解饱和食盐水的化学方程式为_______。
(5)要除去粗盐中含有的Na2SO4、MgCl2、CaCl2等可溶性杂质,可加入氢氧化钠溶液、碳酸钠溶液。其中,加入氢氧化钠溶液是为了除去_____; 在除去上述杂质时,应该先除去,________(选填“Na2SO4”或“CaCl2”)。
-
海水中除含有大量氯化钠外,还含有氯化镁、氯化钙等物质,是巨大的资源宝库。下图是某工厂对海水资源综合利用的示意图。
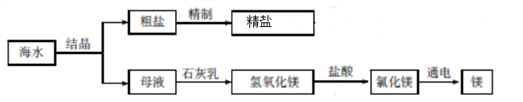
(1)蒸发结晶用到的玻璃仪器除除酒精灯外还有________,该仪器的作用是_________________。
(2)母液和石灰乳反应的化学方程式是______________________。
(3)粗盐的提纯的步骤有________、过滤、___________ 。
-
海水是巨大的资源宝库。下图是某工厂对海水资源综合利用的示意图:
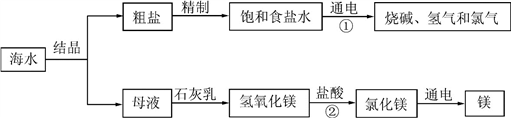
(1)分离粗盐和母液的操作名称为_____________;母液中一定含有的金属元素为_________;
(2)下表为氯化钠在不同温度时的溶解度。请结合表中数据回答问题:
| 温度/℃ | 30 | 50 | 70 | 100 |
| 溶解度/g | 36.3 | 37.0 | 37.8 | 39.8 |
从海水中获取粗盐,宜选用________(选填“蒸发结晶”或“降温结晶”)。
-
浩瀚的海洋蕴藏着丰富的化学资源,我们可以从海水中提取氯化钠等化工原料.现有一包从海水中获得的粗盐,已经过初步提纯,还含有杂质氯化镁、氯化钙.课外活动小组设计了以下提纯方案.(右图是室温时部分物质的溶解性表)
阴离子
阳离子 | OH- | Cl- | NO3- | CO32- |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Mg2+ | 不 | 溶 | 溶 | 微 |
| Ca2+ | 微 | 溶 | 溶 | 不 |
| 实验步骤 | 现象 | 结论或化学方程式 |
| (1)取样品加水溶解,向其中加入过量的氢氧化钠溶液 |
________ | 加入过量氢氧化钠溶液的目的 |
(2)过滤,向滤液中加入过量的
________ | 有白色沉淀 | 化学方程式为________ |
| (3)过滤 | 滤液澄清 | 滤液中含有的溶质________ |
| (4)向上述滤液中加入适量的________,然后将液体倒入蒸发皿中,加热并不断搅拌,直至________时,停止加热. | 有白色晶体 | 得到纯净的氯化钠 |
-
海水蕴藏着丰富的资源.
(1)海水中溶剂 是 .
(2)从海水中提取粗盐一般可采用 方法.
(3)如图1是特殊情况下使用的应急净水器.利用该净水器将2000g含氯化钠3%的海水暴晒4小时,收集到500g可饮用水,此时剩余海水中氯化钠的质量分数为 .
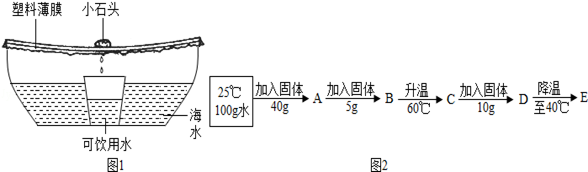
(4)利用氯化钠制备碳酸钠的同时可以得到氯化铵,下表为氯化铵的溶解度:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
①向100g水中不断加入氯化铵固体或改变温度,得到图2相应的溶液A~E.溶液D是 (填“饱和”或“不饱和”)溶液,溶液E中析出晶体 g.
②将盛有溶液E的小烧杯放入盛有水的大烧杯中,向大烧杯内加入NaOH固体,小烧杯内的固体溶解,原因是 .
-
海水蕴藏着丰富的资源.
(1)海水中溶剂 是________.
(2)从海水中提取粗盐一般可采用________方法.
(3)如图1是特殊情况下使用的应急净水器.利用该净水器将2000g含氯化钠3%的海水暴晒4小时,收集到500g可饮用水,此时剩余海水中氯化钠的质量分数为________.
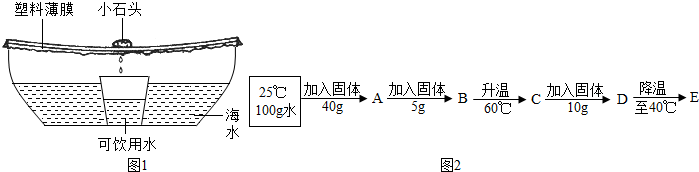
(4)利用氯化钠制备碳酸钠的同时可以得到氯化铵,下表为氯化铵的溶解度:
| 温度/℃ | | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
①向100g水中不断加入氯化铵固体或改变温度,得到图2相应的溶液A~E.
溶液D是________(填“饱和”或“不饱和”)溶液,溶液E中析出晶体________g.
②将盛有溶液E的小烧杯放入盛有水的大烧杯中,向大烧杯内加入NaOH固体,小烧杯内的固体溶解,原因是________.
-
已知海水中含有氯化镁,但因其含量低而不能用于生产镁.某工厂利用海水和海边丰富的贝壳(主要成分是CaCO3)资源来制取氢氧化镁,然后制取较纯净的氯化镁,并再用于生产镁.写出制取氯化镁的有关反应的化学方程式________.
-
海洋蕴藏着丰富的自然资源。工业上可利用海水中的氯化镁来制取金属镁,其简化后的流程如图所示:
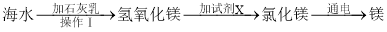
(1)操作Ⅰ的名称是_____。
(2)石灰乳与海水混合发生反应的化学方程式为_____。
(3)试剂X的主要成分为_____(写化学式)。
(4)氯化镁在熔融状态下通电得到金属镁和一种气体单质,它属于基本反应类型中的_____反应。
-
海洋是巨大的资源宝库,蕴藏着非常丰富的海洋资源,开发前景远大。
(1)海盐是人类最早从海洋中获取的矿物质之一。从海水中提取食盐的方法主要为盐田法,所得到的母液是当时温度下氯化钠的_________溶液(填“饱和”或“不饱和”)。
(2)金属镁广泛应用于生活、生产和国防工业,从卤水中提取镁的过程如图所示。
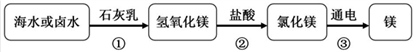
在上述转化过程中,所发生的化学反应属于中和反应的是___________(填反应序号)。
(3)我国化学家侯德榜在氨碱法的基础上创立的“侯氏制碱法”,是向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl。NH4Cl和NaCl两种物质的溶解度曲线如下图所示。
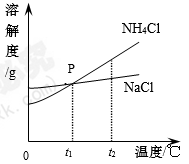
①t1℃时,NH 4Cl的溶解度___________ NaCl的溶解度(填写“大于”“等于”“小于”之一)。
②若把t1℃ 时NH4Cl和NaCl的饱和溶液(无固体剩余),均升温到t2℃,则t2℃ 时NH4Cl溶液的溶质质量分数____________NaCl溶液的溶质质量分数(填“大于”、“小于”、“等于”之一)。
③已知t1℃时,NH4Cl的溶解度为36g;t2℃时,NH4Cl的溶解度为60g。在t1℃时,向盛有200g水的烧杯中加入90g NH4Cl固体,充分溶解,然后使烧杯内物质缓慢升温至t2℃,则此时所得溶液中溶质与溶剂的质量之比为__________(填最简整数比)。