-
(2019河南省实验一模改编)Na2CO3在工业和生活中有重要的作用。它的来源主要有以下两种途径:
Ⅰ、将制碱与制氨结合起来的联合制碱法。这个方法是由我国的制碱工业先驱_____发明的。
A 张青莲 B 道尔顿 C 侯德榜 D 华罗庚
Ⅱ、自然界有很多咸水湖,人们通过“冬天捞碱,夏天晒盐”的方式获得湖盐,其中就含有Na2CO3。
(1)小明同学想对某夏天制得的湖盐样品成分进行探究,查阅资料后他对样品成分做出了三种猜想。猜想一:NaCl、Na2CO3;猜想二:NaCl、Na2SO4;猜想三:NaCl、Na2CO3、Na2SO4.请帮助他完成如下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取少量样品于试管中,加适量水溶解后,加入过量稀HNO3 | 产生能使澄清石灰水变浑浊的气体 | ①猜想_____不成立 |
| 实验二 | 向实验一所得的溶液中加入适量的②_____ | ③_____ | 猜想三成立 |
(2)小明同学为进一步确定上述湖盐样品中Na2CO3的质量分数,取该湖盐样品10.0g做了如图所示的补充实验。(注:所用药品均足量)

①反应结束之后打开止水夹并通入空气的目的是_____。
②装置D中发生的反应为_____(用化学方程式表示)。
③实验中碱石灰(含氧化钙和氢氧化钠)的作用是_____。
④实验结束后,测得装置D增重0.44g,则该湖盐样品中Na2CO3的质量分数为多少_____?
-
(2019河南省实验一模改编)Na2CO3在工业和生活中有重要的作用。它的来源主要有以下两种途径:
Ⅰ、将制碱与制氨结合起来的联合制碱法。这个方法是由我国的制碱工业先驱_____发明的。
A 张青莲 B 道尔顿 C 侯德榜 D 华罗庚
Ⅱ、自然界有很多咸水湖,人们通过“冬天捞碱,夏天晒盐”的方式获得湖盐,其中就含有Na2CO3。
(1)小明同学想对某夏天制得的湖盐样品成分进行探究,查阅资料后他对样品成分做出了三种猜想。猜想一:NaCl、Na2CO3;猜想二:NaCl、Na2SO4;猜想三:NaCl、Na2CO3、Na2SO4.请帮助他完成如下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取少量样品于试管中,加适量水溶解后,加入过量稀HNO3 | 产生能使澄清石灰水变浑浊的气体 | ①猜想_____不成立 |
| 实验二 | 向实验一所得的溶液中加入适量的②_____ | ③_____ | 猜想三成立 |
(2)小明同学为进一步确定上述湖盐样品中Na2CO3的质量分数,取该湖盐样品10.0g做了如图所示的补充实验。(注:所用药品均足量)
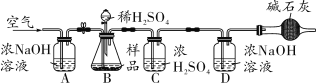
①反应结束之后打开止水夹并通入空气的目的是_____。
②装置D中发生的反应为_____(用化学方程式表示)。
③实验中碱石灰(含氧化钙和氢氧化钠)的作用是_____。
④实验结束后,测得装置D增重0.44g,则该湖盐样品中Na2CO3的质量分数为多少_____?
-
人类的日常生活和工农业生产离不开水,下列说法错误的是( )
A.自来水中只含有水分子
B.海水淡化是人类应对淡水资源短缺的重要途径
C.电解水实验可以证明水由氢氧两种元素组成
D.水体污染的来源主要有工业污染、农业污染和生活污染
-
(2019河南省实验一模改编)水是生命之源,下列关于水的说法正确的是( )
A.硬水中含有较多的Ca2+和Mg2+
B.水的天然循环主要是通过化学变化完成的
C.净化水过程中加明矾可起杀菌作用
D.电解水是一种常用的净水方法
-
(2019河南省实验二模改编)下列生活用品的材质,属于有机合成材料的是( )
A.纯羊毛衫 B.铂金戒指
C.塑料玩具 D.玻璃茶杯
-
纯碱的产量是衡量一个国家化学工业发展水平的重要指标.下面是实验室摸拟侯氏制碱法生产原理的主要过程:

请回答以下问题:
(1)纯碱属于______;
A、碱 B、酸 C、盐 D、无机物
(2)第②步中加入的是磨细食盐粉.食盐磨细的目的是:______;操作a的名称是______;
(3)加入食盐后,请写出发生复分解反应的化学方程式______;
(4)侯氏制碱法的优点之一是所得的副产品氯化铵是一种氮肥.若要通过实验区分氯化铵和另一种氮肥硝酸铵,常用的试剂是______溶液.另一个优点是比较环保,有些物质可以循环再用,你认为该生产流程中,可以循环再利用的物质是______.
-
氧气在人类的生产和生活中有十分重要的作用,请按要求回答以下与氧气制取有关的问题:在之前的学习中,我们了解到有六种途径可以制得氧气,如图1所示:

(1)属于物理变化的途径是____________(填字母代号)。
(2)根据“绿色化学”理念,通常____________ (填字母代号)途径是实验室制氧气的最佳 方法。该反应需要添加一种黑色固体 MnO2 作为催化剂,若反应结束后想要回收该粉末,需对反应后的混合物进行操作,然后对固体进行洗涤和烘干。如图2是实验室制氧气常用的装置

(3)写出装置中仪器的名称:a_____;b_____。
(4)若小明同学选择图中的途径 F 制备并收集较为纯净的氧气,他应在图2中选择的发 生和收集装置分别为____、____,该反应的化学方程式为_________; 若实验收集到的氧气不纯,则可能的错误操作为:_____。
(5)若选择图 1 中的途径 B 制取氧气,则需要在试管口塞一小团棉花,目的是_____, 该反应的化学方程式为 _____。
(6)若使用图中 E 装置来收集氧气,则验满的方法为:_____。
-
纯碱(Na2CO3)是一种重要的有机化工原料。侯氏制碱法制出的纯碱常含少量NaCl杂质,化学兴趣小组对工业纯碱样品进行实验探究。
Ⅰ研究Na2CO3的性质
(1)Na2CO3溶液显____(填“酸性”、“中性”或“碱性”)。
(2)检验样品中碳酸根的方法是____。
Ⅱ设计以下实验方案,测定样品中Na2CO3的质量分数。
[方案一]取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。
(3)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为____。
(4)实验中判断沉淀是否完全的方法是____。
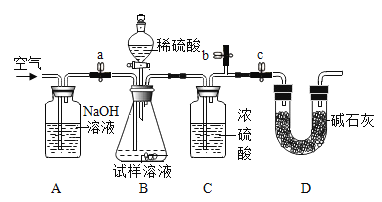
[方案二]采用如图装置,检查装置气密性;称取样品m1g于锥形瓶中,称装置D质量为m2 g;关闭止水夹c,打开止水夹a、b,缓慢鼓入空气数分钟,关闭止水夹a、b,打开止水夹c,缓慢加入稀硫酸至不再产生气体为止;打开止水夹a,缓慢鼓入空气数分钟,再称量装置D质量为m3g。
(查阅资料)浓硫酸具有吸水性,碱石灰的成分为CaO和NaOH固体
(5)装置B中发生的化学方程式为______。
(6)样品中Na2CO3的质量分数的计算式是______。
(7)反应后鼓入空气的目的是______。
(8)该测定结果比实际值偏高,从装置上分析其原因可能是______;改进措施为______。
-
(2019河南省实验二模改编)根据题意书写化学方程式。
(1)稀盐酸除铁锈_____。
(2)用含氢氧化镁的药物治疗胃酸过多_____。
(3)工业上用熟石灰处理含有硫酸的废水_____。
(4)已知过氧化钙(CaO2)和水反应的化学方程式为2CaO2+2H2O =2Ca(OH)2+O2↑,请写出过氧化钙放入碳酸钠溶液中的总化学方程式_____。
-
纯碱(Na2CO3)是一种重要的有机化工原料。侯氏制碱法制出的纯碱常含少量NaCl杂质,化学兴趣小组对工业纯碱样品进行实验探究。
Ⅰ研究Na2CO3的性质
(1)Na2CO3溶液显______(填“酸性”、“中性”或“碱性”)。
(2)检验样品中碳酸根的方法是______。
Ⅱ设计以下实验方案,测定样品中Na2CO3的质量分数。
[方案一]取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。
(3)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为______。
(4)实验中判断沉淀是否完全的方法是______。
[方案二]采用如图装置,检查装置气密性;称取样品m1g于锥形瓶中,称装置D质量为m2 g;关闭止水夹c,打开止水夹a、b,缓慢鼓入空气数分钟,关闭止水夹a、b,打开止水夹c,缓慢加入稀硫酸至不再产生气体为止;打开止水夹a,缓慢鼓入空气数分钟,再称量装置D质量为m3g。
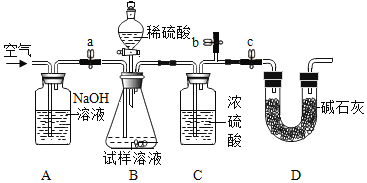
(查阅资料)浓硫酸具有吸水性,碱石灰的成分为CaO和NaOH固体
(5)装置B中发生的化学方程式为______。
(6)样品中Na2CO3的质量分数的计算式是______。
(7)反应后鼓入空气的目的是______。
(8)该测定结果比实际值偏高,从装置上分析其原因可能是______;改进措施为______。






