-
为探究物质间的反应规律,化学兴趣小组的同学做了以下实验,每个实验最后都有一种叫复合肥的物质生成。推出符合a、b、c、d对应的物质是( )
①a+K2SO4→②b+K2O→③c+K2CO3→④d+KOH→
a
b
c
d
A
Ba(NO3)2
HNO3
Ca(NO3)2
Mg(NO3)2
B
Ca(NO3)2
HNO3
M(NO3)2
Ba(NO3)2
C
HNO3
Ba(NO3)2
Ca(NO3)2
Mg(NO3)2
D
Mg(NO3)2
HNO3
Ba(NO3)2
Ca(NO3)2
A. A B. B C. C D. D
九年级化学单选题困难题查看答案及解析
-
某化学兴趣小组的同学进行了如下两个实验探究:
实验探究Ⅰ.怎样证明Ca(OH)2溶液与稀盐酸能发生化学反应?
(查阅资料)根据化学反应的本质:有新物质生成。可从两个方面设计实验证明:一是设计实验证明反应物的消失;二是设计实验证明有新物质生成。
(实验探究)
方案一:在Ca(OH)2溶液中滴入几滴酚酞后再滴加盐酸,当观察到___________时,即可确定二者恰好完全反应。其反应的化学方程式为________。
方案二:在Ca(OH)2溶液滴加盐酸的过程中,用pH试纸不断测量溶液的酸碱度,当pH<7即可确定二者发生了化学反应。实验测得其图象如图。
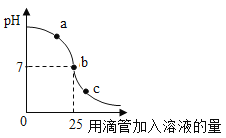
实验探究Ⅱ.探究Ca(OH)2溶液与稀盐酸反应后溶液中溶质的成分。
(猜想)猜想一:CaCl2、Ca(OH)2和HCl;猜想二:CaCl2和Ca(OH)2
猜想三:________(化学式); 猜想四:CaCl2和HCl。
根据所学知识判断,猜想________是一定不成立的。
(查阅资料)氯化钙溶液呈中性。
(进行实验)实验步骤:取少量烧杯内溶液加入试管中,滴入几滴酚酞溶液,振荡。实验现象:_______。结论:猜想二不成立。实验步骤:取少量烧杯内溶液加入另一支试管中,逐滴加入碳酸钠溶液至过量。实验现象:_____。结论:猜想三不成立,猜想四成立。
(反思与拓展)
(1)氢氧化钙固体在空气中变质的化学方程式____________。
(2)酸性较强的液体直接进入下水道,会污染环境。要处理该烧杯内的溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的________。(填化学式)
九年级化学科学探究题困难题查看答案及解析
-
某化学兴趣小组做镁条在空气中燃烧实验时,发现生成物中有黑色固体。针对这一现象,该小组同学猜想可能是镁与N2或CO2反应生成黑色固体。于是他们设计以下实验探究活动:
(提出猜想)猜想I:镁在空气中燃烧产生的黑色固体是镁与N2反应生成的。
猜想Ⅱ:镁在空气中燃烧产生的黑色固体是镁与CO2反应生成的。
(实验一)镁带与氮气的反应
(1)以下是获取氮气的方法及装置,其中得到氮气较纯的是_______(填字母)

(2)燃烧镁带,观察现象:将镁带打磨光亮,点燃,伸入盛N2的集气瓶中,瓶内壁附着一层淡黄色的固体。
(3)实验结论:镁与氮气在点燃的条件下发生化学反应,生成淡黄色的______(用化学式表示)。
(4)实验反思:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁?原因是__________。
(实验二)镁带与二氧化碳的反应
将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内产生氧化镁和一种黑色固体单质,该反应的化学方程式是________。
(探究结论)通过实验可以得出猜想________是正确的。
(反思交流)小组同学通过以上实验发现镁在二氧化碳中也能燃烧,由此他们认为燃烧并不一定需要______。
九年级化学科学探究题简单题查看答案及解析
-
某化学兴趣小组同学,用如图所示三个实验探究质量守恒定律。

(1)充分反应冷却后,天平不能平衡的是______(填字母序号)。我们在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在_____(填“密闭”或“敞口”)装置中进行。
(2)在化学反应前后,一定发生改变的是________(填数字序号)。
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类
(3)铜锈主要成分是碱式碳酸铜[Cu2(OH)2CO3],加热分解的化学方程式为:Cu2(OH)2CO3
2X+H2O+CO2↑,则X的化学式为____。
九年级化学实验题中等难度题查看答案及解析
-
食醋的某些性质与盐酸相似,某化学兴趣小组为探究食醋的化学性质,进行了以下实验:
查阅资料可知:
①盐酸显酸性;酸性物质能使紫色石蕊溶液变红色;
②盐酸能与含碳酸根离子的物质反应生成二氧化碳气体;
③盐酸能与金属活动性排在氢前面的金属发生置换反应。
限选试剂:紫色石蕊溶液,碳酸钙粉末,镁条、铜片。
预测
预测的依据
验证预测的实验操作与预期现象
①食醋显酸性
取少量食醋于试管中,滴加_____,如果观察到_____,则预测成立。
②食醋能与碳酸钙反应
_________
取少量_______加入试管中,滴入少量食醋,如果观察到__________,则预测成立。
③食醋能够与_____ 反应
________
取少量_____加入试管中,滴入少量食醋,如果观察到________,则预测成立。
九年级化学填空题中等难度题查看答案及解析
-
某校化学兴趣小组的同学在探究金属的化学性质时发现:铁粉与硫酸铜溶液反应,不但有铜生成,而且固体中还混有少量的黑色物质,同时有较多气体产生.为确定铁与硫酸铜溶液反应的产物,他们进行了如下的实验探究.
[猜 想]:从物质组成元素角度分析,气体可能是二氧化硫、氧气、氢气中的一种或几种,黑色固体可能是氧化铜或过量的铁粉中的一种或几种.
[实验过程]:
(1)在实验的过程中未能闻到刺激性的气味,则该气体中________二氧化硫(填“有”或“无”).小宝同学认为如有氧气,则可用燃烧的木条来检验.小红认为这种方法存在安全隐患,理由是________.
(2)小林同学为判断是否含有氧气,通过查阅资料得知:O2+4KI+4HCl=2I2+4KCl+2H2O,I2为碘单质.于是他按如图进行实验,
他观察到________,证明无氧气.小军同学用产生的气体吹肥皂泡,发现肥皂泡________,证明该气体是氢气.
(3)小靖同学把铁粉和硫酸铜溶液反应后的固体放入________中,她根据看到的现象判定黑色固体仅为氧化铜.
(4)由上述实验可知,硫酸铜溶液显________性(填“酸”或“碱”).本实验不适宜用石蕊试液检验硫酸铜溶液酸碱性的原因是________.
(5)根据实验探究的结果得到:铁放入硫酸铜溶液中发生反应的化学反应方程式有
①CuSO4+2H2O=Cu(OH)2+H2SO4(水解反应),②CuSO4+Fe=Cu+FeSO4,
③________,④________.
[反思]:若将铁粉换成铁块,则氢气吹肥皂泡实验可能无法获得成功,原因是________.
九年级化学填空题中等难度题查看答案及解析
-
某校化学兴趣小组的同学在探究金属的化学性质时发现:铁粉与硫酸铜溶液反应,不但有铜生成,而且固体中还混有少量的黑色物质,同时有较多气体产生.为确定铁与硫酸铜溶液反应的产物,他们进行了如下的实验探究.
[猜 想]:从物质组成元素角度分析,气体可能是二氧化硫、氧气、氢气中的一种或几种,黑色固体可能是氧化铜或过量的铁粉中的一种或几种.
[实验过程]:
(1)在实验的过程中未能闻到刺激性的气味,则该气体中________二氧化硫(填“有”或“无”).小宝同学认为如有氧气,则可用燃烧的木条来检验.小红认为这种方法存在安全隐患,理由是________.
(2)小林同学为判断是否含有氧气,通过查阅资料得知:O2+4KI+4HCl=2I2+4KCl+2H2O,I2为碘单质.于是他按如图进行实验,
他观察到________,证明无氧气.小军同学用产生的气体吹肥皂泡,发现肥皂泡________,证明该气体是氢气.
(3)小靖同学把铁粉和硫酸铜溶液反应后的固体放入________中,她根据看到的现象判定黑色固体仅为氧化铜.
(4)由上述实验可知,硫酸铜溶液显________性(填“酸”或“碱”).本实验不适宜用石蕊试液检验硫酸铜溶液酸碱性的原因是________.
(5)根据实验探究的结果得到:铁放入硫酸铜溶液中发生反应的化学反应方程式有
①CuSO4+2H2O=Cu(OH)2+H2SO4(水解反应),②CuSO4+Fe=Cu+FeSO4,
③________,④________.
[反思]:若将铁粉换成铁块,则氢气吹肥皂泡实验可能无法获得成功,原因是________.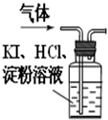
九年级化学填空题中等难度题查看答案及解析
-
合肥市某中学化学兴趣小组按照课本实验方法,做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。
(提出问题)
暗红色的固体是什么?如何选择合适的条件,使木炭还原氧化铜的实验现象更明显?
(查阅资料)
铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,碳的化合价为+4或-4.
(猜想与假设)
(1)同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为______。
(2)同学们还认为,通过改变反应物的状态、质量比,以及反应装备,可以使该实验现象更加明显,减少出现暗红色固体的情况。
(分析与交流)
(1)小吴建议用超细炭粉与氧化铜粉末进行实验。你认为这样建议的原理是______。
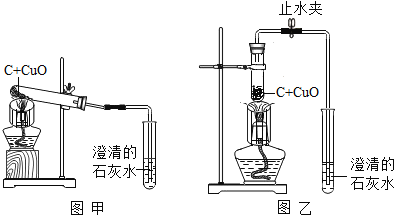
(2)小周建议用图中的乙装置替代甲装置。与甲相比较,乙装置中将试管直立放置的作用是______。
(3)对下列三种氧化铜和碳的质量比例,小施建议选择______(填选项序号)的比例。
A.32:3 B.40:3 C.48:3
(实验与结论)
①同学们决定按改进后的方案进行实验,他们在检验了乙装置的______后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时,______(填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。
②不久,即可看到试管底部变红热,停止加热后,仍然看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是______(填“吸”或“放”)热反应。
③待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却。若不关闭止水夹,可能出现的问题是______。待产物冷却后,同学们终于找到了期待已久的此红色铜球,实验获得了圆满成功。
九年级化学科学探究题困难题查看答案及解析
-
合肥市某中学化学兴趣小组按照课本实验方法 ,做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。

【提出问题】暗红色的固体是什么?如何选择合适的条件,使木炭还原氧化铜的实验现象更明显?
【查阅资料】铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,碳的化合价为+4或-4。
【猜想与假设】
(1)同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为__________________。
(2)同学们还认为,通过改变反应物的状态、质量比,以及反应装置,可以使该实验现象更加明显,减少出现暗红色固体的情况。
【分析与交流】
(1)小吴建议用超细炭粉与氧化铜粉末进行实验。你认为这样建议的原理是__________________________________________________。
(2)小周建议用图中的乙装置替代甲装置。与甲相比较,乙装置中将试管直立放置的作用是__________________________________________。
(3)对下列三种氧化铜和碳的质量比例,小施建议选择___________(填选项序号)的比例。
A. 32︰3 B. 40︰3 C. 48︰3
你认为小施这样选择的理由是__________________________________________________。
【实验与结论】
同学们决定按改进后的方案进行实验,他们在检验了乙装置的__________后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时,________(填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。
不久,即可看到试管底部变红热,停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是________(填“吸”或“放”)热反应。
待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却。若不关闭止水夹,可能出现的问题是____________________________________________。
待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
九年级化学探究题困难题查看答案及解析
-
某校化学兴趣小组就空气中氧气的含量进行实验探究。
(小组讨论)(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应而且生成物为固体。他们应该选择的物质是________(填序号)。
A.蜡烛 B.红磷 C.硫 D.木炭
为了充分消耗容器中的氧气,药品的用量应保证_________________。
(2)小组同学共同设计下图所示的两套装置,你认为合理的是________(填序号)。为了确保实验的成功,在装药品之前应该进行的操作是_______________________________。
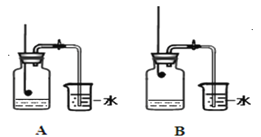
(小组实验)在讨论的基础上,他们分组进行了实验。
(数据分析)实验结束后,整理数据如下:(注:集气瓶容积为100 mL)
组别
1
2
3
4
5
6
进入集气瓶中水的体积/mL
20
21
19
20
22
19
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的________。通过实验还可以推断集气瓶中剩余气体的性质是_____________________(答一点即可)。
九年级化学实验题简单题查看答案及解析