-
某校甲、乙两兴趣小组进行硫酸铜溶液与与氢氧化钠溶液的实验。
甲组实验:先往试管中各加入2mL 10%的CuSO4溶液,再往试管中加入5mL 10%的NaOH溶液,观察到试管中有蓝色沉淀生成。
乙组实验:先往试管中各加入2mL 10%的CuSO4溶液,再往试管中加入2滴10%的NaOH溶液,观察到试管中有浅绿色沉淀生成(与甲组的沉淀颜色差别较大)。
【实验讨论】甲组实验中的蓝色沉淀是氢氧化铜,写出反应的化学方程式: 。
那么乙组实验中浅绿色沉淀是什么呢?
【查阅资料】
(1)NaOH溶液和CuSO4溶液反应可生成多种组成的碱式硫酸铜,它们都是浅绿色固体。如Cu2(OH)2SO4、Cu3(OH)4SO4或Cu4(OH)6SO4,它们的相对分子质量分别为258、356、454。
(2)各种组成的碱式硫酸铜,受热均会分解。
(3)SO2气体能使酸性高锰酸钾稀溶液褪色。
(4)白色的无水CuSO4固体吸收水蒸气后变成变蓝色固体。
【实验探究】该小组对碱式硫酸铜产生了兴趣,想探究碱式硫酸铜受热分解的产物。
【实验设计】取少量碱式硫酸铜加入试管中并按以下流程进行实验:
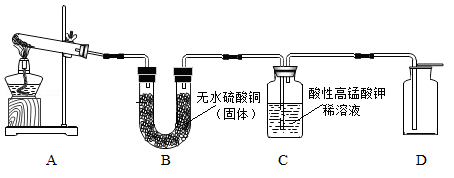
实验结束后,试管中残留有黑色固体,滴入稀硫酸黑色固体溶解,溶液呈蓝色,证明黑色固体是CuO;B中无水CuSO4变蓝色,证明有 生成;C中现象为 ,证明生成SO2;D中气体能使带火星木条复燃,证明生成O2.
【实验反思】
(1)当NaOH溶液和CuSO4溶液反应时,只要控制CuSO4溶液的量一定,NaOH溶液 (填“过量”或“不足”)时就能生成浅绿色沉淀。
(2)若碱式硫酸铜Cu3(OH) 4SO4可表示为:2Cu(OH)2• CuSO4,则Cu4(OH)6SO4还可表示为: 。
【拓展延伸】
(1)当反应物相同,而反应物的量不同,产物可能不同。试另举一个例子: 。
(2)当反应物相同,而 不同时,产物也可能不同。如常温下二氧化碳和水反应生成碳酸;在光照作用下,二氧化碳和水在植物的叶子中发生光合作用生成氧气。
(3)为了确定所得浅绿色沉淀的组成,再进行后续实验,取8.9g碱式硫酸铜(假设化学式为:aCu(OH)2• bCuSO4)放入试管中加热,充分反应后生成了0.9g水,通过计算确定所得浅绿色沉淀的化学式为 。
-
某兴趣小组向甲、乙试管中各加入2mL 10%的CuSO4溶液,再向两支试管中加入10%的NaOH溶液,甲试管中加入5mL、乙试管中加入2滴,振荡后观察到甲试管中有蓝色沉淀生成,乙试管中有浅绿色沉淀生成。

(实验讨论)得到的蓝色沉淀一定是氢氧化铜,写出反应的化学方程式:_____,那么浅绿色沉淀是什么呢?
(查阅资料)(1)NaOH溶液和CuSO4溶液反应可生成碱式硫酸铜,它是浅绿色固体,受热会分解;
(2)碱式硫酸铜有多种可能的组成,如Cu2(OH)2SO4、Cu3(OH)4SO4或Cu4(OH)6SO4;
(3)SO2气体能使酸性高锰酸钾溶液褪色。
(实验探究)该小组对碱式硫酸铜产生了兴趣,想探究碱式硫酸铜受热分解的产物。
(实验设计)取少量碱式硫酸铜加入试管中并按以下流程进行实验:
实验结束后,试管A中残留有黑色固体,滴入稀硫酸后观察到_____的现象,证明该黑色固体是氧化铜;B中无水硫酸铜变为蓝色,证明有水生成;C中酸性高锰酸钾溶液褪色,证明生成_____;D中气体能使带火星木条复燃,证明有_____生成;
(实验反思)
(1)当NaOH溶液和CuSO4溶液反应时,只要CuSO4溶液的量一定,NaOH溶液_____(填“过量”或“不足”)时就能生成浅绿色沉淀;
(2)碱式硫酸铜可表示为:aCu(OH)2•bCuSO4,如将Cu4(OH)6SO4改写该表示方式,则a与b的比值为_____;
(拓展延伸)当反应物的量不同,产物可能不同,试另举一个例子:_____。
-
氢氧化钠与硫酸的反应无明显现象,某化学兴趣小组为证明氢氧化钠与硫酸发生了化学反应,进行了如下的实验探究.
【实验探究】
小倩在试管中加入约2ml稀氢氧化钠溶液,滴入2滴酚酞溶液,振荡,溶液变为红色.然后向该试管中倒入稀硫酸观察到溶液由红色变为无色,证明氢氧化钠与硫酸发生了反应该反应的化学方程式为________.
【改进实验】
小娜使用与小倩相同的试剂,通过改进上述实验中某一步的操作方法,不但证明氢氧化钠与硫酸发生了反应,还能验证二者恰好完全反应.小娜改进的实验操作中关键的一点是________.
【反思评价】
小霞提出也可以使用紫色石蕊溶液代替无色酚酞溶液进行上述实验.你认为________(填“酚酞溶液”或“石蕊溶液”)更适合用于验证二者恰好完全反应,你的理由是________.
【拓展延伸】
不是所有的碱与硫酸反应都无明显现象,例如________(填一种碱)与硫酸反应就有明显的实验现象.
-
氢氧化钠与硫酸的反应无明显现象,某化学兴趣小组为证明氢氧化钠与硫酸发生了化学反应,进行了如下的实验探究.
【实验探究】
小倩在试管中加入约2ml稀氢氧化钠溶液,滴入2滴酚酞溶液,振荡,溶液变为红色.然后向该试管中倒入稀硫酸观察到溶液由红色变为无色,证明氢氧化钠与硫酸发生了反应该反应的化学方程式为 ________ .
【改进实验】
小娜使用与小倩相同的试剂,通过改进上述实验中某一步的操作方法,不但证明氢氧化钠与硫酸发生了反应,还能验证二者恰好完全反应.小娜改进的实验操作中关键的一点是 ________ .
【反思评价】
小霞提出也可以使用紫色石蕊溶液代替无色酚酞溶液进行上述实验.你认为 ________ (填“酚酞溶液”或“石蕊溶液”)更适合用于验证二者恰好完全反应,你的理由是 ________ .
【拓展延伸】
不是所有的碱与硫酸反应都无明显现象,例如 ________ (填一种碱)与硫酸反应就有明显的实验现象.
-
下面呈现的是某实验小组在课堂上做的一组探究实验:
(1)在a试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的现象是_____。

(2)向b、c两支试管中各加入少量相同质量的氢氧化钙粉末,然后各加入1mL水,振荡,呈浑浊状,静置,再各滴入1~2 滴酚酞溶液,观察到两试管溶液均变红。继续向b试管中加入约1mL水振荡;向c试管中加入约1mL稀盐酸,振荡。发现b试管变澄清,溶液仍呈红色,c试管变澄清,溶液变成无色。向b试管中第二次加入约1mL水的作用是________。
(提出问题)试管c中加入约1mL稀盐酸后,溶液中的溶质是什么?
(查阅资料)查阅资料:CaCl2溶液呈中性。
(猜想假设)小丽猜想:I.CaCl2 Ⅱ.CaCl2和HCl Ⅲ.CaCl2和Ca(OH)2
(反思质疑)小明对猜想Ⅲ产生质疑,理由是___________
(进行实验)小组同学通过交流,设计如下实验方案进行验证:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量c试管中的溶液于试管中,_______ | ________ | 猜想Ⅱ成立 |
实验结束,小组同学将a、b、c三支试管中的剩余物质混合,发现废液呈浑浊。
(问题与交流)废液中大量存在的阳离子有_______。写出废液中可能发生反应的一个化学方程式________。
-
下面呈现的是某实验小组在课堂上做的一组探究实验:
(1)在a试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的现象是_____。

(2)向b、c两支试管中各加入少量相同质量的氢氧化钙粉末,然后各加入1mL水,振荡,呈浑浊状,静置,再各滴入1~2 滴酚酞溶液,观察到两试管溶液均变红。继续向b试管中加入约1mL水振荡;向c试管中加入约1mL稀盐酸,振荡。发现b试管变澄清,溶液仍呈红色,c试管变澄清,溶液变成无色。向b试管中第二次加入约1mL水的作用是________。
(提出问题)试管c中加入约1mL稀盐酸后,溶液中的溶质是什么?
(查阅资料)查阅资料:CaCl2溶液呈中性。
(猜想假设)小丽猜想:I.CaCl2 Ⅱ.CaCl2和HCl Ⅲ.CaCl2和Ca(OH)2
(反思质疑)小明对猜想Ⅲ产生质疑,理由是___________
(进行实验)小组同学通过交流,设计如下实验方案进行验证:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量c试管中的溶液于试管中,_______ | ________ | 猜想Ⅱ成立 |
实验结束,小组同学将a、b、c三支试管中的剩余物质混合,发现废液呈浑浊。
(问题与交流)废液中大量存在的阳离子有_______。写出废液中可能发生反应的一个化学方程式________。
-
下面呈现的是某实验小组在课堂上做的一组探究实验:
(1)在a试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的现象是_____。

(2)向b、c两支试管中各加入少量相同质量的氢氧化钙粉末,然后各加入1mL水,振荡,呈浑浊状,静置,再各滴入1~2 滴酚酞溶液,观察到两试管溶液均变红。继续向b试管中加入约1mL水振荡;向c试管中加入约1mL稀盐酸,振荡。发现b试管变澄清,溶液仍呈红色,c试管变澄清,溶液变成无色。向b试管中第二次加入约1mL水的作用是________。
(提出问题)试管c中加入约1mL稀盐酸后,溶液中的溶质是什么?
(查阅资料)查阅资料:CaCl2溶液呈中性。
(猜想假设)小丽猜想:I.CaCl2 Ⅱ.CaCl2和HCl Ⅲ.CaCl2和Ca(OH)2
(反思质疑)小明对猜想Ⅲ产生质疑,理由是___________
(进行实验)小组同学通过交流,设计如下实验方案进行验证:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量c试管中的溶液于试管中,_______ | ________ | 猜想Ⅱ成立 |
实验结束,小组同学将a、b、c三支试管中的剩余物质混合,发现废液呈浑浊。
(问题与交流)废液中大量存在的阳离子有_______。写出废液中可能发生反应的一个化学方程式________。
-
某兴趣小组想通过实验对铁、铜、锌三种金属的活动性强弱进行探究,现提供的药品有:铁粉、铜丝、锌粒、20%稀硫酸、CuSO4,溶液、ZnSO4溶液、FeSO4溶液同学们分成甲乙两组进行了实验。
(1)甲组同学设计如下方案进行实验:
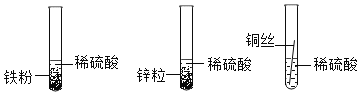
立刻有同学提出反对,理由是___________。
(2)乙组同学设计如下方案进行试验:
| 实验步骤 | 
| 
|
| 实验现象 | 无明显变化 | _____________ |
| 实验结论 | ________________ |
发生反应的化学方程式为________________________。
(3)乙组同学将两支试管中的物质倒在一个洁净的烧杯中,发现烧杯内的红色固体明显增多。充分反应后过滤,同学们又对滤渣的成分展开了探究。
(作出猜想)猜想一:滤渣中一定有铜 猜想二:________
(进行实验)
| 实验步骤 | 实验现象 | 实验结论 |
| 向滤渣中加入__________ | 有气泡产生 | 猜想二正确 |
此时滤液中含有的溶质是______(填化学式)。
(4)(拓展延伸) 通过学习同学们掌握了比较金属活动性的正确方法,同时又选择了另一组试剂_____,进一步验证了三种金属的活动性强弱。
-
某兴趣小组的同学们围绕“酸碱中和反应”,将学生成分若干小组开探宂活动。请你和他们一起完成以下实验探究。
(提出问题一)稀硫酸与氢氧化钠溶液能否发生反应
(实验探究1)甲组同学在烧杯中加入10mL稀硫酸。滴入几滴酚酞试液,接着分两次向烧杯中滴入氢氧化钠溶液。第一次滴加几滴氢氧化钠溶液后,不断搅拌,第二次继续滴加氢氧化钠溶液至过量。则第一次滴加氢氧化钠溶液时,溶液中溶质(不考虑酚酞)的质量变化情况是(1)_________;第二次滴加氢氧化钠溶液时观察到的现象是(2)_________。由上述实验甲组同学得出了稀硫酸与氢氧化钠溶液能发生反应的结论。反应的化学方程为(3)________。
(提出问题二)是否可以用其他试剂证明稀硫酸与氢氧化钠溶液能发生反应呢?
(实验探究2)同学们想要利用找到的生锈的铁钉继续探究,并设计了如下实验方案。
乙组同学的实验过程如图所示:向a试管中滴加氢氧 化钠溶液时无明显现象,再将混合后的溶液倒入盛有生锈铁钉的另一试管中,观察到(4)______的明显现象。
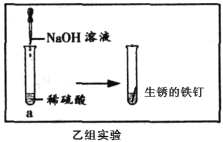
乙组结论:生锈的铁钉可以证明稀硫酸与氢氧化钠溶液能发生反应。
丙组同学的实验过程与乙组相同,但是丙组同学却未观察到明显现象。
丙组结论:生锈的铁钉可以证明稀硫酸与氢氧化钠溶液能发生反应。
(交流讨论)你认为乙、丙两组中哪个小组由实验现象获得的结论是正确的,并说明理由(5)_________。
(反思)若化学反应无明显现象时,可通过证明(6)________来判断有化学反应发生。
-
(8分)氢氧化钠与盐酸的反应无明显现象,某化学兴趣小组为证明氢氧化钠与盐酸发生了化学反应,进行了如下的实验探究。
【实验探究一】小云在试管中加入约2mL稀氢氧化钠溶液,滴入2滴酚酞溶液,振荡,溶液变为红色。然后向该试管中滴加稀盐酸,观察到溶液 ,证明氢氧化钠与盐酸发生了反应,该反应的化学方程式为 。
【反思评价】 小霞提出也可以使用石蕊试液代替无色酚酞进行上述实验。你认为 (填“无色酚酞”或“石蕊试液”)更适合用于验证二者恰好完全反应,你的理由是 。
【实验探究二】小兰同学将不同浓度的盐酸和NaOH溶液各10 mL混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表)。
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65﹪ | 2.00﹪ | 3.5 |
| 2 | 3.65﹪ | 4.00﹪ | x |
| 3 | 7.30﹪ | 8.00﹪ | 14 |
表中x = 。
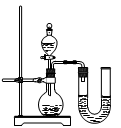
【反思评价】某同学在没使用温度计的情况下,通过右图所示装置完成了实验。则该同学根据
判断NaOH溶液与稀盐酸发生了中和反应。但有同学认为单凭此现象不足以说明该反应放热,其理由是 。
【拓展延伸】不是所有的碱与盐酸反应都无明显现象,例如 (填一种碱)与盐酸反应就有明显的实验现象。







