海水晒盐制得的粗盐中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4等可溶性杂质,如图是进行粗盐提纯的实验步骤。
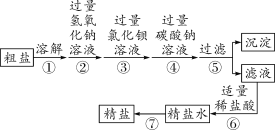
请回答下列问题:
(1)步骤①⑤⑦都用到的玻璃仪器是________,该仪器在步骤⑦中的作用是什么________?
(2)写出该实验过程中发生中和反应的化学方程式________。
(3)能否将氢氧化钠换成氢氧化钙,并给出你的理由________。
九年级化学简答题中等难度题
海水晒盐制得的粗盐中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4等可溶性杂质,如图是进行粗盐提纯的实验步骤。

请回答下列问题:
(1)步骤①⑤⑦都用到的玻璃仪器是________,该仪器在步骤⑦中的作用是什么________?
(2)写出该实验过程中发生中和反应的化学方程式________。
(3)能否将氢氧化钠换成氢氧化钙,并给出你的理由________。
九年级化学简答题中等难度题
海水晒盐制得的粗盐中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4等可溶性杂质,如图是进行粗盐提纯的实验步骤。

请回答下列问题:
(1)步骤①⑤⑦都用到的玻璃仪器是________,该仪器在步骤⑦中的作用是什么________?
(2)写出该实验过程中发生中和反应的化学方程式________。
(3)能否将氢氧化钠换成氢氧化钙,并给出你的理由________。
九年级化学简答题中等难度题查看答案及解析
(12分)盐城濒临黄海,海洋资源非常丰富。
(1)海水晒盐得到的粗盐中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
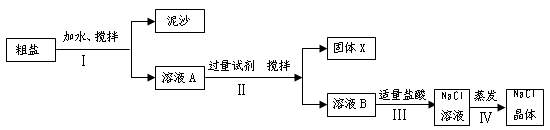
请回答下列问题
①海水是 (填“纯净物”或“混合物”) 海水晒盐得到粗盐是_____变化(填“物理”或“化学”)_
②步骤Ⅰ和步骤Ⅱ都涉及到的实验操作是 。
③步骤Ⅳ加热蒸发时,待 时停止加热。
④为了除去溶液A中的可溶性杂质,步骤Ⅱ中加入过量的试剂是Na2C03、NaOH、BaCl2 , 写出步骤Ⅲ中加入适量盐酸时发生的中和反应的化学方程式 。如果步骤Ⅱ中加入过量的试剂顺序不当,将导致得不到纯净的NaCl,下列加入试剂顺序不当的是
A Na2C03、NaOH、BaCl2 B BaCl2、NaOH 、Na2C03
C NaOH、BaCl2、Na2C03 D.Na2C03、BaCl2 、NaOH E. BaCl2、Na2C03、NaOH
(2)某实验小组利用上面提纯的氯化钠,配置100g 16%的氯化钠溶液。
①他应称取氯化钠质量是 g ,量水时选用量筒的量程最好是
A.10ml B.20ml C.50ml D.100ml
②称量氯化钠时发现天平的指针偏左,正确的处理方法是
A.增加砝码 B.减少药品 C.减少砝码 D.增加药品
③实验中实际配制的溶液中溶质质量分数小于16%,造成的可能原因有__ ; _;(不少于两点)
九年级化学探究题困难题查看答案及解析
潍坊海水资源丰富,从海水得到的粗盐往往含有可溶性杂质(MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活。实验室模拟工业粗盐提纯的流程如图,请回答:
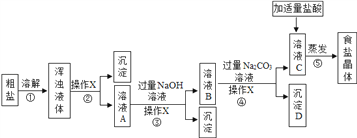
(1)操作X的名称是_____,该操作中用到的玻璃仪器有烧杯、玻璃棒和______。
(2)加适量盐酸的目的是____________________________________________。
(3)生成沉淀D的化学方程式为_____________________________ 。
(4)下图为氯化钠、碳酸钠在水中的溶解度曲线。 请回答下列问题。
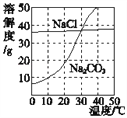
①30℃时,将等质量的两种物质的饱和溶液同时降温至10℃,晶体析出后所得氯化钠溶液的溶质质量分数___(填“>”“<”或“=”)碳酸钠溶液的溶质质量分数。
②在20℃时,各取NaCl、Na2CO3固体30g,分别加入100g水,充分溶解后达到饱和状态的物质是_____。
九年级化学流程题困难题查看答案及解析
潍坊海水资源丰富,从海水得到的粗盐往往含有可溶性杂质(MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活。实验室模拟工业粗盐提纯的流程如图,请回答:
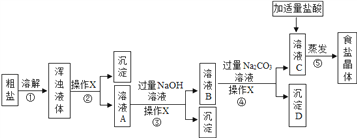
(1)操作X的名称是_____,该操作中用到的玻璃仪器有烧杯、玻璃棒和______。
(2)加适量盐酸的目的是____________________________________________。
(3)生成沉淀D的化学方程式为_____________________________ 。
(4)下图为氯化钠、碳酸钠在水中的溶解度曲线。 请回答下列问题。
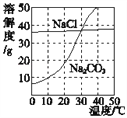
①30℃时,将等质量的两种物质的饱和溶液同时降温至10℃,晶体析出后所得氯化钠溶液的溶质质量分数___(填“>”“<”或“=”)碳酸钠溶液的溶质质量分数。
②在20℃时,各取NaCl、Na2CO3固体30g,分别加入100g水,充分溶解后达到饱和状态的物质是_____。
九年级化学流程题困难题查看答案及解析
从海水中得到的粗盐中往往含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能使用。实验室粗盐提纯的部分流程如图,有关该流程说法错误的是()
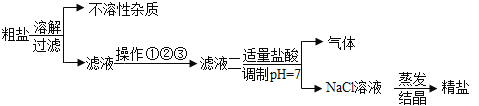
A.不溶性杂质主要是泥沙
B.过滤时要用玻璃棒引流
C.蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干
D.操作①②③依次加入的试剂可以为Na2CO3溶液、NaOH溶液、BaCl2溶液。
九年级化学单选题中等难度题查看答案及解析
从海水中得到的粗盐中往往含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能使用。实验室粗盐提纯的部分流程如图,有关该流程说法错误的是()
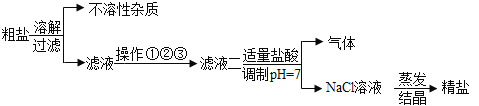
A.不溶性杂质主要是泥沙
B.过滤时要用玻璃棒引流
C.蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干
D.操作①②③依次加入的试剂可以为Na2CO3溶液、NaOH溶液、BaCl2溶液。
九年级化学单选题中等难度题查看答案及解析
现有一定质量含有少量泥沙等不溶性杂质和少量Na2SO4,MgCl2,CaCl2等可溶性杂质的粗盐样品,某实验小组利用化学实验室常用仪器对粗盐样品进行提纯,提纯步骤如下: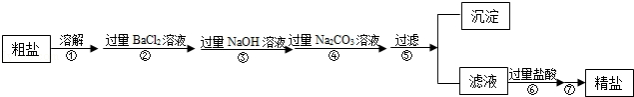
请根据提纯步骤回答下列问题.
(1)步骤⑦的操作名称为 .
(2)请写出实验步骤②中所涉及的化学方程式 .
(3)步骤⑥中加入过量盐酸的目的是 .
(4)步骤②和步骤④ (填“可以”或“不可以”)颠倒,理由是 .
(5)检验步骤④中Na2CO3溶液已过量的方法是 .
(6)加碘食盐相关信息如图所示.

食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),化学方程式如下:
KIO3+5KI+6HCl=6KCI+3I2+3H2O
①向装有碘化钾和淀粉混合液的试管中,滴入稀盐酸将溶液酸化,再加入食盐,若食盐中有碘化钾,则加入食盐后的实验现象 .
②小强同学欲测定加碘盐中碘元素的质量分数,实验步骤如下:取10g食盐样品于试管中加水溶解,加入过量KI的和淀粉混合溶液,再滴入稀盐酸将溶液酸化使其充分反应后,调节溶液呈中性,再向试管中滴加硫代硫酸钠溶液(Na2S2O3),发生化学反应方程式为:2Na2S2O3+I2═Na2S4O6+2NaI
当加入质量分数为0.237%Na2S2O3溶液2g时,I2恰好反应完全,通过计算判断该食盐样品是否合格(已知Na2S2O3的相对分子质量为158.请写出计算过程).
九年级化学计算题中等难度题查看答案及解析
现有一定质量含有少量泥沙等不溶性杂质和少量Na2SO4,MgCl2,CaCl2等可溶性杂质的粗盐样品,某实验小组利用化学实验室常用仪器对粗盐样品进行提纯,提纯步骤如下: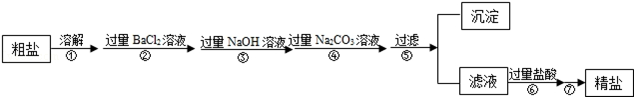
请根据提纯步骤回答下列问题.
(1)步骤⑦的操作名称为________.
(2)请写出实验步骤②中所涉及的化学方程式________.
(3)步骤⑥中加入过量盐酸的目的是________.
(4)步骤②和步骤④________(填“可以”或“不可以”)颠倒,理由是________.
(5)检验步骤④中Na2CO3溶液已过量的方法是________.
(6)加碘食盐相关信息如图所示.
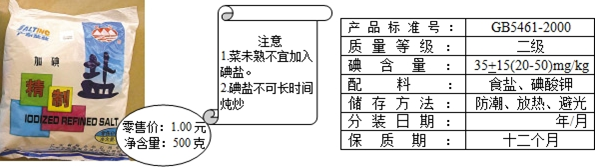
食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),化学方程式如下:
KIO3+5KI+6HCl=6KCI+3I2+3H2O
①向装有碘化钾和淀粉混合液的试管中,滴入稀盐酸将溶液酸化,再加入食盐,若食盐中有碘化钾,则加入食盐后的实验现象________.
②小强同学欲测定加碘盐中碘元素的质量分数,实验步骤如下:取10g食盐样品于试管中加水溶解,加入过量KI的和淀粉混合溶液,再滴入稀盐酸将溶液酸化使其充分反应后,调节溶液呈中性,再向试管中滴加硫代硫酸钠溶液(Na2S2O3),发生化学反应方程式为:2Na2S2O3+I2═Na2S4O6+2NaI
当加入质量分数为0.237%Na2S2O3溶液2g时,I2恰好反应完全,通过计算判断该食盐样品是否合格(已知Na2S2O3的相对分子质量为158.请写出计算过程).
九年级化学计算题中等难度题查看答案及解析
现有一定质量含有少量泥沙等不溶性杂质和少量Na2SO4,MgCl2,CaCl2等可溶性杂质的粗盐样品,某实验小组利用化学实验室常用仪器对粗盐样品进行提纯,提纯步骤如下: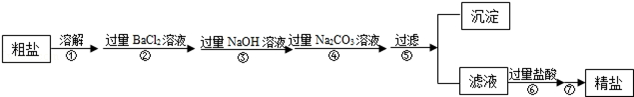
请根据提纯步骤回答下列问题.
(1)步骤⑦的操作名称为________.
(2)请写出实验步骤②中所涉及的化学方程式________.
(3)步骤⑥中加入过量盐酸的目的是________.
(4)步骤②和步骤④________(填“可以”或“不可以”)颠倒,理由是________.
(5)检验步骤④中Na2CO3溶液已过量的方法是________.
(6)加碘食盐相关信息如图所示.
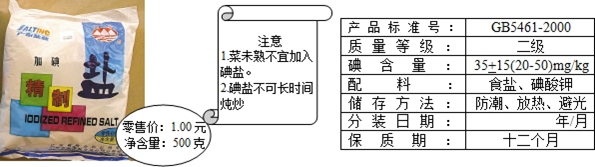
食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),化学方程式如下:
KIO3+5KI+6HCl=6KCI+3I2+3H2O
①向装有碘化钾和淀粉混合液的试管中,滴入稀盐酸将溶液酸化,再加入食盐,若食盐中有碘化钾,则加入食盐后的实验现象________.
②小强同学欲测定加碘盐中碘元素的质量分数,实验步骤如下:取10g食盐样品于试管中加水溶解,加入过量KI的和淀粉混合溶液,再滴入稀盐酸将溶液酸化使其充分反应后,调节溶液呈中性,再向试管中滴加硫代硫酸钠溶液(Na2S2O3),发生化学反应方程式为:2Na2S2O3+I2═Na2S4O6+2NaI
当加入质量分数为0.237%Na2S2O3溶液2g时,I2恰好反应完全,通过计算判断该食盐样品是否合格(已知Na2S2O3的相对分子质量为158.请写出计算过程).
九年级化学计算题中等难度题查看答案及解析
现有一定质量含有少量泥沙等不溶性杂质和少量Na2SO4,MgCl2,CaCl2等可溶性杂质的粗盐样品,某实验小组利用化学实验室常用仪器对粗盐样品进行提纯,提纯步骤如下:
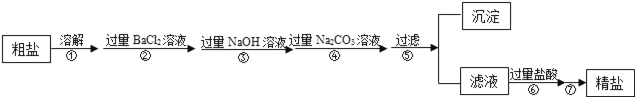
请根据提纯步骤回答下列问题:
(1)步骤⑦的操作名称为___;
(2)请写出实验步骤②中所涉及的化学方程式___;
(3)步骤⑥中加入过量盐酸的目的是___;
(4)步骤②和步骤④___(填“可以”或“不可以”)颠倒,理由是___。
九年级化学简答题简单题查看答案及解析